
Хурсан - Лекции по квантовой механике и квантовой химии / 07Lecture-06
.pdf
Лекция 6. Атомные орбитали.
6.1. Классификация атомных орбиталей.
Таким образом, полная волновая функция водородоподобного атома определена и зависит от трех квантовых чисел: n, l, m. Целочисленные значения и их взаимосвязь обусловлены требованиями конечности и непрерывности волновой функции. Важно, что появление дискретных квантовых чисел автоматически следует из математических условий, налагаемых на волновую функцию, т.е. квантование физических величин естественным образом отражается в математическом аппарате квантовой механики.
Волновую функцию, соответствующую определенному набору квантовых чисел n, l, m называют атомной орбиталью (АО). Каждая АО соответствует определенному электронному состоянию атома водорода. Классификацию АО проводят с помощью квантовых чисел n и l. Причем, как будет показано ниже, число n, называемое главным квантовым числом, определяет уровень энергии орбиталей. Эти уровни нумеруются в соответствии со значением n: первый уровень, второй и т.д. Обозначение орбиталей проводят в соответствии со значением квантового числа l, называемого орбитальным квантовым числом, по следующим правилам:
l |
0 |
1 |
2 |
3 |
4 |
5 |
Обозначение |
s |
p |
d |
f |
g |
h |
Относительная ориентация орбитали в пространстве задается третьим квантовым числом m, называемым магнитным квантовым числом. Здесь следует сделать некоторое отступление. Из выражения для Φ(ϕ) очевидно, что волновые функции с ненулевым магнитным квантовым числом являются комплексными. Между тем, значительно удобнее работать с действительными функциями. Сферические гармоники Yl,m(θ, ϕ) и Yl,-m(θ, ϕ) отвечают вырожденному состоянию, поэтому можно воспользоваться свойством, согласно которому их линейная комбинация также является решением уравнения Шредингера с тем же собственным значением:
Ylm′ = |
1 |
(Yl,m +Yl,−m ); |
Ylm′′ = |
1 |
(Yl,m −Yl,−m ). |
|
2 |
|
|
2 |
|
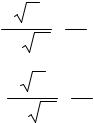
Коэффициенты выводятся из условия нормировки. Кроме того, примем во внимание формулу Эйлера для комплексных чисел:
exp(imϕ) −exp(−imϕ) =sin mϕ ; 2i
exp(imϕ) +exp(−imϕ) = cos mϕ. 2
2
Тогда вместо комплексных функций получим два действительных решения
cos | m | ϕ Ylm (θ,ϕ) = Θlm (θ) sin | m | ϕ ,
где l = 0, 1, 2, …, n – 1; m = 0, 1, 2, …. Для удобства условимся, что отрицательным значениям m соответствует функция синуса, а положительным – косинуса. Тогда, используемая нами в качестве примера волновая функция с n = 3, l = 2, m = ±1 превращается в две, соответствующие орбиталям 3dxz и
3dyz:
|
|
2 |
|
Z |
|
7 / 2 |
|
|
|
− |
Zr |
|
|
|||
|
|
|
|
2 |
|
3a0 |
|
|||||||||
Ψ3,2,1 (r,θ,ϕ) = |
|
|
|
|
|
|
r |
|
e |
|
|
|
|
sinθ cosθ cosϕ. |
||
81 |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
π a0 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
2 |
|
Z |
7 / 2 |
|
|
|
− |
Zr |
|
||||
|
|
|
|
|
2 |
3a0 |
|
|||||||||
Ψ3,2,−1 |
(r,θ,ϕ) = |
|
|
|
|
|
r |
|
e |
|
|
|
sinθ cosθ sinϕ. |
|||
|
|
|
|
|
|
|
|
|
||||||||
|
|
81 |
π a0 |
|
|
|
|
|
|
|
|
|
||||
Компактная форма представления атомной орбитали достигается при комбинировании декартовой и полярной систем координат. Учитывая приведенные выше формулы пересчета, нетрудно получить
Ψ3,2,1 = N x z exp(-Zr/3a0) = Ψ3dXZ ,
Ψ3,2,-1 = N y z exp(-Zr/3a0) = Ψ3dYZ ,
N – нормировочный множитель. Вид волновых функций объясняет причину принятых обозначений соответствующих атомных орбиталей.
6.2. Пространственная структура атомных орбиталей.
Что же представляет собой атомная орбиталь, как она выглядит? К сожалению, волновая функция зависит от трех переменных и ее изображение возможно лишь в четырехмерном пространстве. Поэтому рассмотрим некоторые проекции.
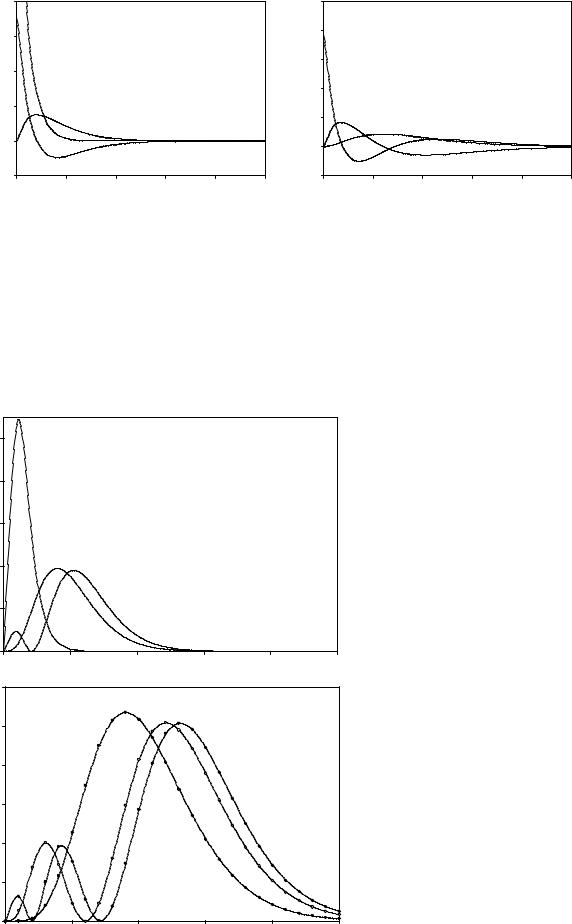
1. Важную информацию дает график зависимости радиальной части волновой функции от r. Для сферически симметричных s-орбиталей, угловые функции которых являются константой, данный график представляет собой характер изменения волновой функции при удалении от ядра. Изменение знака R(r) соответствует изменению знака волновой функции. Точки, в которых радиальная часть обращается в нуль, называются узловыми точками или узлами. Число узлов радиальной части равно n – l – 1.
|
|
|
|
|
3 |
|
0,8 |
|
|
|
|
|
0,5 |
0,6 |
|
|
|
|
|
0,4 |
|
|
|
|
|
|
|
|
1S |
|
|
|
|
0,3 |
0,4 |
|
|
|
|
|
|
R |
|
|
|
|
R |
0,2 |
0,2 |
|
|
|
|
|
|
|
2P |
|
|
|
|
0,1 |
0,0 |
|
|
|
|
|
0,0 |
|
|
|
|
|
|
|
|
2S |
|
|
|
|
|
-0,2 |
|
|
|
|
|
-0,1 |
0 |
5 |
10 |
15 |
20 |
25 |
|
|
3S |
|
|
|
|
|
3P |
3D |
|
|
|
|
|
|
|
|
|
0 |
5 |
10 |
15 |
20 |
25 |
|
|
|
|
r/a0 |
|
|
|
|
|
r/a0 |
|
|
|
|
2. Вероятность нахождения электрона в пространстве между значениями |
||||||||||||
r и r + dr равна: |
|
|
|
|
|
|
|
|
|
|
|||
|
π 2π |
|
|
|
|
|
|
|
|
|
|
|
|
|
∫∫| Ψnlm (r,θ,ϕ) |2 r 2 sinθ dr dθ dϕ =[Rnl (r)]2 r 2 dr × |
|
|
||||||||||
|
0 |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
π 2π |
|
|
|
|
|
|
|
|
|
|
|
|
×∫∫[Ylm (θ,ϕ)]2 sinθ dθ dϕ =[Rnl (r)]2 r 2 dr = Pnl (r)dr. |
|
|||||||||||
|
|
0 |
0 |
|
|
|
|
|
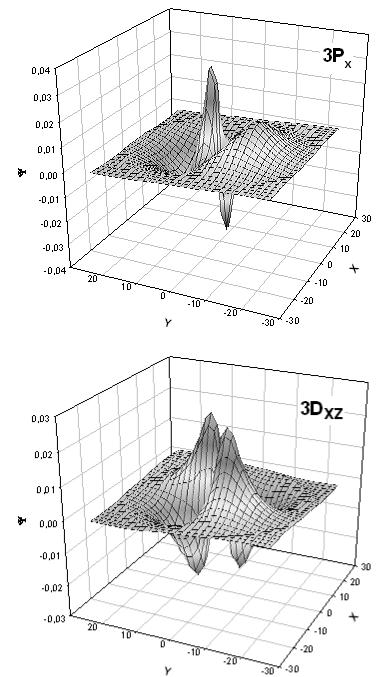
Функцию Pnl(r) назы- |
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
вают радиальной функцией |
|||||
|
0,5 |
|
|
|
|
|
|
распределения. |
|
|
|||
|
1S |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
Эта функция обраща- |
|||||
|
0,4 |
|
|
|
|
|
|
ется в нуль в узловых точ- |
|||||
|
|
|
|
|
|
|
|
||||||
|
0,3 |
|
|
|
|
|
|
ках. |
Из рисунков |
видно, |
|||
P |
|
|
|
|
|
|
что |
наибольшая |
|
вероят- |
|||
|
|
|
|
|
|
|
|
||||||
|
2P |
|
|
|
|
|
ность нахождения электро- |
||||||
|
0,2 |
|
|
|
|
|
|
на на 1S-орбитали в точно- |
|||||
|
|
|
|
|
|
|
|
||||||
|
0,1 |
|
|
2S |
|
|
|
сти |
соответствует |
боров- |
|||
|
|
|
|
|
|
|
скому радиусу a0. Для ор- |
||||||
|
|
|
|
|
|
|
|
||||||
|
0,0 |
|
|
|
|
|
|
биталей |
с n = 2 наиболь- |
||||
|
|
|
|
|
|
|
шая |
вероятность |
соответ- |
||||
|
0 |
|
5 |
10 |
15 |
20 |
25 |
||||||
|
0,12 |
|
|
|
|
|
|
ствует |
~4 – |
5 боровским |
|||
|
|
|
|
|
|
|
|
радиусам и |
~8 – |
14 – для |
|||
|
0,10 |
|
|
|
|
|
|
орбиталей с n = 3. Вместе с |
|||||
|
|
|
3D |
|
|
|
|
тем, |
существует |
конечная |
|||
|
0,08 |
|
|
|
3S |
|
вероятность того, что элек- |
||||||
P |
|
|
|
3P |
|
|
|
троны 2S и 3S (а также с |
|||||
0,06 |
|
|
|
|
|
еще большими значениями |
|||||||
|
|
|
|
|
|
|
|||||||
|
0,04 |
|
|
|
|
|
|
n) находятся в непосредст- |
|||||
|
|
|
|
|
|
|
венной |
близости |
от ядра, |
||||
|
|
|
|
|
|
|
|
||||||
|
0,02 |
|
|
|
|
|
|
r < a0. |
сравнения |
двух |
|||
|
|
|
|
|
|
|
|
|
Из |
||||
|
0,00 |
|
|
|
|
|
|
графиков видно изменение |
|||||
|
0 |
|
5 |
10 |
15 |
20 |
25 |
наиболее вероятного рас- |
|||||
|
|
|
|
|
r/a0 |
|
|
|
|
|
|
|
|
4
стояния электрона от ядра для орбиталей с различными значениями главного и орбитального квантовых чисел.
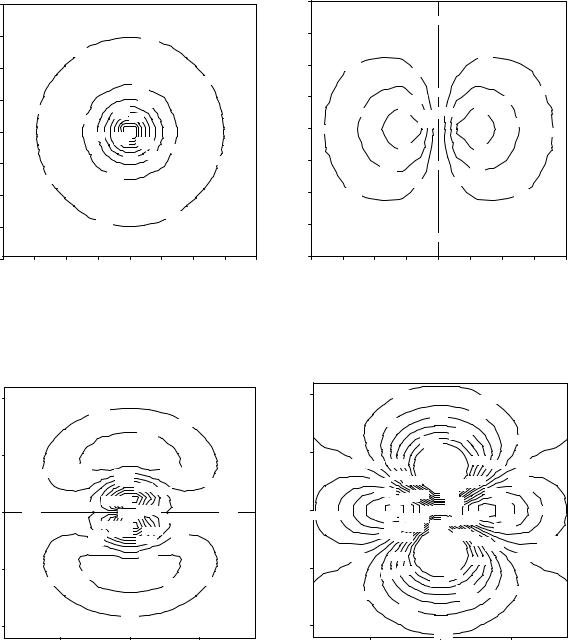
3. Вероятность нахождения электрона в какой-либо точке пространства определяется не только значением r, но также величинами углов θ и ϕ, т.е. зависит как от радиальной, так и от угловой частей атомной орбитали. Графически сферические гармоники строят, соединяя в пространстве все точки, в которых Ylm имеет одно и тоже числовое значение. В результате получаются хорошо известные фигуры: шар для S-орбиталей, объемные вытянутые восьмерки (объемные косинусоиды) для P-орбиталей и т.д.
 Поскольку полная волновая функция является произведением радиальной и угловой частей, то графическое изображение Ψ комбинирует их особенности. Угловая часть задает распределение и знак волновой функции в пространстве, а радиальная часть определяет амплитуду волновой
Поскольку полная волновая функция является произведением радиальной и угловой частей, то графическое изображение Ψ комбинирует их особенности. Угловая часть задает распределение и знак волновой функции в пространстве, а радиальная часть определяет амплитуду волновой
функции и изменение знака Ψ в соответствии с рассмотренными выше графиками. Так, волновая функция 3S-орбитали шарообразна, однако следует иметь в виду, что при удалении от ядра Ψ дважды меняет знак на противоположный. Угловая часть волновой функции 3P-орбитали имеет положительный знак в области положительных значений x и отрицательный – в области –x. Однако, учитывая, что радиальная функция имеет узловую точку в области ~5 боровских радиусов, определяем, что Ψ положительна при 0 < r < 5a0 и ∞ < r < -5a0. Наконец, радиальные части 3D-орбиталей не имеют узлов, по-
этому и форма, и знак Ψ задается угловой частью, а радиальная определяет амплитуду волны.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Pz |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2S |
|
|
|
|
|
|
|
|
|
0,00 |
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
-0,02 |
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
-0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
-0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,02 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
-0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,00 |
|
|
|
|
0,02 |
|
||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
-0,04 |
|
|
|
|
|
|||
|
-0,02 |
|
|
|
0,02 |
|
0,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,04 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,04 |
|
|
-0,06 |
-0,020,020,04 |
|
0,06 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
-0,02 |
|
0,04 |
0,06 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,04 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Z |
0 |
|
|
|
|
-0,04 |
|
|
|
|
|
||||
Z |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,02 |
|
|
|
|
|
|
|
|
||||||
|
|
0,00 |
|
0,100, 2 |
0,06 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,02 |
|
||||||||
|
|
|
|
|
|
0,08 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
0,04 |
|
-0,02 |
|
|
|
|
|
|
|
|
-0,06 |
|
|
|
|
0,06 |
|
|
|||
|
|
|
|
|
|
0,02 |
|
0,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
-2 |
|
|
|
|
|
|
|
-0,02 |
|
|
-2 |
|
|
|
|
|
|
0,00 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,04 |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,04 |
|
|
|||||
|
|
-0,02 |
|
|
-0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,02 |
|
0,02 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-4 |
-0,02 |
|
|
|
|
|
|
|
|
||||
|
-4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,02 |
|
||
|
|
|
|
-0,02 |
|
|
|
|
|
|
-0,02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,00 |
|
|
|
|
|
|
|
-8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-8 |
-6 |
-4 |
-2 |
|
|
0 |
|
|
|
2 |
|
4 |
6 |
8 |
|
-8 |
-6 |
-4 |
|
-2 |
|
|
0 |
|
|
2 |
4 |
6 |
8 |
|
|
|
|
|
|
X |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
X |
|
|
|
|
|
|
|
|
Лучшим способом представления полной волновой функции являются |
|||||||||||||||||||||||||||||
пространственные контурные карты Ψ и Ψ2 от двух переменных (при одной |
||||||||||||||||||||||||||||||
фиксированной). Линии на графиках соединяют точки пространства, в кото- |
||||||||||||||||||||||||||||||
рых волновая функция орбитали имеет одно и то же значение. |
|
|
|
|
|
|||||||||||||||||||||||||
|
20 |
|
|
|
|
|
|
|
|
|
|
|
|
3P |
|
|
20 |
|
|
0,004 |
|
|
|
|
|
|
0,004 |
3Dz2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
-0,005 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,012 |
|
|
0,008 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x |
|
|
|
|
0,008 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
-0,005 |
|
|
|
|
|
|
|
0,016 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
-0,010 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,024 |
0,020 |
|
|
0,004 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
0,028 |
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,0200,008 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,000 0,004 |
0,016 |
|
|
|
|
|
0,000 |
|
|||||
|
|
-0,005 |
|
-0,010 |
|
-0,005 |
|
|
|
-0,010 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,012 |
|
|
|
|
|
|
|
-0,004 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,012 |
|
|||||||
|
|
|
|
|
|
0,005 |
|
|
|
|
|
|
-0,005 |
|
|
|
|
-0,004 |
0,020 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,016 |
|
|
|
|||
|
|
|
|
|
|
|
|
0,010 0,000 |
|
|
|
|
|
|
-0,012 |
|
|
|
0,028 |
|
-0,012 |
-0,008 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,008 |
0,024 |
|
|
|
|||||||||||
|
|
|
|
0,015,030 |
|
|
|
|
|
|
|
|
|
|
|
|
|
- ,008 |
|
|
|
|
|
-0,016 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,016 |
|
|
0,004 |
|
|
|
||||||||
Z |
|
|
|
0,000 |
0,0,0225 |
0, |
0,1005 |
|
|
|
|
Y |
|
|
|
|
|
|
|
|
|
|
-0,008 |
|
||||||
0 |
0,000 |
|
|
|
|
|
|
0,000 |
|
0 |
|
|
|
|
|
0,0000,000 |
|
|
|
|
||||||||||
|
|
|
-0,005 |
|
|
|
|
|
-0,020 |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
-0,010 |
0,000 |
|
|
|
|
-0,004 -0,008 |
-0,016- ,008 |
|
- ,0 |
-0,020 -0,016 |
|
|||||||||||||
|
|
|
|
-0,015-0,030 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,012- |
,00804 |
|
|
|
|||||
|
|
|
|
|
|
-0,010 |
|
|
|
|
|
|
|
|
-0,012 0,004 |
|
0,024 |
|
|
|
-0,012 |
|
||||||||
|
|
|
|
|
|
- , |
|
|
|
0,005 |
|
|
|
|
|
|
|
|
0,028 |
0,020 |
|
|||||||||
|
|
|
|
0,000 -0,0025 |
|
|
|
|
|
|
|
|
|
|
-0,004 |
|
|
|
|
|
|
|||||||||
|
|
|
|
0,005 |
|
|
|
-0,005 |
|
|
|
|
|
|
|
|
|
0,008 |
|
|
0,016 |
|
-0,004 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,008 |
|
||||||
|
|
|
|
|
|
|
|
|
0,010 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,004 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,000 |
|
0,016 |
|
|
|
|
|
0,020 |
0,000 |
|
||||
|
-10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-10 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
0,010 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,020 |
|
0,028 |
|
|
|
|
|
||||
|
|
0,005 |
|
|
|
|
|
|
|
0,010 |
|
0,005 |
|
|
|
|
0,012 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,024 |
0,016 |
|
0,004 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,004 |
|
|
|
|
|
0,008 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,012 |
|
|
|||||
|
|
|
|
|
|
0,005 |
|
|
|
|
|
|
|
|
|
|
|
|
0,008 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
-20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,004 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
-10 |
|
|
|
0 |
|
|
|
|
|
|
10 |
|
|
|
-10 |
|
|
|
|
0 |
|
|
|
|
10 |
|
||
|
|
|
|
|
|
X |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Z |
|
|
|
|
|
|
|
