
- •Российский химико-технологический университет им. Д.И.Менделеева Кафедра общей химической технологии
- •Материальные и тепловые расчеты процесса 2-х ступенчатой конверсии метана в производстве аммиака
- •Задание на курсовую работу
- •Расчетная часть
- •1. Расчет исходных потоков всех компонентов системы.
- •2. Расчет теплового баланса и степени превращения после реактора №1.
- •3. Покомпонентный материальный баланс системы.
- •Описательная часть
- •1) Показать схематично последовательность стадий (привести функциональную схему) производства аммиака из природного газа методом паровоздушной конверсии и дать краткое описание каждой стадии.
- •2)Изобразить схематично все типы химических реакторов, которые используются на различных стадиях производства аммиака с обоснованием их использования.
- •3)Составить структурную схему производства аммиака с указанием основных аппаратов.
- •4) Привести технологическую схему отдельной стадии процесса (по указанию преподавателя). Синтез аммиака3
- •Библиографический список
1) Показать схематично последовательность стадий (привести функциональную схему) производства аммиака из природного газа методом паровоздушной конверсии и дать краткое описание каждой стадии.
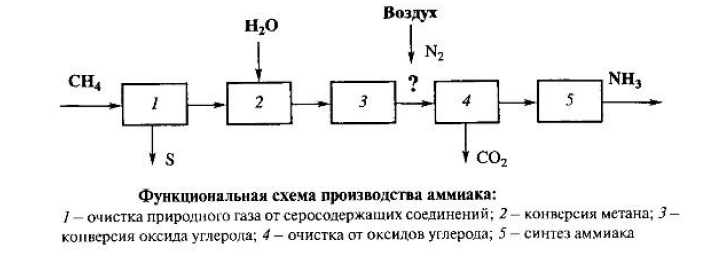
1. Очистка природного газа от серосодержащих соединений2.
Как правило, природный газ содержит в виде примесей сероводород H2S, меркаптаны RSH, тиофен С4Н4S, сероуглерод СS2 и др. соединения. Поэтому первой стадией в производстве аммиака является удаление нежелательных примесей из сырья, которые зачастую являются ядами для катализаторов. Сначала соединения гидрируют до сероводорода:
RSH + H2 = H2S + RH
С4Н4S + 4H2 = H2S + С4Н10
СS2 + 4H2 = 2H2S + СН4
Необходимый водород для гидрирования поступает в виде АВС (азото-водородной смеси) со стадий конверсии метана, температура процесса выше 670К, катализатор – Co-Mo. Вторая ступень очистки - сорбционная чистка в абсорбере с использованием поглотителя оксида цинка:
H2S+ ZnO= ZnS↓+Н2О.
2. Конверсия метана с водяным паром.
И природный газ СН4, и вода Н2O являются сырьем для получения одного из компонентов для синтеза аммиака — водорода Н2. В этом превращении протекают одновременно две реакции:
СН4 + Н2О = СО + 3 Н2;
СО + Н2О = СО2 + Н2.
Конверсия метана протекает с увеличением объема, понижение давления и высокая температура термодинамически выгодны для стадии превращения метана, но не выгоны в целом для процесса, так как синтез аммиака протекает при повышенном давлении 30 МПа. На стадии конверсии метана оптимальным является давление до 4 МПа, а соотношение водяного пара к природному газу целесообразно брать 4:1, температура 1300К. Количество подаваемого воздуха должно обеспечивать соотношение водород:азот = 3:1. Температура газа после конвертера 1230-1280К, давление падает до 3,3 МПа.
3. Конверсия моноокиси углерода с водяным паром.
СО + Н2О = СО2 + Н2.
Конверсия проводится в двух реакторах с различными катализаторами: в первом – Fe-Cr катализатор реагирует при температуре 600-700К, далее после охлаждения реакция протекает во втором реакторе с Сu-содержащим катализатором при температуре 480-540К. Остаточное содержание СО не превышает 0,3-0,5%.
4. Очистка от оксидов углерода СО и СО2.
В конвертированном газе содержание СО не превышает 0,3-0,5%, СО2 до 17-18%. СО является ядом для большинства катализаторов, СО2 – балласт для синтеза аммиака. Эти примеси необходимо удалить. Удаление сорбцией требует специфических сорбентов, необходимых в большом количестве. В настоящее время используется два специфических способа очистки от оксидов углерода.
Диоксид углерода абсорбируют 19-21%-ным водным раствором моноэтиламина (далее – МЭА):
СО2 + 2 RNH2+ Н2О = (RNH3)2CО3.
Эта стадия носит название МЭА-очистки. Поглощение диоксида углерода (карбонизация раствора МЭА) – обратимый процесс: с повышением температуры равновесия сдвигается влево, тем самым позволяя регенерировать сорбент. Поэтому в схеме очистки используются два аппарата: абсорбер и десорбер.
Но раствор МЭА не поглощает оксид углерода, поэтому последний превращают в метан, который безвреден для катализатора и инертен в процессе синтеза аммиака:
СО + 3 Н2 = СН4 + Н2О.
Процесс проводят при низкой температуре (500-550К) с использованием Ni-катализатора при большом избытке водорода (около 75% в АВС).
5. Синтез аммиака.
3 H2 + N2 = 2 NH3.
Синтез аммиака протекает на катализаторе, в качестве которого используют пористое железо с добавками стабилизирующих и промотирующих элементов (алюминий, калий, кальций и др.). Данный катализатор активен и термически устойчив в области температур 650-830К. Реакция обратимая, экзотермическая и протекает с уменьшением объема, следовательно, понижение температуры и повышение давления приводят к увеличению выхода продукта. Оптимальным давлением является 30-32 МПа, выход целевого продукта составляет 16%, для полноты использования АВС используют рецикл, часть газа при этом из рецикла выводится.
