
Органическая химия - Лекции - МГУ - Ненайденко - 2004 / Лекция 4 - Карбоновые кислоты и их производные - 2
.pdf
Лекция 4
Карбоновые кислоты и их производные - 2

Декарбоксилирование карбоновых кислот Галогенирование
кислот по Гелю-Фольгарду-Зелинскому. Реакция Бородина-
Хунсдиккера. Пиролитическая кетонизация, электролиз солей
карбоновых кислот по Кольбе.
Тетраэдрический механизм взаимодействия нуклеофилов с
карбоновыми кислотами и их произвоными. Реакция
карбоксилатов с литийорганическими соединениями.
Галогенангидриды. Получение с помощью галогенидов
фосфора, тионилхлорида. Свойства: взаимодействие с
нуклеофильными реагентами (вода, спирты, аммиак, амины,
гидразин, металлоорганические соединения). Ангидриды.
Методы получения: дегидратация кислот с помощью Р2О5 и
фталевого ангидрида; ацилирование солей карбоновых кислот
хлорангидридами. Смешанные ангидриды, факторы
определяющие хемоселективность. Реакции ангидридов
кислот с нуклеофилами. Реакция Перкина.
Восстановление кислот
CH3(CH2)7CH=CH(CH2)7COOH |
LiAlH4 |
CH3 |
(CH2)7CH=CH(CH2)7CH2OH |
|
ТГФ; 65 °С |
||||
|
|
(87 %) |
||
|
|
|
||
(CH3)3CCOOH |
LiAlH4 |
|
(CH3)3CCH2OH |
|
|
|
|||
эфир или ТГФ; 40 °С |
(92 %) |
|||
|
|
|
||
HOOC(CH2)8COOH |
LiAlH4 |
HOCH2(CH2)8CH2OH |
||
ТГФ; 65 °С |
||||
|
|
(97 %) |
||
|
|
|
||
|
1) B2H6; ТГФ; 20 °С |
O2N |
CH2CH2OH |
||
O2N |
CH2COOH |
2) H O; H+ |
|||
|
|
2 |
|
|
|
|
|
|
|
(95 %) |
|
CH3 |
1) B2H6 |
; ТГФ; 20 °С |
CH3(CH2)4CH2OH |
(100 %) |
|
(CH2)4COOH |
|
||||
|
2) H2O; H+ |
|
|
|
|
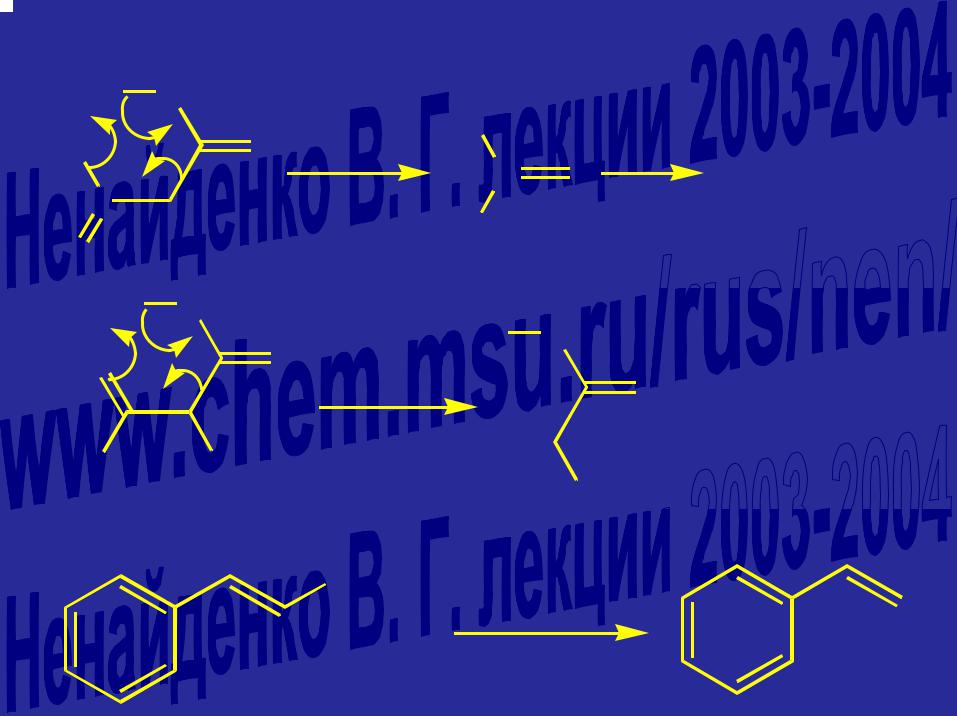
Декарбоксилирование кислот
H |
O |
|
HO |
|
-O |
|
O |
|
|
|
N |
CH3NO2 |
||
N+ |
|
|
||
O |
|
|
-O |
|
|
|
|
|
|
H |
O |
|
H |
O |
O |
|
O |
||
|
|
O |
||
|
|
|
|
HO R
R
COOH Cu
нагрев

Реакция Бородина-Хунсдиккера
RCOOAg + Br2 |
CCl4 |
|
RBr |
80 °C |
|
||
|
+ |
CO2 + AgBr |
|
|
|
CH3(CH2)10COOAg + Br2 |
CCl4 |
CH3(CH2)10Br |
|
80 °C |
|||
|
(67 %) |
||
|
|
CCl4
CH3OOC(CH2)4COOAg + Br2  CH3OOC(CH2)4Br
CH3OOC(CH2)4Br
80 °C
(68 %)

А.П. Бородин (1833-1887)

HgO; Br2
CH3(CH2)15CH2COOH  CH3(CH2)15CH2Br (93 %)
CH3(CH2)15CH2Br (93 %)
CCl4; 80 °C
+ H2O + CO2 + HgBr2
HgO; Br2
COOH 
 Br (46%)
Br (46%)
CCl4; 80 °C
+ H2O + CO2 + HgBr2
Реакция подходит для алифатических и ароматических кислот

O
RCOOAg + Br2  R C + AgBr
R C + AgBr
|
O |
|
O |
OBr |
|
|
|
|
|||
R |
C |
R |
C |
+ |
Br |
|
OBr |
|
O |
|
|
|
O |
|
|
|
|
R |
C |
R |
+ |
CO2 |
|
|
O |
|
|
|
|
|
O |
|
|
|
O |
R |
+ R C |
|
RBr |
+ |
R C и т.д. |
|
OBr |
|
|
|
O |

Реакция Кольбе
2 RCOO |
- 2e- |
RR + 2CO2 |
|||
CH3OH |
|||||
|
|
|
|
||
2 н-C H |
|
COO |
- 2e- |
н-C22H46 + 2CO2 |
|
23 |
|
||||
11 |
|
CH3OH - H2O |
(90 %) |
||
|
|
|
|||
- 2e-
CH3OOC(CH2)nCOO CH3OOC(CH2)2nCOOCH3 + 2CO2 CH3OH
(40-95 %)
- 2e-
CH3OOC(CH2)4COO CH3OOC(CH2)8COOCH3 + 2CO2 CH3OH
(75 %)
монометиловый эфир |
диметиловый эфир |
адипиновой кислоты |
себациновой кислоты |
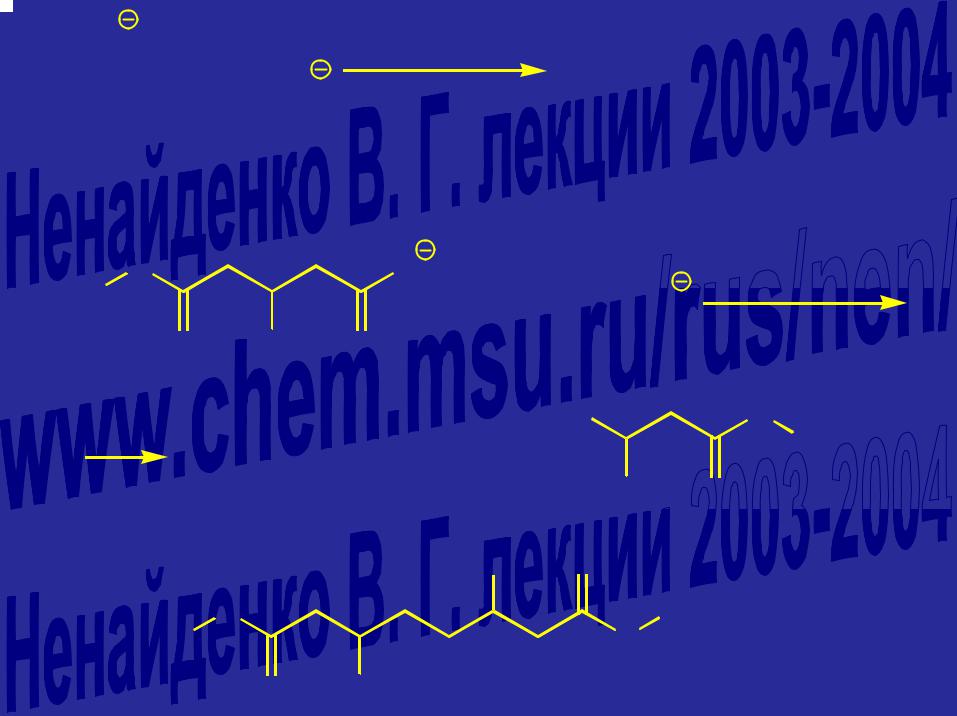
RCOO + |
электролиз |
RR + |
R(CH2)nCOOCH3 |
|
CH3OOC(CH2)nCOO |
CH3OH |
|||
|
|
+ CH3OOC(CH2)2nCOOCH3
O |
|
O |
|
электролиз |
H3C |
|
+ н-C7H15COO |
|
|
|
|
CH3OH |
||
O |
CH3 |
O |
|
|
|
|
CH3(CH2)7 |
|
O |
н-C14H30 |
+ |
O |
CH3 + |
|
|
(49 %) |
CH3 |
|
|
|
(48 %) |
|
||
|
|
|
||
|
|
CH3 O |
|
|
+ H3C |
O |
CH3 |
(3 %) |
|
|
O |
|
||
|
|
|
||
|
O |
CH3 |
|
|
