
Органическая химия - Лекции - МГУ - Ненайденко - 2004 / Лекция 12 - Нитросоединения. Фенолы. Синтез и свойства
.pdf
Лекция 12
Нитросоединения. Cвойства (продолжение)
Фенолы. Синтез и свойства

Фенолы. Методы получения: щелочное плавление аренсульфонатов, замещение галогена на гидроксил, гидролиз солей арендиазония, перегруппировка Байера-Виллигера, гидроксилирование аренов (радикальное и электрофильное), получение фенолов на основе металорганических соединений. Кумольный способ получения фенола в промышленности.
Свойства фенолов. Фенолы как ОН-кислоты. Сравнение кислотного характера фенолов и спиртов, влияние заместителей на кислотность фенолов. Образование простых и сложных эфиров фенолов. Ацилирование фенолов, перегруппировка Фриса.
Фенолы. Синтез и свойства
OH |
OH |
фенол |
|
о-крезол |
OH |
OH |
OH |
|
||
OH |
|
|
OH
OH
1,2-дигидроксибензол 1,3-дигидроксибензол 1,4-дигидроксибензол
пирокатехин |
резорцин |
гидрохинон |
|
OH |
OH |
|
OH |
OH |
OH |
|
|
OH |
|
HO |
OH |
|
|
|
|
1,2,3-тригидроксибензол |
OH |
1,3,5-тригидроксибензол |
|
|
(флороглюцин) |
||
|
|
||
(пирогаллол) |
1,2,4-тригидроксибензол |
|
|
|
|
||
Синтез фенолов
Щелочное плавление сульфокислот
|
ArSO |
Na + 2NaOH |
300-350OC ArONa + Na SO |
3 |
+ H O |
|
3 |
|
2 |
2 |
|
SO3 |
HO |
SO3 |
OH |
|
O |
|
|
|
|
||
|
OH |
|
+ SO2 OH |
|
+ SO23 + H2O |
|
|
|
3 |
|
|
|
SO3Na |
|
ONa |
|
|
|
|
O |
|
|
|
|
NaOH; 330 C |
+ Na2SO3 + H2O |
|
||
|
|
|
|
||
CH3 |
CH3 |
|
SO3Na |
ONa |
|
|
ONa |
||
O |
|
O |
|
|
NaOH; 325 C |
|
|
NaOH; 340 C |
|
|
|
|
|
|
SO3Na |
|
|
SO3Na |
ONa |
|
|
|
Нуклеофильное замещение
NO |
Cl + 2NaOH |
160OC |
NO2 |
|
ONa + NaCl + H2O |
|
|
||||
2 |
|
|
|
|
|
|
|
|
|
76% |
|
|
O2N |
|
|
|
O2N |
NO2 |
Br + 2NaOH |
0-20OC |
NO2 |
|
ONa + NaBr + H2O |
|
|
H2O |
|
|
|
|
O2N |
|
97% |
O2N |
|
|
|
|
|
||
|
Cl |
|
|
|
OH |
NC |
CN |
50OC |
NC |
|
CN |
|
+ H2O ТГФ |
|
|
+ HCl |
|
NC |
CN |
|
NC |
|
CN |
|
CN |
|
|
|
CN |

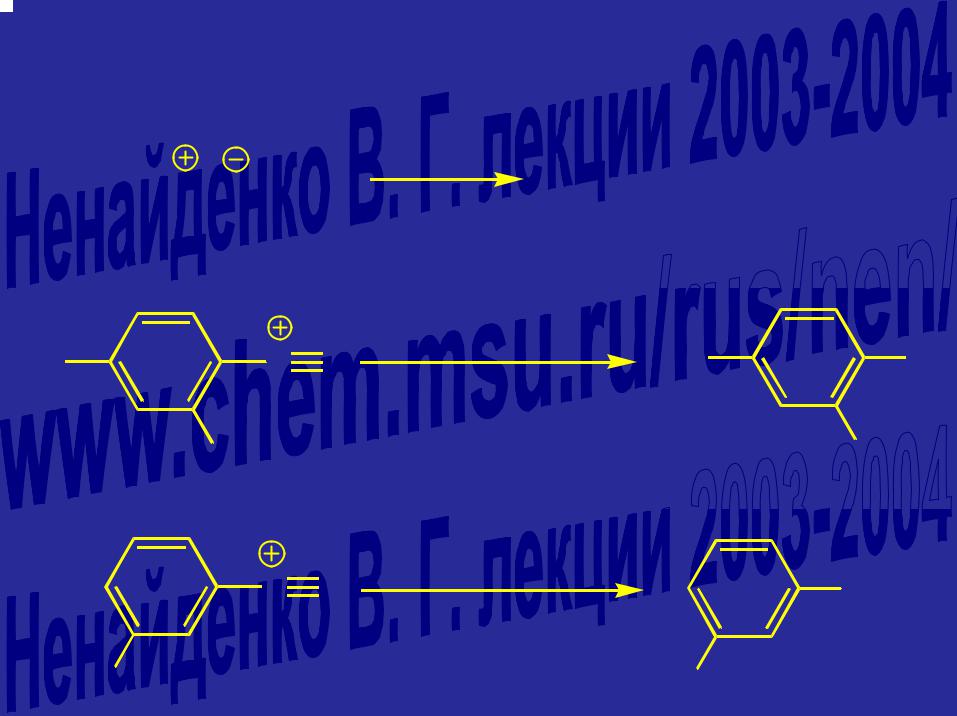
Замещение через арины
+ NaOH |
H2O |
|
|
350 - 400 °C |
|
OH |
|
|
|
||
Cl |
30 MПа |
+ |
2 : 3 |
|
|||
|
|
|
|
|
|
HO |
|
|
|
|
HO |
|
Cl |
+ NaOH |
H2O |
+ 2 : 1 |
|
350 - 400 °C |
||||
|
|
|
||
|
|
30 MПа |
|
HO
Использование солей меди подавляет изомеризацию
CH |
3 |
Cl + 2NaOH |
CuSO4;190-200OC |
CH3 |
ONa |
|
|||||
|
|
|
|
|
Cl |
|
ONa |
|
Cl + 4NaOH |
CuSO4;190OC |
ONa |
|
H2O |
|||
|
|
Cl |
Cl + 4NaOH |
CuSO4;175OC |
NaO |
ONa |
|
H2O |
|||||
|
|
|
|
Гидролиз солей диазония
ArN |
X |
+ H O |
t °C |
+ HX |
ArOH + N2 |
||||
2 |
|
2 |
H2O |
|
|
|
|
|
CH3 |
N N |
H2O |
CH3 |
OH |
|
H2SO4; 100 °C |
|||||
|
|
|
|
||
|
Br |
|
92 % |
Br |
H2O |
OH |
|
N N |
; 100 °C |
|
H2SO4 |
|
|
O2N |
O2N |
81-85 % |
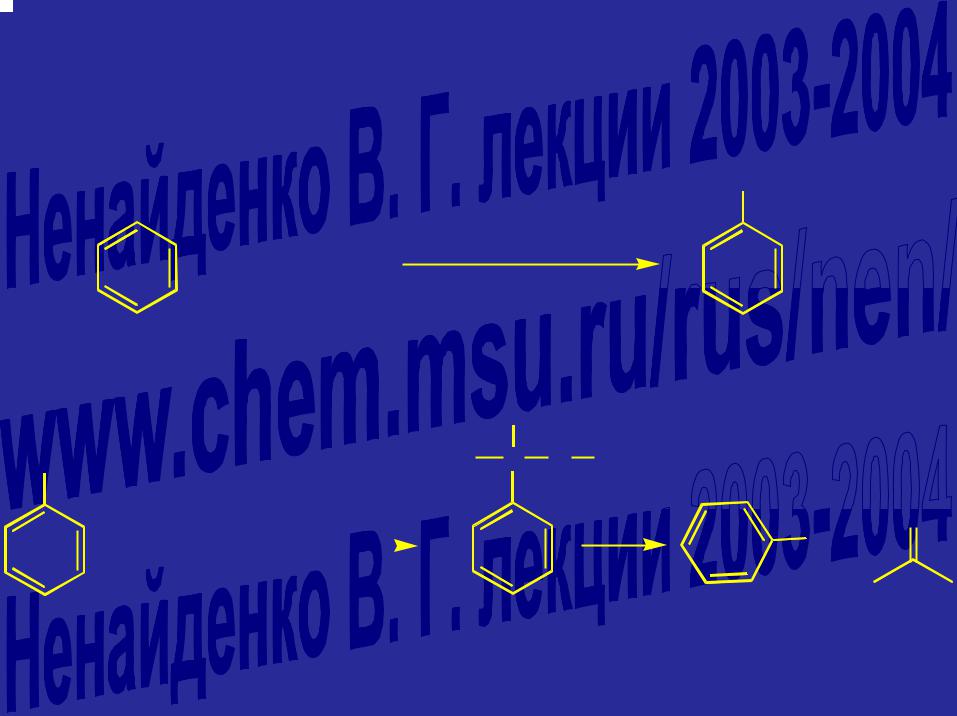
Промышленный способ получения фенола
CH(CH3)2
H3PO4; 250OC; 25 атм
+ CH3CH=CH2
|
CH3 |
|
|
CH(CH3)2 |
CH3 C O OH |
|
|
O |
H |
+ |
O |
100-130 C |
|
||
|
|
OH + |
|
+ O2 |
|
|
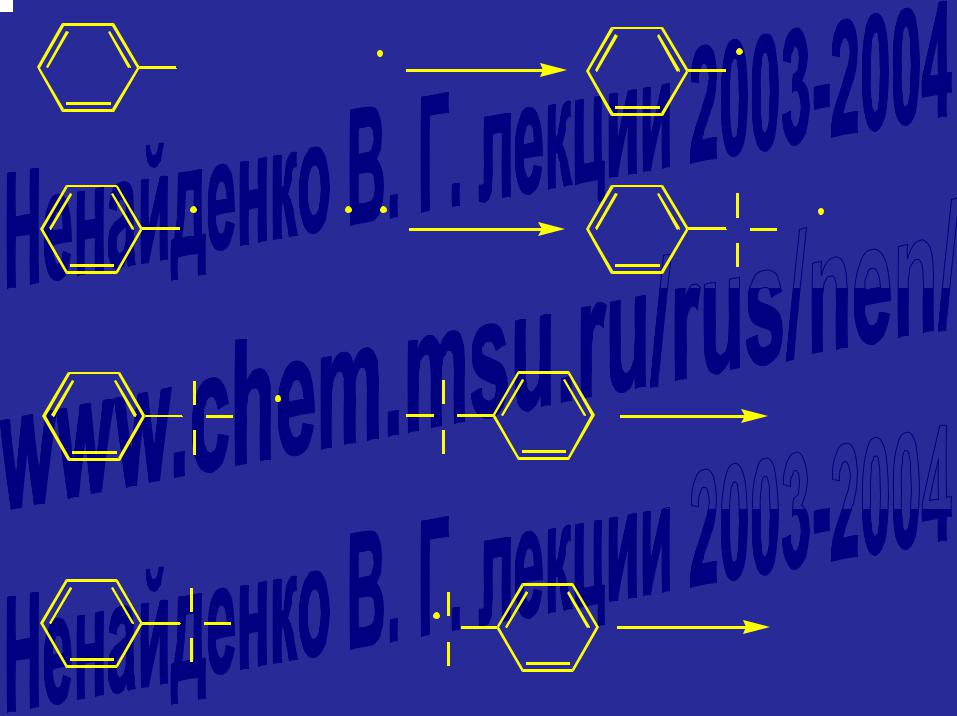
CH(CH3)2 + X |
C(CH3)2 + HX |
||
|
|
CH3 |
|
C(CH3)2 |
+ O-O |
C |
O-O |
|
|
CH3 |
|
CH3 |
|
CH3 |
|
C O-O |
+ H |
C |
|
CH3 |
|
CH3 |
|
CH3 |
|
CH |
|
|
|
3 |
|
C O-OH + |
C |
и т.д. |
|
CH3 |
|
CH |
|
|
|
3 |
|
