
- •0Лекция № 1.
- •1.Статическая биохимия (изучает структуру веществ ) - биоорганическая химия.
- •2.Значение биохимии для диагностики заболеваний.
- •1 .Альфа спираль ( л.Поллинг) - виток составляет от 3 до 6 ак. Терминатором спирали является ак-пролин.
- •2.Бетта складчатый слой.
- •3.Петли полипептидной цепи (соединительные петли).
- •1.Физико-химические свойства белков. Их использование для разделения белков.
- •2.Принципы классификации белков.
- •3.Характеристика простых белков.
- •1.Молекулярная масса белков определяет многие свойства белков: седиментация, диффузия, плотность белковых растворов, коллоидные свойства белков и др. Характеристики.
- •2.Способность белков связываться с лигандами,
- •3.Электрохимические свойства белков.
- •1. Концевыми соон и nh2 группами.
- •2.Боковыми группами:
- •1.Ионообменная хроматография.
- •2.Разделение белков на основании величины заряда - электрофорез белков. С помощью электрофореза в сыворотке крови выделяют как минимум 5 фракций: альбумины, альфа, альфа-2, гамма, бета - глобулины.
- •4.Коллоидные свойства белков.
- •5. Гидратация белков - способность белков связывать воду. Она осуществляется за счёт:
- •1. Повышают скорость реакции.
- •1.Витаминные.
- •4.Специфичность действия ферментов. В основе специфичности действия ферментов лежит конформационное соответствие его активного центра молекуле субстрата. Различают следующие виды специфичности:
- •1.Ингибиторы ферментативной активности.
- •1. Класификация ферментов.
- •1.Энзимопатология (патологическое состояние, связанное с полным отсутствием фермента в организме).
- •1.Поступление веществ из внешней среды посредством питания и дыхания.
- •1 .Катаболическая - распад ацетила.
- •1.Теория «активации» кислорода академика баха. Ведущей ролью в процессе биологического окисления он представлял образование пероксидов.
- •1 .Механизм окислительного фосфорилирования.
- •1. Целостность мембраны - непроницаемость её для протонов.
- •1.Связывание кислорода с активным центром фермента.
- •2.Восстановление кислорода и перенос его на субстрат.
- •1.Диоксигеназы - ферменты, включающие в субстрат молекулу кислорода.
- •2. Вторичные радикалы (он, липидные радикалы – l,, lo,, loo,) Их образование происходит с участием железа (11). Это патологические продукты.
- •3. Третичные радикалы (антиоксиданты) - образуются под влиянием вторичных радикалов.
- •1 .Фермент - супероксиддисмутаза (сод).
- •2.Она раздражает слизистую оболочку жкт, усиливая секрецию желёз.
- •3.Усиливает сокращение кишечника,
- •4.В толстом кишечнике под действием ферментов условно-патогенной микрофлоры клетчатка подвергается брожению с образованием глюкозы, лактозы и газообразных веществ.
- •1. Основной фосфоролитический путь
- •2.Неосновной амилолитический.
- •1.Болезнь ферса - фосфорилаза печени.
- •3 Реакции гликолиза являются необратимыми:
- •1.Гексокиназная.
- •2.Фосфофруктокиназная.
- •3.Пируваткиназная.
- •1. Глицеральдегид-3-фосфат
- •1. Транскетолазные реакции:
- •1.Липиды, их классификация и биологическая роль.
- •2.Превращение липидов в органах пищеварения.
- •1.Структурными липидами.
- •2.Резервными липидами.
- •3.Свободными липидами. — хиломикроны,
- •1 .Структурная. Липиды являются обязательным структурным компонентом биологических мембран клеток.
- •1. Эмульгируют пищевые жиры.
- •2. Активируют липолитические ферменты.
- •3. Выполняют роль переносчиков трудно растворимых в воде продуктов гидролиза жира и жирорастворимых витаминов a, d, е, к.
- •1.Транспортные липопротеины крови. Состав и биологическая роль. 2.Простагландины, простациклины, тромбоксаны, лейкотриены. Механизм их образования и биологическая роль.
- •3.Окисление глицерина и вжк в тканях.
- •1. Хиломикроны. Образуются в стенке кишечника и имеют самый крупный размер частиц.
- •2. Лпонп. Синтезируются в стенке кишечника и печени.
- •3. Лпнп. Образуются в эндотелии капилляров из лпонп.
- •4. Лпвп. Образуются в стенке кишечника и печени.
- •1.Простагландины:
- •1 . Альфа -глицерофосфата
- •1.Биосинтез вжк в тканях, химизм реакций, биологическая роль. 2.Холестерин, биологическая роль, биосинтез, окисление. 3.Патология липидного обмена.
- •1.Наличие атф, со2, н2о, надф*н2, поступающий из гексозомонофосфатного пути превращения глюкозы.
- •2.Наличие специальных белков-переносчиков (hs -апб). 3.Наличие специальных ферментов синтеза.
- •1.Структурная. Свободный холестерин является, обязательным структурным компонентом мембран клеток.
- •2.На этапе пищеварения.
- •1. Белковое питание.
- •2. Превращение белков в органах пищеварения.
- •3. Гниение белков. Образование токсических продуктов и механизм их обезвреживания.
- •1 .На этапе поступления жиров с пищей:
- •2.На этапе пищеварения.
- •1. Белковое питание.
- •1.Реакция декарбоксилированая.
- •1. Источники аминокислот в клетке и пути их использования.
- •3.Реакции дезаминирования - разрушение nн2-группы с выделением аммиака. В организме возможны следующие виды дезаминирования.
- •1. Образование амидов
- •2. Восстановительное аминирование.
- •3. Образование солей аммония.
- •4. Синтез мочевины - основной путь обезвреживания аммиака - орнитиновый цикл.
- •1.Особенности метаболизма нуклеопротеинов.
- •2.Бета -аминоизобутират.
- •1.Азот промежуточных продуктов (пептиды, ао, ак, креатин, индол, скатол и т.Д.)
- •2.Азот конечных продуктов (мочевина, мочевая к-та, индикан, креатинин)—
- •1.Продукционная - повышение образования компонентов остаточного азота, главным образом
- •2.Ретенционная - задержка азотистых шлаков из-за нарушения выделительной функции почек.
- •1. Нарушение на этапе поступления белков. В норме в организм должно поступать 80 - юОгр белков. Обязательно поступление всех незаменимых ак.
- •2. Нарушение на этапе пищеварения:
- •3. Нарушение межуточного обмена - нарушение обмена аминокислот в тканях.
- •1. Матрица - нити днк. Расщепление нити называется репликативная вилка. Она
- •2. Репарация днк.
- •3. Транскрипция гена.
- •1. Матрица - 1 нить днк. Образуется транскрипционный глазок.
- •1.Рекогниция (распознавание) - узнавание между аминокислотами и их транспортной
- •3. Инициация - начало процесса трансляции.
- •4. Элонгация (продолжение) протекает циклически в виде последовательной смены трёх фаз:
- •5. Терминация (прекращение).
- •6. Броцессинг белка (созревание) совокупность химических модификаций
- •1. Регуляция происходит только на уровне транскрипции. Первичные транскрипты генов у них транслируются до завершения транскрипции.
- •3. Регуляция биосинтеза белков у прокариот протекает альтернативно путём репрессии и индукции.
- •1. Выделение днк из биологического материала.
- •2. Амплификация - репликация на органическом участке молекулы днк. Производится за счёт работы ферментов и смены температурных режимов.
- •3. Детекция продуктов pcr (копий заданного участка) Схема pcr:
- •1. Изучаемая днк,
- •1. Структурные гены
- •2. Регуляторные элементы
- •1. Фенотипическое различие между клетками,
- •2. Индивидуальные различия между организмами одного вида. Каждый человек отличается от другого человека на 0,1% генома.
- •3. Широкое разнообразие белков. На основе 35000 генов синтезируются около 5000000 белков. В настоящее время нельзя сказать точно, что изучать важнее - геном или белковый состав организма.
- •1. Лежит в основе развития предрасположенности к заболеваниям (атеросклероз)
- •1.Внутриклеточное и межклеточное согласование клеточных процессов,
- •1.Малый период жизни (динамичность, оперативность регуляции).
- •1. Фактор расширения сосудов;
- •1. Передняя
- •1. Стимуляция синтеза белка: (через ифр I.)_
- •2. Влияние на углеводный обмен:
- •3. Влияние на минеральный обмен (через ифр1) - задержка кальция, фосфора, магния в организме,
- •4. Влияние на липидный обмен (не через ифр 1):
- •1. Альфа -меланоцитстимулирующий гормон (мсг) (промежуточная доля).
- •1. Гормоны щитовидной и паращитовидной желез.
- •1. Повышение поглощения тканями кислорода за исключением мозга, ретикуло-эпителиальной системы и гонад.
- •1. Углеводный обмен:
- •2. Липидный обмен:
- •1. Выделяют группу энзимовитаминов - это предшественники коэнзимов или простетических групп ферментов:
- •4. Участвуют в синтезе медиаторов (вит.С - серотонин), стероидных гормонов. Авитаминоз - это патологическое состояние, которое развивается в результате отсутствия
- •1. Он принимает участие в дифференцировке эпителиальных тканей, а также участвует в регуляции роста и дифференцировке эмбриональных тканей. В эмбриональных тканях
- •1. Нарушение дифференцировки эпителия - кератинизация.
- •2. Нарушение восприятия света и сумеречного зрения - гемеролапия («куриная слепота»). При хроническом гиповитаминозе вит.А развивается дистрофия и необратимая дегенерация палочек.
- •1 Витамин к и витамин е.
- •2 Водорастворимые витамины.
- •1. Является кофактором карбоксилирования глу в протромбине, т.Е. Необходим для его поевпашения в тромбин.
- •2. Участвует в превращении проконвертина в конвертин
- •1. Участие в окислительно-восстановительных реакциях:
- •2. Синтез кортикостероидов
- •1. Входит в состав тдф: тиамин(атф) ® тдф
- •2.Участвует в передаче нервного импульса.
- •1. Участвует в окислительно-восстановительных реакциях, т.К. Входит в состав фермента фмн
- •I. Метилирование в12
- •1. Является ко-ферментом карбоксилаз пвк, ацетил -коа, пропионил-коа.
- •2. Участвует в реакциях синтеза жирных кислот и стерина.
- •1. Входит в состав ко-фермента а, следовательно, участвует в синтезе ацетил-коа, различных ацил-коа, образующихся в результате следующих реакций:
- •2. Участвует в синтезе более 80 различных ферментов.
- •1. Участвует в образовании фосфотидилхолина.
- •1. Прямо воздействующие:
- •2. Структуры аналогичные витаминам:
- •1. Снижение затрат энергии в современных условиях, следовательно, необходимость снижение
- •1. Для крови: нб - 75%, кб - 25%. Суммарно этот показатель обозначается, как общий билирубин крови, который в норме для взрослого человека составляет 8 -20ммоль/л.
- •2. Печеночная желтуха (токсические и вирусные и другие гепатиты).
- •3. Подпеченочная желтуха (механическая).
- •4. Физиологическая желтуха новорождёных.
- •1. Транспортирует ионы меди, связывает и удерживает их в кровеносном русле
- •3. Обладает противовоспалительным действием
- •4. Является антиоксидантом, обезвреживает активные формы кислорода и пол.
- •IgD. Функция неизвестна.
- •1. Метаболиты: аминокислоты (25%), креатин (5%), полипептиды и нуклеотиды (3,5%)
- •2. Конечные азотистые продукты: мочевина(50%), мочевая кислота (4%), креатинин (2,5%), индикан и аммиак.
- •1.Экскреторная функция - это выделение мочевины, мочевой кислоты, креатина, лекарств, токсинов, избытка воды, микроэлементов, электролитов. Состоит из трёх фаз:
- •2.Регуляторная и гомеостатическая.
- •3.Секреторная функция:
- •1.Мочевина (20 - 35г/сутки). Повышается при повышенном распаде белков при нормальной функции печени, высокобелковое питание. Понижается при нарушении синтеза в печени, нарушении функции почек.
- •3. Креатинин (0,8 - 2,3г/сутки). Повышается при усиленном распаде компонентов мышечной ткани (травмы мышц), увеличение употребления мясной пищи. Понижается при угнетении фильтрации почками.
- •4. Белок (не более зОмг/л). Качественными реакциями не обнаруживается. Протеинурия наблюдается при гематурии, нарушении функции почек.
- •1. Химический состав нервной ткани.
- •1. Глу связывает аммиак
1.Ингибиторы ферментативной активности.
2.Виды ИНГИБИРОВАНИЯ.
3.Активаторы ферментов.
4.Понятие об ИЗОФЕРМЕНТАХ.
ИНГИБИТОРЫ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ.
Ферменты - это катализаторы с регулируемой активностью. Ею можно управлять с помощью различных веществ. Действие фермента можно подавить или частично, или полностью, т.е. ИНГИБИРОВАТЬ определёнными химическими веществами, находящимися в организме или поступающими извне. Эти вещества называются ИНГИБИТОРАМИ.
По характеру действия ингибиторы делятся на 2 большие группы:
1.Обратимые - это соединения, которые НЕКОВАЛЕНТНО взаимодействуют с ферментом, при этом образуется комплекс, способный к диссоциации.
2.Необратимые - это соединения, которые могут специфически связывать определенные функциональные группы активного центра фермента. Они образуют с ним прочные КОВАЛЕНТНЫЕ связи, поэтому такой комплекс трудно разрушить.
ВИДЫ ИНГИБИРОВАНИЯ. По механизму действия выделяют следующие виды ИНГИБИРОВАНИЯ:
1. КОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ - это торможение ферментативной реакции, вызванное связыванием с активным центром фермента ингибитора, который по своей структуре близок к структуре субстрата. При этом и субстрат, и ингибитор могут взаимодействовать с ферментом, но они будут конкурировать за активный центр фермента, и связываться будет то вещество, которого больше.
![]()
ПРИМЕР: СУКЦИНАТДЕГИДРОГЕНАЗНАЯ реакция.
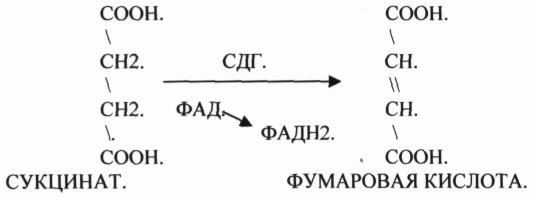
Конкурентным ингибитором данной реакции является МАЛОНОВАЯ кислота, поэтому с активным центром фермента связывается и та, и другая кислота, в зависимости от их соотношения в растворе. Чтобы снять частично или полностью действие конкурентного ингибитора, нужно повысить концентрацию субстрата. При этом весь фермент будет находиться в форме фермент-субстратного комплекса, а доля комплекса фермент-ингибитор будет резко понижаться, поэтому скорость ферментативной реакции может быть максимальной даже в присутствии ингибитора. Многие лекарственные препараты действуют по типу конкурентного ингибитора. При этом они тормозят активность ряда ферментов, необходимых для функционирования бактериальных клеток. Примером является применение СУЛЬФАНИЛА (СА). При различных инфекционных заболеваниях, которые вызываются бактериями, применяются СА препараты. Эти препараты имеют структурное сходство с ПАРААМИНОБЕНЗОЙНОЙ кислотой, которая используется бактериями для синтеза ФОЛИЕВОЙ кислоты, необходимой для роста и размножения бактерий.
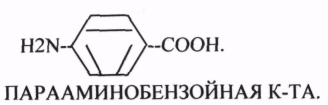

Введение СА приводит к ИНГИБИРОВАНИЮ фермента бактерий, которые синтезируют ФОЛИЕВУЮ кислоту. Нарушение синтеза этой кислоты проводит к нарушению роста микроорганизмов и их гибели.
По принципу конкурентных ингибиторов действует целая группа различных препаратов -это АНТИХОЛИНЭСТЕРАЗЫ. Они являются конкурентными ингибиторами фермента
ХОЛИНЭСТЕРАЗЫ, катализирующего ГИДРОЛИЗ АЦЕТИЛХОЛИНА. АЦЕТИЛХОЛИН обеспечивает проведение нервного импульса. АНТИХОЛИНЭСТЕРАЗЫ конкурируют с АЦЕТИЛХОЛИНОМ за активный центр фермента ХОЛИНЭСТЕРАЗЫ. В результате этого распад АЦЕТИЛХОЛИНА тормозится, он накапливается в организме, вызывая нарушение проведения нервного импульса.
2.НЕКОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ - это торможение ферментативной реакции, вызванное влиянием ингибитора на каталитическое превращение субстрата. При этом ингибитор не влияет на связывание фермента с субстратом. Неконкурентный ингибитор может связываться либо с каталитическими группами активного центра фермента, либо вне активного центра фермента, но при этом он изменяет КОНФОРМАЦИЮ фермента и затрагивает каталитический участок его активного центра. При неконкурентном ИНГИБИРОВАНИИ, возможно образование тройного комплекса.
![]()
В качестве неконкурентного ингибитора выступают ЦИАНИДЫ. Они прочно связываются с ионами железа, которые входят в состав каталитического ГЕМИНОВОГО фермента -ЦИТОХРОМОКСИДАЗЫ. Этот фермент является одним из компонентов дыхательной цепи. Блокирование дыхательной цепи выключает её из работы, что приводит к мгновенной гибели организме. Примером неконкурентного ингибитора являются соли тяжёлых металлов. Они блокируют -SH группы, которые входят в каталитический участок фермента. При этом образуется F-I комплекс. Он способен присоединять субстрат, но дальнейшего превращения субстрата не происходит, т.к. каталитические группы фермента заблокированы. Реакция непродуктивна. Снять действие неконкурентного ингибитора очень сложно, т.к. ионы металлов очень прочно связываются с активным центром фермента. Действие этого ингибитора можно снять только с помощью специальных веществ - РЕАКТИВАТОРОВ.
3.СУБСТРАТНОЕ ИНГИБИРОВАНИЕ - это торможение ферментативной реакции, вызванное избытком субстрата. При этом образуется F-S комплекс, но он не подвергается каталитическим превращениям, т.к. делает молекулу фермента неактивной. Действие субстратного ингибитора снимается путём уменьшения концентрации субстрата.
4.АЛЛОСТЕРИЧЕСКОЕ ИНГИБИРОВАНИЕ характерно для ферментов, имеющих четвертичную структуру, молекула которых состоит из нескольких единиц (ПРОТОМЕРОВ). АЛЛОСТЕРИЧЕСКИЕ ферменты могут иметь 2 и более единиц. При этом одна имеет каталитический центр и называется каталитической, а другая - АЛЛОСТЕРИЧЕСКИЙ центр и называется регуляторной. В отсутствии АЛЛОСТЕРИЧЕСКОГО ИНГИБИТОРА субстрат присоединяется к каталитическому центру, и идёт обычная каталитическая реакция. При появлении АЛЛОСТЕРИЧЕСКОГО ИНГИБИТОРА, он присоединяется к регуляторной единице, т.е. к АЛЛОСТЕРИЧЕСКОМУ центру, и изменяет КОНФОРМАЦИЮ центра фермента, в результате этого активность фермента снижается.
АКТИВАТОРЫ ФЕРМЕНТОВ.
Это вещества, повышающие скорость ферментативной реакции. Выделяют несколько групп активаторов:
1. Соляная кислота - активатор пепсина. Желчные кислоты - активаторы ЛИПАЗЫ.
2. Ионы различных металлов
Некоторые ферменты для проявления ферментативной активности требуют присутствия ионов нескольких металлов. Ионы металлов в разных случаях могут быть или донорами, или акцепторами электронов. Некоторые ионы металлов способны присоединять субстрат к активному центру фермента, т.е. способствуют образованию F-S комплекса.
3. Активация некоторых ферментов осуществляется путём частичного ПРОТЕОЛИЗА. Эти ферменты действуют в основном в ЖКТ. Они вырабатываются в неактивной форме, а именно, в форме ПРОФЕРМЕНТА. Активация таких ферментов происходит путём разрыва одной или нескольких ПЕПТИДНЫХ связей.
![]()
Из оставшейся части, после отнятия ГЕКСАПЕПТИДА, формируется новый фермент, отличающийся по ПРОСТРАНСТВЕННОЙ КОНФИГУРАЦИИ от неактивного ТРИПСИНОГЕНА, а также формой активного центра ТРИПСИНА.
4. АЛЛОСТЕРИЧЕСКАЯ АКТИВАЦИЯ ферментов характерна для АЛЛОСТЕРИЧЕСКИХ ферментов. Активатор присоединяется к АЛЛОСТЕРИЧЕСКОМУ центру и влияет на КОНФОРМАЦИЮ активного центра фермента, делает её КОМПЛЕМЕНТАРНОЙ молекуле субстрата.
ПОНЯТИЕ ОБ ИЗОФЕРМЕНТАХ.
ИЗОФЕРМЕНТЫ - это семейство или группа ферментов, катализирующих одну реакцию, но различающихся по некоторым физико-химическим свойствам:
по А К составу;
по последовательности АК;
по молекулярной массе;
по электрофоретической подвижности;
по способам регуляции.
ИЗОФЕРМЕНТЫ называют ещё молекулярными формами фермента, причём физико-химические различия в их формах возникли, вследствие генетического различия в первичной структуре белка. Множественные формы ферментов - это модификации одного фермента, у которого различия в физико-химических свойствах возникли не вследствие генетических причин, а вследствие каких-то внешних воздействий.
ЛДГ (ЛАКТАТДЕГИДРОГЕНАЗА) имеет 5 ИЗОФОРМ, каждая из которых является ТЕТРОМЕРОМ - состоит из 4 СУБЪЕДИНИЦ Н и М типов.
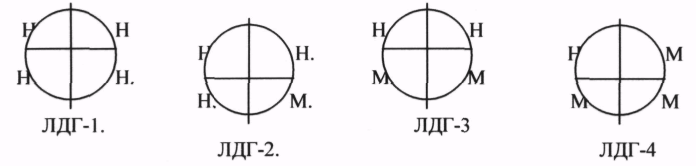
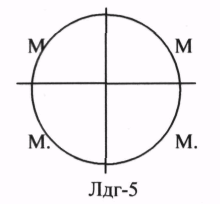
ИЗОФЕРМЕНТЫ отличаются строгой органной специфичностью. В миокарде, почках наиболее активна ЛДГ-1, ЛДГ-2. Для печени и мышц наиболее активны ЛДГ-4, ЛДГ-5. Определение активности ИЗОФЕРМЕНТОВ имеет диагностическое значение. При патологии печени в сыворотке крови резко возрастает активность ЛДГ-4, ЛДГ-5.
Лекция № 6.
ФЕРМЕНТЫ (продолжение).
