
Тесты в ЭМИРСе / ВСЕ ТЕСТЫ ПО ХИМИИ
.docxСтудент_Пр
тест "Электрохимия"
Вопрос: Система, состоящая двух электродов первого рода, соединенных во внешней и внутренней цепях, называется _________ 1. аккумулятором 2. двойным электрическим слоем 3. гальваническим элементом 4. электролизером Ответ: 3 Правильно!
Вопрос: Электродный потенциал цинка, опущенного в 0,01М раствор его соли, равен ______ В 1. −0,59 2. +0,819 3. −0,819 4. +0,30 Ответ: 3 Правильно!
Вопрос: При замене 0,1М раствора ZnSO4 на 0,01М в гальваническом элементе Zn/ZnSO4(0,1M)//NiSO4(0,1M)/Ni, величина ЭДС_________ 1. уменьшится 2. увеличится 3. не изменится 4. упадет до нуля Ответ: 2 Правильно!
Вопрос: В гальваническом элементе _____ медь является анодом: 1. Cu /CuSO4 //SnCl2/Sn 2. Cu /CuSO4 //Pb(NO3)2/Pb 3. Ni/NiSO4//CuSO4/Cu 4. Cu /CuSO4 //AgNO3/Ag Ответ: 4 Правильно!
Вопрос: Иодная вода (I2 ) может быть окислителем в процессе _______, если φ0: Br−/Br2 = 1,07 B; Cu2+/Cu+ = 0,15 B; MnO4−/MnO2 = 0,60 B; Fe3+/Fe2+ = 0,77 B; I2/2I− = 0,54 B; 2IO3−/I2 = 1,19 B 1. Cu+ → Cu2+ 2. Fe2+ → Fe3+ 3. I2 → 2IO3− 4. MnO2 → MnO4− Ответ: 4 Неправильно!
Вопрос: Анодным по отношению к покрываемому металлу является покрытие 1. кобальт покрыт оловом 2. серебро - никелем 3. цинк – медью 4. медь – золотом Ответ: 2 Правильно!
Вопрос: Уравнения процессов электрохимической коррозии железа в контакте с цинком в нейтральной среде в присутствии кислорода____ 1. Fe – 2ē → Fe2+ 2H2O + O2 + 4ē → 4ОH− 2. Zn – 2ē → Zn2+ 2H2O + 2ē → H2 + 2OH− 3. Zn2+ + 2ē → Zn Fe2+ + 2ē → Fe 4. Zn – 2ē → Zn2+ 2H2O + O2 + 4ē → 4ОH− Ответ: 4 Правильно!
Вопрос: Электролизом расплавов солей или оксидов получают _______ 1. Cu 2. Ni 3. Ag 4. Ca Ответ: 4 Правильно!
Вопрос: При электролизе водного раствора NaOH на инертном аноде протекает процесс _______ 1. 4ОH− − 4ē → О2↑ + 2H2O 2. 2H2O + 2ē → H2↑ + 2OH− 3. Na+ + ē → Na 4. 2H2O → O2↑ + 4H+ + 4ē Ответ: 1 Правильно!
Вопрос: Объем газа (н.у.), выделившегося на аноде при пропускании тока силой 6А через раствор нитрата серебра в течение 30 мин составила ____ л 1. 2,51 2. 1,25 3. 0,627 4. 0,25 Ответ: 3 Правильно!
тест "Классификация неорганических соединений для МП,ЭКТ, ЭТМО"
Вопрос: Укажите формулы амфотерных оксидов 1. ZnO 2. Na2O 3. Al2O3 4. CO2 5. N2O Ответ: 3,1 Правильно!
Вопрос: Укажите формулу безразличного оксида 1. NO2 2. Al2O3 3. Li2O 4. N2O 5. PbO Ответ: 4 Правильно!
Вопрос: Укажите оксид, реагирующий с K2O. 1. MgO 2. FeO 3. CO 4. N2O5 5. Bi2O3 Ответ: 4 Правильно!
Вопрос: Укажите формулу пирофосфорной кислоты. 1. HPO3 2. H3PO4 3. PH3 4. H4P2O7 5. HPO2 Ответ: 4 Правильно!
Вопрос: Укажите название солей ортоборной кислоты. 1. тетрабораты 2. метабораты 3. ортобораты 4. бориды Ответ: 3 Правильно!
Вопрос: Укажите схему суммарной диссоциации гидроксида хрома (III). 1. Cr(OH)3 ⇄ Cr3+ + 3OH- 2. H3CrO3 ⇄ H+ + H2CrO3- 3. Cr3+ + 3OH- ⇄ Cr(OH)3 ⇄ 3H+ + CrO33- 4. H3CrO3 ⇄ 2H+ + HCrO32- 5. Cr(OH)3 ⇄ CrOH2+ + 2OH- Ответ: 1 Неправильно!
Вопрос: Укажите вещество, при добавлении которого ослабляется диссоциация сернистой кислоты. 1. HNO3 2. KOH 3. Na2SO4 4. KNO3 5. K2S Ответ: 1 Правильно!
Вопрос: Укажите группу формул, соответствующих следующим солям: нитрат алюминия; сульфат цинка; хлорид кальция. 1. Al(NO2)3; ZnS; CaSO4 2. CaCl2; Al2S3; Al2(SO4)3 3. Al(NO3)3; ZnSO4; CaCl2 4. AlPO4; ZnSO3; CaOCl2 5. AlCl3; Zn(NO3)2; Ca3(PO4)2 Ответ: 3 Правильно!
Вопрос:
Укажите
формулу серной
кислоты
1. 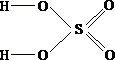 2.
2. 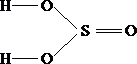 3.
3.  4.
4. 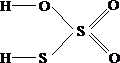 5.
5. 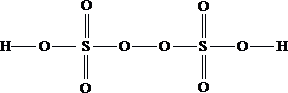 Ответ: 1
Правильно!
Ответ: 1
Правильно!
Вопрос: Укажите формулу средней (нормальной) соли 1. K2Cr2O7 2. KHCr2O7 3. KHS 4. CaOHCl 5. KAl(SO4)2 Ответ: 1 Правильно!
Вопрос: Укажите формулу кислой соли 1. NaHSO3 2. KAl(SO4)2 3. Cr(OH)2NO3 4. [Zn(NH3)4]SO4 5. Na2SO4 Ответ: 1 Правильно!
Вопрос: Укажите формулу основной соли 1. [Cu(NH3)4]SO4 2. CuSO4 3. K2[Cu(OH)4] 4. CuOHCl 5. Cu(HSO4)2 Ответ: 4 Правильно!
Вопрос:
Укажите
реакцию, в результате которой можно
получить основную
соль
1. ![]() 2.
2. ![]() 3.
3. ![]() 4.
4. ![]() 5.
H2SO4 + NaOH →
Ответ: 1
Неправильно!
5.
H2SO4 + NaOH →
Ответ: 1
Неправильно!
Вопрос:
Укажите
реакцию, в результате которой можно
получить кислую соль
1. ![]() 2.
2. ![]() 3.
H3PO4 + NaOH →
4.
3.
H3PO4 + NaOH →
4. ![]() 5.
5. ![]() Ответ: 4
Правильно!
Ответ: 4
Правильно!
Вопрос: Укажите формулу гидрофосфата железа (II) 1. (FeOH)3PO4 2. FeOHCl 3. Fe(H2PO4)2 4. FeHPO4 5. Fe2(HPO4)3 Ответ: 4 Правильно!
Вопрос: Для последовательного осуществления превращений по схеме NiO → NiSO4 → Ni(OH)2 → (NiOH)2 SO4 → NiCl2 необходимы вещества____ 1. SO2; Na2CO3; H2О; H2SO4 2. H2SO4; NaOH; H2SO4(нед.); НCl 3. H2S; NH4ОН; H2О; НCl 4. SO3; NiO; NaOH; H2О Ответ: 2 Правильно!
Вопрос: С помощью какого реагента можно отличить в растворах NaCl и NaNO3 1. HNO3 2. CaCl2 3. AgNO3 4. BaCl2 5. H2SO4 Ответ: 3 Правильно!
тест "Комплексные соединения "
Вопрос: Какая из реакций невозможна 1. KNO3 + NH4OH(изб.) 2. AgCl + KCN(изб.) 3. Cu(OH)2 + NH4OH(изб.) 4. Fe(OH)3 + KCN(изб.) Ответ: 4 Неправильно!
Вопрос: Величина и знак заряда комплексного иона [Cu+2(CN)3(CNS)] равны 1. 0 2. 1- 3. 3+ 4. 2- Ответ: 4 Правильно!
Вопрос: Соединение [Ni(NH3)6](OH)2 относится к классу 1. кислот 2. солей 3. оснований 4. аммиакатов Ответ: 3,4 Правильно!
Вопрос: Из соединений NiCl2 или [Ni(NH3)6]Cl2 более сильным электролитом является 1. оба слабые 2. оба сильные 3. NiCl2 4. [Ni(NH3)6]Cl2 Ответ: 3 Неправильно!
Вопрос: Самым неустойчивым комплексным ионом из представленных является 1. [Cd(NH3)4]2+, Kн ≈ 10-8 2. [CdCl4]2-, Kн ≈ 10-3 3. [Cd(CN)4]2-, Kн ≈ 10-17 4. [CdI4]2-, Kн ≈ 10-7 Ответ: 2 Правильно!
Вопрос: Комплексный ион [Co(NH3)6]3+ имеет __________ форму 1. линейную 2. тетраэдрическую 3. квадратную 4. октаэдрическую Ответ: 4 Правильно!
Вопрос: Концентрация NH3 в 1 моль/л растворе соли K[Ag(NH3)2], если Кн = 1•10-3, составляет_______ 1. 6,3•10-2 2. 1,26•10-1 3. 2,2•10-3 4. 5,85•10-2 Ответ: 4 Неправильно!
тест "Способы выражения концентрации растворов"
Вопрос: 120 г 5% раствора упарили до 80 г. Определить процентную концентрацию вновь полученного раствора. 1. 6,25% 2. 6% 3. 4,8% 4. 7,5% 5. 3,75% Ответ: 4 Правильно!
Вопрос: Какое количество нитрата натрия необходимо взять для приготовления 300 мл 0,2 н. раствора? 1. 15,3 г 2. 51 г 3. 10,2 г 4. 102 г 5. 5,1 г Ответ: 5 Правильно!
Вопрос: Сколько миллилитров воды нужно прибавить к 25 мл 40% раствора гидроксида калия, плотность которого 1,40 г/мл, чтобы получить 2% раствор? 1. 66,5 мл 2. 665 мл 3. 332,5 мл 4. 675 мл 5. 1330 мл Ответ: 4 Неправильно!
Вопрос: Вычислить нормальную концентрацию 20% раствора сульфата железа (III), плотность которого 1,2 г/мл. 1. 0,6 н 2. 3,6 н 3. 1,8 н 4. 1,2 н 5. 7,2 н Ответ: 2 Правильно!
Вопрос: На нейтрализацию 20 мл 5 н. раствора гидроксида натрия израсходовано 50 мл раствора серной кислоты. Вычислить молярность раствора серной кислоты. 1. 2М 2. 4М 3. 1М 4. 0,5М 5. 3М Ответ: 3 Правильно!
тест "Гидролиз"
Вопрос: Сульфат натрия при растворении в воде 1. гидролизуется по катиону 2. гидролизуется по аниону 3. гидролизуется по катиону и аниону 4. не гидролизуется Ответ: 4 Правильно!
Вопрос: Силикат калия при растворении в воде 1. гидролизуется по одной ступени 2. гидролизуется по первой ступени 3. гидролизуется необратимо 4. не гидролизуется Ответ: 3 Неправильно!
Вопрос: Сульфат хрома (III) при растворении в воде образует 1. основание и кислоту 2. кислую соль и основание 3. основные соли и кислоту 4. не гидролизуется Ответ: 1 Неправильно!
Вопрос: рН среды в растворе сульфата меди 1. =7 2. > 7 3. <7 4. ≥ 7 Ответ: 3 Правильно!
Вопрос: При гидролизе _________ образуется основная соль 1. Na2SO4 2. (NH4)3PO4 3. AlCl3 4. KCN Ответ: 3 Правильно!
Вопрос: На степень гидролиза соли _______ не влияет разбавление раствора 1. NH4CN 2. FeSO4 3. NH4Cl 4. K2Cr2O7 Ответ: 1 Правильно!
Вопрос: Константа гидролиза цианида аммония равна __, если KNH4OH = 1,8·10-5, KHCN = 5·10-10. 1. 3,3 2. 5,5 3. 7,7 4. 1,1 Ответ: 4 Правильно!
Вопрос: Уравнение SO32- + HOH ⇔ HSO3- + OH- относится к гидролизу соли_____ 1. NaHSO3 2. CdSO3 3. K2SO3 4. KHSO3 Ответ: 3 Правильно!
Вопрос: При гидролизе _____ образуется основная соль 1. Na2CO3 2. Na2SO4 3. FeCl3 4. CH3COONa Ответ: 3 Правильно!
Вопрос: Добавление _________ к раствору FeCl3 приводит к полному необратимому гидролизу 1. KCl 2. K2S 3. K2SO4 4. KCN Ответ: 2 Правильно!
тест "Строение атома, химическая связь"
Вопрос: Укажите количество энергетических состояний на f-подуровне четвертого уровня: 1. 3 2. 5 3. 6 4. 7 5. 14 Ответ: 5 Неправильно!
Вопрос: Укажите, по какому принципу рассчитывается количество электронов на уровнях: 1. по уравнению Шредингера 2. по уравнению Де-Бройля 3. по принципу Гейзенберга 4. по принципу Паули 5. по правилам Клечковского Ответ: 4 Правильно!
Вопрос: Укажите относительную энергию электронов на подуровнях 3p 4f 5d 6s: 1. 3,4,5,6 2. 2,4,3,1 3. 1,3,2,0 4. 4,7,7,6 5. 3,7,5,1 Ответ: 3 Неправильно!
Вопрос: Укажите электронную формулу, соответствующую атому в стационарном состоянии: 1. …3s23p43d2 2. …3s23p64s1 3. …2s12p1 4. …4s23d104p34d1 5. …4s13d104p2 Ответ: 2 Правильно!
Вопрос: Укажите положение ( № группы, подгруппу и № периода) в таблице Д.И.Менделеева элемента электронный паспорт которого заканчивается на ....4d7 1. V период VIIIB группа 2. IV период IVB группа 3. V период IVА группа 4. III период IVВ группа 5. V период IIIВ группа Ответ: 1 Правильно!
Вопрос: Насыщаемость ковалентной связи определяется 1. энергией связи 2. полярностью связи 3. формой электронных облаков 4. количеством неспаренных электронов в возбужденном состоянии атома Ответ: 4 Правильно!
Вопрос: σ- и π-связи образуются в молекуле 1. CI2 2. C2H6 3. F2 4. N2 Ответ: 1 Неправильно!
Вопрос: Расположите связи в порядке возрастания их энергии: а) As-O, б) S-O, в) Se-O, г) Ga-O, д) Zn-O 1. а, б, в, г, д 2. д, г, в, б, а 3. д, г, а, в, б 4. б, в, а, г, д Ответ: 4 Неправильно!
Вопрос: Дипольный момент молекулы ______ равен нулю 1. NH3 2. PCl3 3. SF6 4. HCl Ответ: 3 Правильно!
Вопрос: В молекуле __________угол между связями равен 109°28': 1. GeCl2 2. BeCl2 3. PCl3 4. SiH4 Ответ: 4 Правильно!
Вопрос: Угловую форму имеет молекула 1. HCl 2. F2 3. H2S 4. GeCl4 Ответ: 3 Правильно!
Вопрос: Наибольшей степенью ковалентности обладает связь ______ 1. Na-F 2. Na-S 3. Na-O 4. Na-Se Ответ: 1 Неправильно!
Вопрос: Атомную кристаллическую решетку образует 1. кремний 2. кадмий 3. йод 4. хлорид натрия NaCl Ответ: 1 Правильно!
тест "Строение атома, химическая связь"
Вопрос: Укажите количество энергетических состояний на f-подуровне четвертого уровня: 1. 3 2. 5 3. 6 4. 7 5. 14 Ответ: 4 Правильно!
Вопрос: Укажите емкость d- и p- подуровней четвертого энергетического уровня: 1. 2 и 6 2. 3 и 5 3. 10 и 6 4. 7 и 5 5. 10 и 14 Ответ: 3 Правильно!
Вопрос: Укажите сумму (n+l) для 2s-, 3d- и 4f- подуровней: 1. 2,3 и 4 2. 2,4 и 5 3. 4,6 и 8 4. 2,5 и 7 5. 0,4 и 6 Ответ: 4 Правильно!
Вопрос: Укажите электронную формулу, соответствующую атому в стационарном состоянии: 1. …2s12p3 2. …3s23p43d1 3. …3p64s13d104p1 4. …4s23d104p1 5. …5s14d105p1 Ответ: 4 Правильно!
Вопрос: Укажите положение ( № группы, подгруппу и № периода) в таблице Д.И.Менделеева элемента , у которого на 5р-подуровне есть 2 неспаренных электрона: 1. Ш период VА группа 2. IV период IVB группа 3. V период IVА группа 4. III период IVВ группа 5. V период IVB группа Ответ: 3 Правильно!
Вопрос: Межмолекулярной химической связью является 1. ионная 2. ковалентная 3. металлическая 4. водородная Ответ: 4 Правильно!
Вопрос: Только σ - связи образуются в молекуле 1. C2H2 2. C2H4 3. C2H6 4. CO2 Ответ: 1 Неправильно!
Вопрос: Расположите связи в порядке возрастания их длины: а) H-Br, б) H-I, в) H-F, г) H-Cl 1. а, б, в, г 2. б, а, в, г 3. в, г, а, б 4. г, в, а, б Ответ: 3 Правильно!
Вопрос: Дипольный момент молекулы ______ равен нулю 1. H2O 2. PCl5 3. AsCl3 4. PCl3 Ответ: 2 Правильно!
Вопрос: Наименьший угол между связями в молекуле 1. PCl3 2. SCl6 3. BeCl2 4. SiCl4 Ответ: 2 Правильно!
Вопрос: Линейную форму имеет молекула 1. PCl5 2. CН4 3. CO2 4. КF Ответ: 3 Правильно!
Вопрос: Наибольшей степенью ковалентности обладает связь ______ 1. Na-F 2. Na-S 3. Na-O 4. Na-Se Ответ: 4 Правильно!
Вопрос: Атомную кристаллическую решетку образует 1. алмаз 2. кобальт 3. СО2 4. хлорид меди CuCl2 Ответ: 1 Правильно!
тест "Химическая термодинамика и химическая кинетика"
Вопрос: Стандартная энтальпия образования вещества соответствует изменению энтальпии химической реакции образования ______ этого вещества при взаимодействии____ 1. любого количества ......... любых исходных веществ 2. 1моля ............ простых исходных веществ при любых условиях 3. 1моля ............ простых исходных веществ при стандартных условиях 4. любого количества ......... любых исходных веществ при любых условиях Ответ: 3 Правильно!
Вопрос: При образовании 22г СО2 выделилось 196,75 кДж тепла. Стандартная энтальпия образования СО2 равна______ кДж/моль. 1. +196,75 2. +393,5 3. +98,37 4. -393,5 Ответ: 1 Неправильно!
Вопрос: При реакции H2O(г) → H2O(ж) изменение энтропии соответствует 1. ΔS > 0 2. ΔS < 0 3. ΔS = 0 4. ΔS ≤ 0 Ответ: 2 Правильно!
Вопрос: Определить тепловой эффект реакции восстановления хрома алюминием (ΔH°х.р.) Cr2O3 + 2Al = 2Cr + Al2O3 1. -1440,6 кДж 2. +1440,6 кДж 3. -1676 кДж 4. -235,4 кДж Ответ: 1 Неправильно!
Вопрос: Правилу Бертло подчиняются реакции, протекающие при ______ температурах 1. высоких 2. любых 3. низких 4. строго определенных Ответ: 3 Правильно!
Вопрос: Для реакции 2С(т) + О2(г) = 2СО(г) ΔH<0. Самопроизвольно реакция протекает ______ 1. при низких температурах 2. при высоких температурах 3. при любых температурах 4. невозможна ни при каких условиях Ответ: 3 Правильно!
Вопрос: Вычислить изменение ΔG°298 в реакции 2Al2O3(кр) +3C(графит) = 4Al(кр) + 3СO2(г) 1. -1187,6 кДж 2. +1187,6 кДж 3. -1980,8 кДж 4. +1980,8 кДж Ответ: 4 Правильно!
Вопрос: При какой температуре константа равновесия системы равна 1, если ΔS°298, Si = 18,7Дж/моль• К? SiO2(к) + 2Н2(г) = Si(к) + 2H2O(г) Зависимостью ΔG от температуры пренебречь. 1. 5,73 K 2. 5727,9 K 3. 572,7 K 4. 4580 K Ответ: 3 Неправильно!
Вопрос: При каких концентрациях (моль/л) азота (CN) и водорода (CH) скорость реакции 3H2 + N2 => 2NH3 численно равна константе скорости? 1. CH = 2.5 CN = 2.5 2. CH = 0.1 CN = 100 3. CH = 10 CN = 1.0 4. CH = 0.5 CN = 2.5 5. CH = 2.0 CN = 0.125 Ответ: 5 Правильно!
Вопрос: Как изменится скорость реакции 2CO + O2 => 2CO2 при увеличении давления в системе в 4 раза? 1. увеличится, x18 2. увеличится, x216 3. уменьшится, x18 4. увеличится, x64 5. уменьшится, x216 Ответ: 4 Правильно!
Вопрос: Каким из способов можно сместить равновесие экзотермической реакции 2CO <=> CO2 + C(T) + Q в сторону образования угарного газа? 1. понижением температуры 2. снижением давления 3. уменьшением концентрации углекислого газа 4. повышением давления 5. введением катализатора Ответ: 4 Неправильно!
