
Свойства веществ и материалов / Korolchenko - Pozharo-vzryvoopasnost veshchestv i materialov chast-1 2004
.pdf
3.20.Максимальное давление взрыва
èскорость нарастания давления при взрыве
Для определения максимального давления взрыва зажигают газо-, пароили пылевоздушную смесь заданной концентрации в объеме реакционного сосуда и фиксируют развивающееся при воспламенении горючей смеси давление взрыва. Изменяя концентрацию горю- чего в смеси, выявляют максимальное давление взрыва. Для определения скорости нарастания давления при взрыве находят максимальную скорость изменения давления, возникающего в объеме реакционного сосуда при взрыве газо-, пароили пылевоздушных смесей заданного состава.
Определение максимального давления взрыва и скорости нарастания давления при взрыве газов и паров жидкостей выполняют на установке, схема которой показана на рис. 3.28.
Реакционный сосуд вместимостью 4 дм3 представляет собой две соединенные фланцами полусферы. Нижняя полусфера имеет термостатируемый электронагреватель для проведения испытаний при повышенной температуре с легкоконденсируемыми парами жидкостей. Реакционный сосуд должен быть рассчитан на давление, которое не менее чем в два раза превышает максимальное давление взрыва испытуемых смесей. Датчик давления имеет верхний предел измерения до 1000 кПа. Показания датчика давления фиксируются электроннолучевым осциллографом. Термопара типа ТХА поверхностная, обыкновенная, среднеинерционная, с электродами диаметром 0,5 мм. Потенциометр типа КСП-4 с градуировкой ХА имеет диапазон измерения температур от 0 до 400 °С. В качестве источника зажигания используют электроды с разрядным промежутком 5 мм или электриче- скую спираль. Разрядный промежуток электродов приходится на центр реакционного сосуда. От источника питания на зажигающее устройство подается напряжение: 3 кВ на электроды, 36 В на спираль. Выделяемая энергия искр на электродах при длительности разряда 1 – 2 с составляет 30 – 40 Дж; температура накаленной спирали 1100 °С. Смеситель для приготовления газо-, паровоздушной смеси снабжен встроенной мешалкой с электроприводом и штуцерами для подвода газов и крепления манометра. Смеситель че-
|
|
|
|
|
ÐÈÑ. 3.28. Установка для определения максимального давления взрыва и скорости нарастания давления при взрыве газов и паров жидкостей:
1 — термостатируемый электронагреватель; 2 — реакционный сосуд; 3 — осциллограф; 4 — датчик давления; 5 — потенциометр; 6 — термопара; 7 — источник зажигания; 8 — смеситель; 9, 10 — краны; 11 — ртутный манометр; 12 — источник питания; 13 — вакуумный насос
61
рез кран сообщается с реакционным сосудом. Ртутный манометр с ценой деления 0,1 кПа соединен через трехходовой кран с реакционным сосудом. Вакуумный насос обеспечивает остаточное давление не более 0,6 кПа.
Перед проведением испытаний установку проверяют на герметичность. Тарируют систему измерения давления подачей воздуха в реакционный сосуд до давления 1000 кПа с интервалом 50 кПа, а затем сбрасыванием давления до нуля через те же интервалы, фиксируя весь процесс осциллографом. По данным, снятым с осциллограммы, строят тарировочный график зависимости отклонения луча осциллографа от приращения давления, который должен представлять собой прямую линию.
Рассчитывают стехиометрическую концентрацию исследуемого вещества.
Для первого испытания количество исследуемого вещества принимают равным 70% от рассчитанной стехиометрической концентрации.
Для приготовления газо-, паровоздушной смеси требуемого состава смеситель вакуумируют до остаточного давления 0,5 кПа и затем поочередно подают в него компоненты смеси по парциальным давлениям. После впуска компонентов включают мешалку и перемешивают смесь в течение 6 мин. Реакционный сосуд вакуумируют до остаточного давления 0,5кПа, перепускают в него из смесителя заготовленную газо-, паровоздушную смесь, перекрывают краны и зажигают смесь искрой или спиралью. Результаты испытания регистрируют осциллографом. После взрыва сбрасывают избыточное давление в атмосферу, два – три раза вакуумируют реакционный сосуд для удаления газообразных продуктов горения. Определение максимального давления взрыва состоит из предварительных и основных испытаний. В серии предварительных испытаний находят зависимость давления взрыва от концентрации газа (пара) в смеси. Газо-, паровоздушную смесь, соответствующую максимуму этой зависимости, принимают за оптимальную.
В основных испытаниях проводят серию из десяти испытаний с оптимальной газо-, паровоздушной смесью и две серии из десяти испытаний со смесями, отличающимися от оптимальной на 1 – 2% в большую и меньшую стороны.
За величину максимального давления взрыва исследуемой газо-, паровоздушной смеси принимают наибольшее значение давления взрыва, полученное в трех сериях основных испытаний.
Среднюю скорость нарастания давления (dp /d )c рассчитывают по формуле:
(dp d )c = (pk – p0 ) k , |
(2.45) |
ãäå pk — давление, возникающее в реакционном сосуде при сгорании газо-, паровоздушной смеси, определяемое по осциллограмме “давление – время”, кПа; ð0 — первоначальное давление в реакционном сосуде, равное атмосферному, кПа; k — время, в течение которого достигается давление pk , ñ.
Максимальную скорость нарастания давления (dp d )màõ рассчитывают по формуле:
(dp d )màõ = p |
(2.46) |
ãäå ð — приращение давления, определяемое по прямолинейному участку осциллограммы “давление – время” по тарировочному графику, кПа (рис. 3.29); — время, в течение которого происходит приращение давления ð, ñ.
За величину средней или максимальной скорости нарастания давления при взрыве исследуемой газо-, паровоздушной смеси принимают их наибольшее значение, рассчитанное по результатам основных испытаний.
62

$ %! / 0 |
100 |
|
|
0 |
|
|
|
|
Определение максимального давления взрыва и |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
размером менее 50 мкм для металлических веществ и |
||||
|
500 |
|
|
|
|
|
|
|
|
скорости нарастания давления при взрыве пылей вы- |
|
|
|
|
|
|
|
|
|
|
полняют на установке, схема которой представлена на |
|
300 |
|
|
0 |
|
|
|
|
|
ðèñ. 3.11. |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
При испытании используют пыли с частицами |
|
|
|
|
|
|
|
|
|
|
менее 100 мкм для других веществ. Установку прове- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,1 |
0,2 |
|
0,3 |
|
ряют на герметичность. Тарируют систему измерения |
||||
|
|
|
|
|
|
|
|
давления подачей воздуха в реакционный сосуд до |
||
|
|
|
|
|
|
|
|
|
|
|
ÐÈÑ. 3.29. Осциллограмма изме- |
давления 800 кПа с интервалом 50 кПа, а затем сбрасы- |
|||||||||
нения давления при сгорании сме- |
ванием давления до нуля через те же интервалы, фик- |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
си внутри замкнутого сосуда |
сируя весь процесс осциллографом. По данным, сня- |
|
|
|
тым с осциллограммы, строят тарировочный график |
зависимости отклонения луча осциллографа от приращения давления, который должен представлять собой прямую линию.
Определяют давление “холостого” испытания установки ð0, возникающее в реакционном сосуде от подачи распыляющего газа при включенном источнике зажигания.
Время распыления 1 с, давление распыляющего газа в ресивере 300 кПа. Определение максимального давления взрыва состоит из предварительных и основных испытаний. В серии предварительных испытаний находят оптимальную массу исследуемого образца, при которой возникает наибольшее давление взрыва.
Последовательность проведения испытания: образец помещают в распылитель, подают в ресивер воздух до требуемого давления, устанавливают на пуско-регулирующем блоке продолжительность распыления, включают источник зажигания и распыляют образец. За взрыв принимают увеличение давления в реакционном сосуде не менее чем на 10 кПа по сравнению с давлением “холостого” испытания.
После каждого испытания реакционный сосуд продувают воздухом для удаления газообразных продуктов сгорания.
Первое испытание начинают с образца массой 0,5 г, увеличивая ее в последующих испытаниях на 0,2 г. По результатам испытаний строят кривую зависимости давления взрыва от массы образца. Массу образца, соответствующую максимуму этой зависимости, принимают за оптимальную.
Затем проводят серию основных испытаний на десяти образцах оптимальной массы и по полученным осциллограммам определяют давление взрыва.
За величину максимального давления взрыва пыли исследуемого вещества принимают наибольшее из десяти значений давления взрыва, полученных в серии основных испытаний.
Среднюю скорость нарастания давления (dp /d )c рассчитывают по формуле (3.50), где pk — давление, возникающее в реакционном сосуде при сгорании пылевоздушной смеси, определяемое по осциллограмме “давление – время”, кПа; ð0 — давление “холостого” испытания, кПа; k — время, в течение которого достигается давление pk , ñ.
Максимальную скорость нарастания давления (dp d )max рассчитывают по формуле (3.46). За величину средней или максимальной скорости нарастания давления при взрыве исследуемого вещества принимают их наибольшее значение, рассчитанное по результатам основных испытаний.
63
4. Расчет показателей пожаровзрывоопасности веществ и материалов
екомендуемые расчетные методы по точности зачастую не уступают эксперименталь- Ðным. В ряде случаев они являются единственной возможностью получения количественных характеристик пожаровзрывоопасности новых веществ.
Предлагаемые методы могут использоваться специалистами проектных организаций, научно-исследовательских институтов и высших учебных заведений при решении практи- ческих вопросов обеспечения пожарной безопасности объектов.
4.1. Расчет температуры вспышки
Температура вспышки индивидуальных веществ в закрытом тигле (з.т.)
Температура вспышки t âñï веществ, молекулы которых содержат структурные группы, представленные в табл. 4.1, рассчитывается по формуле, °C:
q |
|
t âñï 7314, 0,659t êèï a j l j , |
(4.1) |
j 2
ãäå t êèï — температура кипения жидкости при 101 кПа, .С; lj — число структурных групп j-го вида в молекуле; aj — эмпирические коэффициенты, значения которых приведены в табл. 4.1.
ТАБЛИЦА 4.1. Значения коэффициентов aj формулы (4.1)
Структурная группа |
a j , .C |
Структурная группа |
a j , .C |
|
|
|
|
|
|
C – C |
– 2,03 |
Ñ = Î |
11,66 |
|
|
|
|
|
|
Ñ Ñ |
– 0,28 |
Ñ 0 N |
12,13 |
|
C – H |
1,105 |
N – H |
5,83 |
|
|
|
|
|
|
C – O |
2,47 |
O – H |
23,90 |
|
|
|
|
|
|
C = C |
1,72 |
C – F |
3,33 |
|
|
|
|
|
|
C – N |
14,15 |
C – S |
2,09 |
|
|
|
|
|
|
C – Cl |
15,11 |
C = S |
– 11,91 |
|
C – Br |
19,40 |
H – S |
5,64 |
|
|
|
|
|
|
Si – H |
11,00 |
P – O |
3,27 |
|
|
|
|
|
|
Si – C |
– 4,84 |
|
|
|
|
|
P = O |
9,64 |
|
Si – Cl |
10,07 |
|||
|
|
|||
|
|
|
|
|
|
|
|
|
Средняя квадратическая погрешность расчета по формуле (4.1) составляет 10 .С.
64

Пример расчета tâñï по формуле (4.1)
Условие. Рассчитать tâñï толуола: С6Í5 – ÑÍ3; t êèï = 110,6 .Ñ.
Решение. В молекуле толуола имеется шесть связей вида С – С, одна связь С – С и во-
семь связей С – Н. По табл. 4.1 находим: |
|
àÑ – Ñ 0,28; |
aÑ – Ñ 2,03; àÑ – Í 1105,. |
Подставляя эти величины в формулу (1), получаем: |
|
t âñï 7314, 0,659 !110,6 6 !(0,28) 1!(2,03) 8 !(11, 05) 4,86 . C 1 5. C.. |
|
Экспериментальное значение t âñï |
толуола 7 .С. |
Для органических соединений, молекулы которых состоят их атомов С, Н, О и N, а |
|
также для галоидорганических и элементоорганических соединений, содержащих атомы S, Si, P и Cl, температура вспышки может быть рассчитана по формуле:
t âñï Ñ 0 Ñ1 t êèï Ñ 2 Í ñã , |
|
|
(4.2) |
|||
ãäå Ñ0 , Ñ1 è Ñ2 — константы, значения которых приведены в табл. 4.2; Í ñã |
— стандарт- |
|||||
ная теплота сгорания вещества, кДж моль. |
|
|
|
|
|
|
Средняя квадратическая погрешность расчета по формуле (4.2) составляет 10 .С. |
||||||
ТАБЛИЦА 4.2. Значения коэффициентов формулы (4.2) для различных классов соединений |
||||||
|
|
|
|
|
|
|
Класс соединений |
|
Ñ0 |
|
Ñ1 |
|
Ñ2 |
|
|
|
|
|
|
|
Соединения, состоящие из: |
|
|
|
|
|
|
атомов С, Н, О, N; |
|
– 45,5 |
|
0,83 |
|
– 0,0082 |
атомов С, Н, О, N, Cl |
|
– 39,6 |
|
0,86 |
|
– 0,0114 |
Соединения, содержащие атомы F, Br |
|
– 57,4 |
|
0,79 |
|
– 0,0147 |
Элементоорганические соединения, со- |
|
– 45,5 |
|
0,83 |
|
– 0,0082 |
держащие атомы S, Si, P, Cl |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пример расчета tâñï по формуле (4.2)
Условие. Рассчитать температуру вспышки диэиламина NH(C2H5)2, имеющего t êèï = 55,2 .Ñ è Í ñã = 2820 êÄæ ìîëü.
Решение. Используя данные табл. 4.2, получаем:
t âñï 45,5 0,83!55,2 0,0082 !2820 23,4.
Экспериментальное значение t âñï диэтиламина – 26 .С.
Если известна зависимость давления насыщенного пара от температуры, то темпера-
тура вспышки, .С, рассчитывается по формуле: |
|
|
|
|||
t âñï |
|
280 |
|
273 , |
(4.3) |
|
Ðâñï Ä 0 |
|
|||||
|
|
|
|
|||
ãäå Ðâñï — парциальное давление паров горючей жидкости при температуре вспышки, кПа; Ä0 — коэффициент диффузии пара в воздух, см2 с; — стехиометрический коэффициент кислорода в реакции горения.
Средняя квадратическая погрешность расчета по формуле (4.3) составляет 10 .С.
65

Наиболее точно величина t âñï рассчитывается по линейной зависимости температуры вспышки от температуры кипения, выполняющейся в пределах отдельных классов хими- ческих соединений:
tâñï = à + ât êèï . |
(4.4) |
Значения коэффициентов à è â для различных классов органических веществ приведены в табл. 4.3.
Средняя квадратическая погрешность при расчете по формуле (4.4) составляет 4 °С.
ТАБЛИЦА 4.3. Значения коэффициентов à è â формулы (4.4)
Класс веществ |
à |
â |
|
|
|
Алканы |
– 73,22 |
0,693 |
Спирты |
– 41,69 |
0,652 |
Алкиланилины |
– 21,94 |
0,533 |
Карбоновые кислоты |
– 43,57 |
0,708 |
Алкилфенолы |
– 38,42 |
0,623 |
Ароматические углеводороды |
– 67,83 |
0,665 |
Альдегиды |
– 74,76 |
0,813 |
Бромалканы |
– 49,56 |
0,665 |
Кетоны |
– 52,69 |
0,643 |
Хлоралканы |
– 55,70 |
0,631 |
|
|
|
|
|
|
Температура вспышки смесей горючих жидкостей в закрытом тигле
Температура вспышки смесей горючих жидкостей tâñï ñì , .С, рассчитывается по формуле:
k |
|
H |
èñï i |
|
H èñï i |
|
|
|
x i |
|
|
|
|||||
!exp |
|
|
|
|
|
1, |
(4.5) |
|
|
273) |
R(t âñï ñì 273) |
||||||
i 1 |
R(t âñï i |
|
|
|
|
|||
ãäå x i — мольная доля i-го компонента в жидкой фазе; Í èñï i — мольная теплота испарения i-го компонента, кДж моль; tâñï, i — температура вспышки i-го компонента, .С; R — универсальная газовая постоянная.
Величина Í èñï i R может быть рассчитана по интерполяционной формуле:
Í èñï i R= 2918,6 + 19,6 ( t êèï i 273),
ãäå têèï i — температура кипения i-го компонента.
Средняя квадратическая погрешность расчета по формуле (4.5) составляет 10 .С. Температура вспышки бинарных смесей жидкостей, принадлежащих к одному гомо-
логическому ряду, рассчитывается по формуле: |
|
|||
t |
âñï ñì |
t 2 |
[x (m 1)( x 2) m ], |
(4.6) |
|
âñï |
|
|
|
ãäå t 2âñï — температура вспышки легкокипящего компонента смеси, .С; — гомологиче- ская разность по температуре вспышки в рассматриваемом ряду, .С; õ — массовая доля
66

высококипящего компонента в жидкой фазе; m — разность между числом углеродных атомов компон ентов смеси; x 2 — коэффициент, учитывающий нелинейный характер зависимости tâñï îò õ : ïðè x 3 0,5 x 2 2 x 1; ïðè x % 0,5 x 2 0 .
Средняя квадратическая погрешность расчета, по формуле (4.6) составляет 2 .С.
4.2. Расчет температуры воспламенения
Если известна зависимость давления насыщенных паров от температуры, то для рас- чета температуры воспламенения tвоспл , .C, веществ, состоящих из атомов С, Н, О и N, используется формула:
t воспл |
|
453 |
|
. |
(4.7) |
|
Ðвоспл Ä 0 |
|
|||||
|
|
|
|
Средняя квадратическая погрешность расчета по формуле (4.7) составляет 6 .С. Температура воспламенения веществ, в молекулах которых содержатся структурные
группы, представленные в табл. 4.4, рассчитывается по формуле:
q |
|
t воспл 47,79 0,882t êèï a j l j . |
(4.8) |
j 2
Средняя квадратическая погрешность расчета по формуле (4.8) составляет 5 .С.
ТАБЛИЦА 4.4. Значения коэффициентов aj формуле (4.8)
Структурная группа |
a j |
Структурная группа |
a j |
|
|
|
|
|
|
|
|
|
|
|
C – C |
0,027 |
Ñ = Î |
– 0,826 |
|
C – H |
– 2,118 |
N – H |
– 0,261 |
|
C – O |
– 0,111 |
O – H |
8,216 |
|
C = C |
– 8,980 |
Ñ Ñ |
– 2,069 |
|
C – N |
– 5,876 |
|||
|
|
|||
|
|
|
|
4.3. Расчет температуры самовоспламенения
Наиболее общим методом расчета температуры самовоспламения tñâ органических соединений является расчет по формулам (4.9) и (4.10):
t ñâ |
300 116 |
|
5 lñð |
ïðè lñð 5; |
(4.9) |
|
|
|
|
|
|
|
|
t ñâ |
300 38 |
lñð 5 |
ïðè lñð & 5, |
(4.10) |
||
ãäå lñð — условная средняя длина молекулы соединения, равная среднему арифметическому всех возможных длин lj цепей молекулы:
|
|
1 |
|
nö |
|
|
lñð |
|
|
l j , |
(4.11) |
||
|
||||||
|
|
|
|
|
|
|
|
nö j 1 |
|
||||
ãäå nö — число цепей в молекуле соединения.
67

Под цепью молекулы понимается непрерывная цепь атомов, соединяющая две концевые группы:
nö = 0,5m (m – 1), |
(4.12) |
ãäå m — число концевых групп в молекуле.
Концевыми группами принято считать группы –СH3, =ÑH2, а также все функциональные группы и циклы. В случае, если функциональная группа или цикл расположены в середине цепи, то их рекомендуется считать одновременно и концевой, и промежуточной группой.
Длина цепи молекулы lj вычисляется по формуле:
lj = mÑj + 4lý , |
(4.13) |
ãäå mCj — число атомов углерода в j-îé öåïè; lý — эквивалентная длина функциональной группы или цикла, входящих в j-óþ öåïü.
Эквивалентная длина lý функциональной группы является аддитивной величиной, не зависящей от класса соединения. Величина lý вычисляется по формуле:
lý (a bmC ) r , |
(4.14) |
ãäå mÑ — общее число атомов углерода в молекуле. Если функциональная группа, для которой вычисляется lý , присоединена к ароматическому циклу с боковой углеродной цепью или отделена от ароматического цикла не менее чем одним атомом углерода, то при под- счете mÑ вместо реального числа атомов углерода в этом ароматическом цикле следует использовать его эквивалентную длину, вычисленную по формуле (4.15); r — общее число функциональных групп, циклов и локализованных кратных связей “углерод – углерод” в молекуле; a, b — коэффициенты, принимаемые по табл. 4.5.
ТАБЛИЦА 4.5. Значения коэффициентов a è b в формуле (4.14)
Функциональная группа |
a |
b |
Примечание |
|
|
|
|
|
|
|
|
|
Только для алифатических эфиров, в которых атом |
|
– O – |
16,5 |
–1,0 |
кислорода с обеих сторон присоединен к первичным |
|
|
|
|
или вторичным атомам углерода |
|
|
|
|
Для эфиров, в которых атом кислорода с одной сторо- |
|
– O – |
10,0 |
–0,5 |
ны присоединен к первичному или вторичному атому |
|
|
|
|
углерода алифатической группы |
|
– O – |
3,5 |
0 |
В прочих соединениях |
|
– OH |
3,0 |
–0,5 |
|
|
– O – |
1,0 |
0 |
Полагать r = 1 |
|
|
||||
|
|
|
|
|
– CO – |
1,2 |
–0,4 |
|
|
– COO – |
1,0 |
0 |
Полагать r = 1 |
|
– NH2 |
3,0 |
–0,2 |
|
|
– NH – |
2,5 |
0 |
|
|
N |
2,5 |
0 |
Полагать r = 1 |
|
|
|
|
|
|
P |
6,2 |
–0,23 |
Полагать r = 1 |
|
|
|
|
|
|
POH |
–4,8 |
6,9 |
Только для веществ с mC 6 |
|
|
|
|
|
|
|
|
|
Полагать r = 1 |
|
PO |
3,8 |
–0,38 |
||
|
||||
|
|
|
|
68

Тройная связь С 0 С увеличивает длину цепи, в которой она расположена, на 6/mC атомов углерода. Двойная связь С = С длину цепи не изменяет.
Эквивалентная длина неароматического моноядерного углеродного цикла равна числу атомов углерода в цикле, уменьшенному на 0,5.
Эквивалентная длина ароматического цикла lýà определяется по формуле:
lýà = nÿ – 0,5 + 4lýô , |
(4.15) |
ãäå nÿ — число ядер в цикле; 4lýô — алгебраическая сумма эквивалентных длин функциональных групп, входящих в состав цикла. К ароматическим в данном случае отнесены все циклы, имеющие симметрию правильного многоугольника и удовлетворяющие равенству= 4n + 2, где — число -электронов в цикле; n = 1, 2, 3… .
Эквивалентная длина неароматического моноядерного цикла равна алгебраической сумме общего числа атомов углерода и эквивалентных длин функциональных групп, составляющих цикл. Группы, только присоединенные к циклу, рассматриваются как самостоятельные и при подсчете эквивалентной длины цикла не учитываются.
Эквивалентная длина неароматического конденсированного цикла равна алгебраиче- ской сумме углеродных атомов в ядре цикла (при этом учитываются только те атомы, которые не входят в другие ядра и функциональные группы), эквивалентных длин моноядерных неароматических циклов, ароматических циклов и функциональных групп, входящих в состав данного ядра.
Длина цепи молекулы lj увеличивается на две единицы, если в ее состав входят две группы или цепи, присоединенные к ароматическому циклу в орто-положении друг к другу.
Если среднюю длину молекулы можно подсчитать различными способами из указанных выше, то предпочтительнее выбирать среднее значение из всех величин подсчитанных длин.
Средняя квадратическая погрешность расчета по формулам (4.9) и (4.10) для органи- ческих соединений, состоящих из атомов C, H, O и N, составляет 70 °С для значений температуры самовоспламенения в интервале 300 – 400 °С и 40 °С в остальных случаях.
Пример. Рассчитать температуру самовоспламенения изопропилбензола по формулам (4.9), (4.10).
Структурная формула изопропилбензола имеет вид:
Число концевых групп в молекуле равно трем (две группы CH3 и фенильное ядро). Общее число углеродных цепей в молекуле равно трем (это цепи следующих атомов: 1-2-3; 1-2-фенил; 3-2-фенил). Длину углеродных цепей, в которые входит фенил, уменьша-
ем на единицу. Имеем: nC |
3;m1 |
= 1; nC |
1;m2 = 2. Вычисляем среднюю длину углерод- |
||||
1 |
|
|
|
|
|
2 |
|
ной цепи молекулы изопропилбензола по формуле (11): |
|||||||
|
|
l |
|
|
2 (1!3 2 !1) |
1,7. |
|
|
|
ñð |
|
||||
|
|
|
|
|
3(3 1) |
||
|
|
|
|
|
|
||
Поскольку lñð < 5, то по формуле (9) вычисляем:
t ñâ 300 116
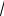 5 1,7 432°C.
5 1,7 432°C.
69

Экспериментальное значение температуры самовоспламенения изопропилбензола составляет 424 °С. Относительная погрешность расчета — 1,85%.
Расчет температуры самовоспламенения органических соединений может быть произведен с использованием метода групповых инкрементов:
|
|
|
|
|
n |
|
|
t ñâ |
300 100 |
|
8 |
a j l j |
(ïðè < 8); |
(4.16) |
|
|
|
|
|
|
j 2 |
|
|
|
|
|
|
|
n |
|
|
t ñâ |
300 10 |
8 |
a j l j |
(ïðè > 8), |
(4.17) |
||
j 2
ãäå aj — коэффициент, характеризующий вклад j-ой структурной группы в величину температуры самовоспламенения, °С; lj — число структурных групп в молекуле вещества.
Значения коэффициента aj для формул (4.16) и (4.17) приведены в табл. 4.6.
ТАБЛИЦА 4.6. Величины коэффициента aj для различных структурных групп
Структурная группа |
aj |
Структурная группа |
aj |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
190 |
| |
60 |
|
|
С (третичный) |
||||
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
180 |
– С– (четвертичный) |
100 |
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
160 |
– О – (простой эфир) |
–20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
140 |
|
–20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
120 |
Ñ = O |
60 |
|
|
|
|
|
|
|
|
|
|
|
100 |
– NH4 |
60 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
| |
|
|
–7 |
– NH2 |
40 |
– CH2 (вторичный) |
||||||
|
| |
|
|
|
NH |
|
– СH (вторичный) |
20 |
30 |
||||
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
– С– (вторичный) |
30 |
N |
20 |
|||
|
| |
|
|
|
| |
|
– СH – (третичный) |
40 |
|
|
|||
Примечания: 1. Вклад фенильного радикала aj учитывается только один раз независимо от числа фенильных радикалов в молекуле.
2.Для алканов, содержащих более восьми групп – СН2 –, вклад этой группы учитывается только восемь раз.
3.При 7,5 вклад четвертичной группы учитывается только один раз.
Проверка формул (4.16) и (4.17) на двухстах веществах показала, что максимальное расхождение между расчетными и экспериментальными величинами температуры самовоспламенения не превышает 40 град.
70
