
Лекция_АХ1
.pdfЛЕКЦИЯ 1
УЧЕНИЕ ОБ АНАЛИТИЧЕСКОМ СИГНАЛЕ
1.Виды анализа. Методы аналитической химии. Инструментальные методы анализа.
2.Учение об аналитическом сигнале. Био- и хемосенсоры.
3.Свойства аналитического сигнала.
4.Способы определения концентрации веществ. Метод градуировочного графика. Метод добавок.
1. Виды анализа. Методы аналитической химии. Инструментальные методы анализа
Аналитическая химия – наука о способах идентификации химических соединений, о принципах и методах определения химического состава веществ и их химической структуры. Она разрабатывает теоретические основы методов анализа, определяет границы их применимости, метрологические и другие характеристики, предлагает способы анализа различных объектов.
Методы аналитической химии используют в различных отраслях науки и техники, в том числе молекулярной биологии, биохимии, исследованиях и анализе пищевых продуктов, фармацевтических препаратов, материалов особой степени чистоты, объектов окружающей среды.
Аналитическая химия – это не только анализ, это широкая область знаний, наука об определении химического состава вещества, независимо от того, какими методами или способами выполнено это определение.
Виды анализа
I. Качественный анализ. Устанавливает, какие вещества (или элементарные объекты, составные части) включает анализируемый образец.
Элементарные объекты (или элементарные составляющие химических компонентов) – атомы, молекулы, функциональные группы атомов, ионы.
Качественный анализ отвечает на вопрос да/нет или свидетельствует о положительном или отрицательном результате анализа. Т.е. качественный анализ устанавливает, присутствует или не присутствует в анализируемом образце определённое вещество (это вещество называется аналитом). Пример – домашний тест на беременность, который позволяет установить, присутствует или нет в моче половой гормон – гонадотропин.
По технике выполнения качественный анализ делят на дробный и систематический. Дробный анализ – удаётся создать условия для селективного обнаружения только одного элементарного объекта на фоне всех остальных. Например, соответствующие ионы могут быть обнаружены непосредственно в отдельных порциях исследуемого раствора при использовании специфических реакций, не считаясь с тем, какие другие ионы
содержатся в этом растворе. При этом не имеет значения порядок обнаружения отдельных ионов.
Когда достаточно специфические реакции отсутствуют и нельзя повысить их специфичность каким-либо способом, прибегают к систематическому анализу, для чего разрабатывается определенная последовательность реакций обнаружения. К обнаружению каждого иона приступают лишь после того, как все другие ионы, мешающие его обнаружению (т.е. также реагирующие с применяемым реагентом), будут предварительно обнаружены и удалены из раствора.
II. Количественный анализ. Позволяет установить количественное содержание всех или отдельных компонентов, т.е. отвечает на вопрос «сколько?».
При определении микропримесей грань между этими видами анализа подчас стирается.
Известен другой способ классификации видов анализа:
1.Валовый (общий состав) – локальный.
2.Деструктивный – недеструктивный.
3.Контактный – дистанционный
4.Дискретный – непрерывный.
Классификация видов анализа может быть также основана на природе обнаруживаемых или определяемых частиц. По этому признаку выделяют виды анализа:
1.Элементный (атомно-ионный).
2.Структурно-групповой (функциональный).
3.Молекулярный – обнаружение и определение химических соединений (например, анализ основных компонентов и примесей в воздухе O3, N2, O2,
CO2).
4.Изотопный анализ. Профессиональные аналитики этим видом анализа занимаются мало. Такой анализ чаще проводят физики, геологи. Например, определение дейтерированной воды в обычной воде. Изотопный анализ необходим при исследовании искусственных элементов.
5.Вещественный анализ устанавливает, в какой форме присутствует интересующий нас компонент в анализируемом объекте и каково содержание
этих форм. Например, ртуть может присутствовать в воде в виде таких форм
–Hg0, Hg2+ CH3Hg+, (CH3)2Hg.
6.Фазовый анализ – анализ включений в неоднородном объекте, например, минералах. Так, CuS и CuO не распределены в минерале гомогенно, а образуют отдельные фазы.
Методы аналитической химии:
Все существующие методы аналитической химии можно разделить на:
1.Методы пробоотбора.
2.Методы разложения проб.
3.Методы разделения компонентов.
4.Методы обнаружения (идентификации).
5.Методы определения.
Есть гибридные методы, в которых сочетаются метод разделения и измерения.
Наибольшее значение имеют методы определения. Все эти методы основаны на одном принципе – зависимости между составом вещества и его свойствами.
В соответствии с другой классификацией методы определения делят:
I. Химические методы – основаны на химических, в том числе электрохимических реакциях. Анализируемую пробу подвергают химическому взаимодействию с аналитическим реагентом.
II. Физико-химические методы.
III. Физические методы. Основаны на физических явлениях и процессах (взаимодействие вещества с потоком энергии).
IV. Биологические методы – основаны на явлении жизни.
Эта классификация достаточно условна. Так, фотометрические методы могут быть и физико-химическими и чисто физическими. В ядернофизических методах иногда важную роль играют химические операции (радиохимические методы).
Вторая и третья группы методов объединяются под общим названием
инструментальные методы анализа.
2. Учение об аналитическом сигнале. Био- и хемосенсоры
Любой из методов анализа использует определенный сигнал, который в данных условиях дают конкретные элементарные объекты.
Аналитический сигнал – это любое проявление химических или физических свойств вещества, которое можно использовать для установления качественного состава анализируемого объекта или для количественной оценки содержащихся в нем компонентов.
Это фундаментальная характеристика вещества, такая, как заряд ядра атома, атомная масса и др. Аналитический сигнал – носитель как качественной, так и количественной информации.
Классификация аналитических сигналов: 1. Физические сигналы
Например, испускание или поглощение светового излучения веществами при высоких температурах. В результате этого наблюдается спектр. Положение линии в спектре, которое можно охарактеризовать длиной волны
λ или частотой ν, указывает на присутствие того или иного элемента. Например, попадание поваренной соли на газовую горелку на кухне ведет к окрашиванию пламени в желтый цвет. Длина волны света является качественной информацией и свидетельствует о наличии в поваренной соли
натрия. В то же время интенсивность линии излучения (I) дает информацию о количестве. К физическим аналитическим сигналам относятся плавление вещества (характеристика – tпл), кипение (tкип), вращение плоскости поляризации света (показатель преломления) и др.
2. Химические сигналы
Например, выпадение осадка – это качественный аналитический сигнал, а его масса – это количественный сигнал. К химическим сигналам относятся также изменение цвета, выделение газа, изменение температуры раствора и др.
Приведем примеры химических аналитических сигналов: |
|
Pb2+ + 2I– PbI2↓ выпадает желтый осадок; |
|
Co2+ + 4SCN– [Co(SCN)4]2– |
появление голубого окрашивания |
раствора в присутствии этанола свидетельствует о том, что для проявления отдельных сигналов необходимо создавать особые условия;
Fe3+ + 4SCN− [Fe(SCN)4]– кроваво-красное окрашивание раствора. Иногда аналитический сигнал не проявляется или исчезает в
присутствии некоторых веществ. Например, если добавить в кровавокрасный раствор роданидного комплекса железа фторид-ионы, произойдет
обесцвечивание:
[Fe(SCN)4]− + 6F− FeF63− + 4 SCN−.
Не появится также красное окрашивание раствора, если перед добавлением роданида аммония в раствор соли железа(III) ввести фосфатионы. Это явление подавления аналитического сигнала называется
маскированием.
Сигнал, который отличается от других высокой селективностью, получен при определении никеля(П) с помощью органического реактива, предложенного в 1905 г. Л.А. Чугаевым. Химический реактив называется диметилглиоксим (обозначается H2Dm) или реактив Чугаева:
+ 2H2Dm + 2NH3 Ni(HDm)2↓ + 2NH4+ образуется осадок диметилглиоксимата никеля(П) розового цвета.
3. Биологические сигналы
Эти аналитические сигналы часто используют для общего токсикологического контроля объектов окружающей среды, т.е. для биотестирования. К биологическим сигналам относятся:
–скорость потребления кислорода микроорганизмами;
–изменение фотосинтетической активности и флуоресценции водорослей;
–изменение двигательной активности, частоты дыхания и сердцебиения дафний;
–смена статического состояния медицинской пиявки на динамическое и
др.
Биологические аналитические сигналы часто используют в мониторинге. Мониторинг – специальная информационно-аналитическая система наблюдения, контроля и оценки состояния природной среды. На основе биологических сигналов устроены биосигнализаторы токсичности СБ-1,

СБР-1. Устройство состоит из рабочих аквариумов с рыбами и электродами, фотодатчиков, фиксирующих переход рыб из одной зоны в другую. Если контролируемая вода не токсична, рыбы не уходят из зоны поступления воды. Если в воде содержатся токсиканты, то рыбы переходят в безопасную зону аквариума, куда дополнительно подается чистая вода. Сигнал о токсичности подается в случае ухода не менее 3х рыб из пяти за данный промежуток времени (5-25 минут). Чтобы рыбы не адаптировались к низким концентрациям, аквариумы поочередно переключают.
Непрерывный биоконтроль осуществляют с помощью биосигнализатора, где в аквариуме размещены 10 моллюсков, створки раковин которых связаны с датчиками перемещения, формирующими дискретные сигналы, соответствующие двум положениям створок “открыто” или “закрыто”. Сигнал о токсичности формируется при одновременном закрывании створок раковин не менее, чем у 70% моллюсков. Биологический аналитический сигнал – сложное понятие, для него характерно свойство адаптивности.
Одним из новых направлений в аналитической химии является использование микроэлектроники и компьютеров. Это направление включает в себя разработку хемо- и биосенсоров. Химический сенсор – это небольшие устройства, способные непрерывно определять концентрацию химических составляющих в жидкостях или газах и превращать эту информацию в электрический или оптический сигнал в режиме реального времени, как это показано на рис. 1.1:
Отклик
сенсора
Время Рис. 1.1. Изменение сигнала сенсора во времени
Биосенсоры – это безреагентная система, содержащая специфичную к определяемому веществу поверхность, покрытую биомолекулами, распознающими молекулярные участки или их аналоги. Биосенсоры можно сравнить с биорецепторами (датчиками живого организма), которые преобразуют все типы сигналов из окружающей среды в электрические. В основе биосенсоров лежат ферменты – биологические катализаторы. Фермент катализирует только один тип реакций или только одну реакцию вообще.
Например, возьмем датчик кислорода (специальный кислородный электрод Кларка). Покроем его пленкой, содержащей фермент
глюкозоксидазу, и опустим в анализируемый раствор. В присутствии кислорода возможно протекание реакции:
глюкоза + O2 + H2O  глюконовая кислота + H2O2
глюконовая кислота + H2O2
катализатор
глюкозоксидаза
Чем больше глюкозы в растворе, тем больше кислорода расходуется и тем меньше ток в цепи. Никакое другое вещество, кроме глюкозы, этот датчик не определяет. Т.е. можно обследовать больных на сахарный диабет. Вместо датчика можно взять ионочувствительный транзистор. Принцип тот же, но главное преимущество такого биосенсора – небольшие габариты и многофункциональность. Так, в Японии делают многоканальный сенсор на мочевину, глюкозу и калий размером всего 2×6×0,4 мм. Сейчас чистые ферменты в биосенсорах не применяют, а используют препараты тканей многоклеточных растений и животных. Ведь они тоже содержат ферменты, но получать их гораздо проще и дешевле. Например, концентрацию аскорбиновой кислоты в пробе можно определить с помощью электрода на кислород, нанизав на него кусочек свежего огурца или тыквы – источники фермента аскорбиноксидазы. Сейчас сенсоры известны на десятки веществ.
Второе направление – это реализация целых аналитических схем в пределах микроэлектронного плоского чипа (микросхем). Идея была высказана Терри в 1979 году. Она сулила перспективу существенного удешевления анализа. Недавно описана миниатюризированная схема общего химического анализа для контроля объектов окружающей среды. В пределах одной микросхемы осуществляется: подготовка пробы, разделение компонентов, последующая регистрация (всё – автоматически). На кремниевой или стеклянной пластинке методами фотолитографии или наращивания плёнок наносится нужная система коммуникаций. Например, для электрофоретического определения использован капилляр диаметром 1030 мкм длиной 9,6 см, на котором реализуется 70 тыс. теоретических тарелок (интенсивно развивающийся метод капиллярного электрофореза).
Работа по поиску новых аналитических сигналов продолжается. Так, на кафедре аналитической химии Донецкого национального университета профессором Шевчуком И.А.открыт новый аналитический сигнал. При кристаллизации из органических растворителей трибензиламин и другие органические вещества образуют ритмические и волновые структуры, характерные для каждого растворителя и вещества. Образование волновых кристаллизационных структур происходит спонтанно при испарении растворителя. В растворах трибензиламина в органических растворителях образуется до 50 центров кристаллизации на 1 мм2. При испарении растворителя вокруг центров кристаллизации образуются концентрические окружности. Внешние волны от разных центров кристаллизации соприкасаются друг с другом. Зависимость расстояния между концентрическими окружностями от концентрации трибензиламина имеет линейный характер l=kc+b. Этот сигнал основан на явлении ритмической самоорганизации ассоциатов и микрокристаллов.
3. Свойства аналитического сигнала
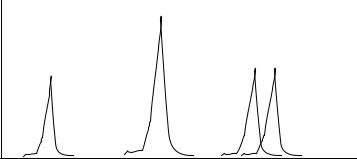
Аналитические сигналы можно изобразить графически. Изобразим сигналы 4-х элементарных объектов (рис. 1.2).
При определённых значениях величины х, представляющей собой константы для данного вещества (tкип, tпл, λ) появляются аналитические сигналы. Компоненты 1 и 2 дают раздельные сигналы, которые могут быть использованы для их качественного обнаружения (по величине х) или для количественного определения по величине у. Сигналы компонентов 3 и 4 перекрываются, поэтому качественное обнаружение и количественное определение невозможны. Один компонент мешает обнаружению другого. Говорят, что сигналы 1 и 2 специфичны, а сигналы 3 и 4 неспецифичны.
y
2
1 |
3 |
4 |
|
|
x
Рис. 1.2. Сигналы четырех различных элементарных объектов:
y – интенсивность аналитического сигнала (масса осадка, интенсивность испускания света и др.); x – переменная величина, постоянная для данного элементарного объекта, т.е. его качественная характеристика (длина волны испускаемого света, температура плавления и др.)
Рис. 1.2 иллюстрирует первое свойство аналитического сигнала –
специфичность.
Если сигналы неспецифичны, то их селективность (специфичность) можно повысить следующими приемами.
1. Маскирование. После маскирования или определения компонента, создают условия, в которых компонент опять даёт сигнал – демаскируют этот компонент. Например, в случае маскирования сигнала иона Fe(III) в присутствии фторид-ионов способом демаскирования может быть
подкисление раствора с последующим удалением летучей HF: F– + H+  HF↑
HF↑
кипячение
2.Предварительное разделение мешающего компонента.
3.Использование другого метода (или сигнала).
Изобразим аналитический сигнал в других координатах (рис. 1.3). Интенсивность аналитического сигнала y зависит от количества n элементарных объектов, вызывающих этот сигнал.

y
n (C, ν, ω и т.д.)
Рис.1.3. Зависимость интенсивности аналитического сигнала от количества элементарных объектов
Математическую функцию y=S·n называют градуировочной функцией, её графическое изображение называется градуировочным графиком.
Коэффициент S называют чувствительностью метода анализа. Чувствиительность – это второе свойство аналитического сигнала. Градуировочный график может быть прямой линией или нелинейной зависимостью. Во втором случае чувствительность S не является постоянной величиной. Коэффициент S имеет смысл тангенса угла наклона линейного градуировочного графика или отклик сигнала на прирост количества элементарных объектов. На рис. 1.4 чувствительность определения у первого сигнала выше, чем у второго.
y 1
2
n
Рис.1.4. Графическое изображение двух аналитических сигналов
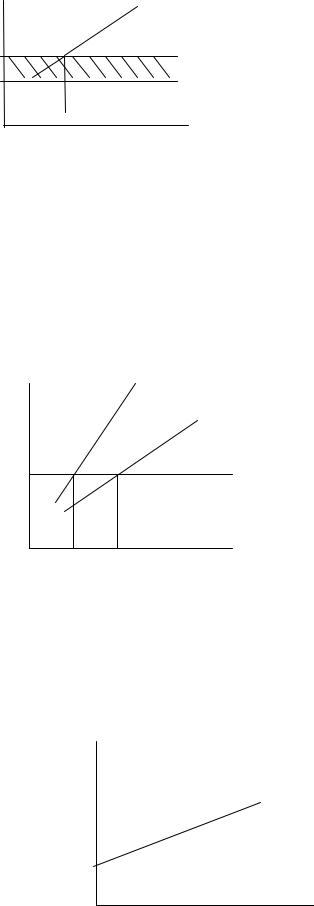
Уменьшение количества элементарных объектов, вызывающих аналитический сигнал, влечет за собой уменьшение интенсивности сигнала. Если интенсивность ниже какого-то определённого и характерного для данного метода значения, в ряде параллельных опытов сигнал удаётся измерить, а в остальных – нет. Говорят, что в таких условиях аналитический сигнал уверенно обнаружить нельзя. Этому положению на рис. 1.5 отвечают интенсивности сигнала в заштрихованной области.
y
nmin |
n |
Рис. 1.5. Определение предела обнаружения сигнала
Ниже него обнаружение не удаётся ни в одном из параллельно проведенных опытов. Верхняя граница заштрихованного интервала определяет величину предела обнаружения. Предел обнаружения – это третье свойство аналитического сигнала.
Значение предела обнаружения зависит от:
1. Величины чувствительности S – чем больше чувствительность, тем лучше (т.е. меньше) предел обнаружения (рис. 1.6);
y |
1 |
2 S1>S2
n1 |
n2 |
n |
Рис.1.6. Пределы обнаружения двух сигналов с различной чувствительностью
2. Величины фона (шума, background).
Фон (шум) – это небольшие случайно возникающие посторонние сигналы, появляющиеся даже при полном отсутствии данных элементарных объектов (рис. 1.7).
y
фон 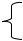
n
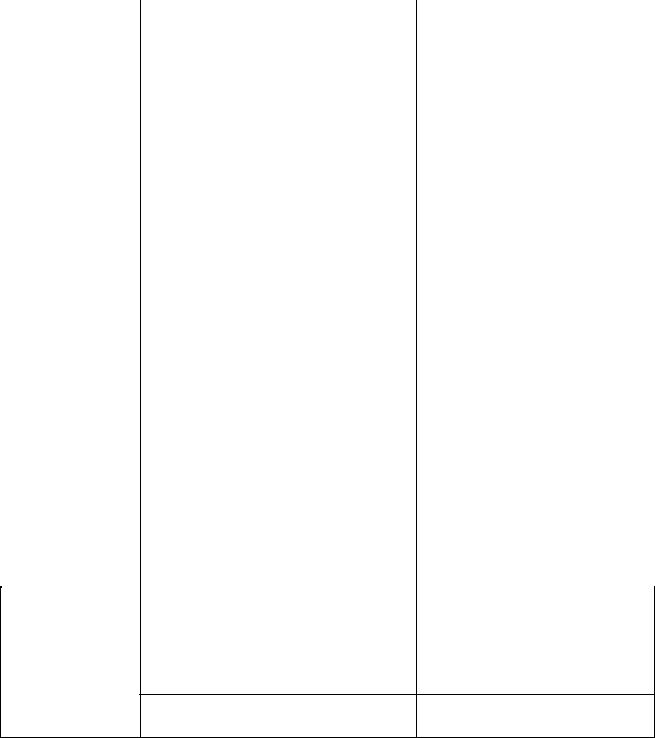
Рис. 1.7. Сигнал, имеющий фон (шум)
Аналитический сигнал должен иметь настолько высокую интенсивность, чтобы он отчётливо выделялся на фоне шума.
С точки зрения теории аналитического сигнала при классификации аналитических методов характер процесса, обуславливающего возникновение аналитического сигнала, должен играть первостепенную роль. На этой основе методы анализа можно подразделять на химические, электрохимические, спектроскопические и радиохимические (табл. 1.1).
Таблица 1.1. Классификация методов анализа
Группа |
|
Измеряемая величина |
|
Название метода |
|||
методов |
|
|
|
|
|
|
|
Химические |
Масса |
|
|
|
|
Гравиметрия |
|
методы |
Объём раствора реагента |
|
Титриметрия |
||||
|
Объём газообразных продуктов |
Газоволюметрия |
|||||
|
реакции |
|
|
|
|
|
|
|
|
|
|
|
|
||
Электрохимиче |
Равновесный |
|
|
потенциал |
Потенциометрия |
||
ские методы |
электродов |
|
|
|
|
|
|
|
Сопротивление |
поляризуемого |
Вольтамперометрия |
||||
|
электрода |
|
|
|
|
|
|
|
|
|
|
||||
|
Количество |
израсходованного |
Кулонометрия |
||||
|
электричества |
|
|
|
|
|
|
|
Электропроводность раствора |
Кондуктометрия |
|||||
|
|
|
|
|
|||
Спектроскопич |
ПОТОК ФОТОНОВ: |
|
|
|
|||
еские методы |
– |
испускаемых |
атомами |
при |
Атомно-эмиссионный |
||
|
переходах внешних электронов |
метод |
|||||
|
|
|
|
|
|
||
|
– |
поглощенных |
атомами |
при |
Атомно-абсорбционный |
||
|
переходах внешних электронов |
метод |
|||||
|
|
|
|
|
|
||
|
– |
испускаемых |
при |
переходах |
Рентгеновская |
||
|
внутренних электронов атомов |
спектроскопия |
|||||
|
– |
поглощённых при переходах |
Фотометрия |
||||
|
внешних |
электронов |
в |
|
|||
|
молекулах |
|
|
|
|
|
|
|
– поглощённых при изменении |
ИК-спектроскопия |
|||||
|
колебательной |
|
энергии |
|
|||
|
молекулы |
|
|
|
|
|
|
|
– |
испускаемых |
атомами |
или |
Люминесцентный анализ |
||
|
молекулами |
|
|
после |
|
||
|
предварительного поглощения |
|
|||||
|
фотонов с |
более |
высокой |
|
|||
|
энергией |
|
|
|
|
|
|
Относительная масса ионов m/e Масс-спектральный анализ при движении в магнитном поле
