
Задача №087
.docxЗадача №87
Масса газа m = 10 г при давлении имеет температуру t = 20 ºС. Как изменится объем газа, если при уменьшении давления в 5 раз его температура увеличится в 2 раза, при этом 20% газа улетучится?
Дано:
m = 10 г = 0,01 кг
t = 20 ºС = 293 K
t1 = 2t
P/P1 = 5
m1 = 0,8m
Найти: V1/V = ?
Решение:
Воспользуемся уравнением Менделеева – Клапейрона, применив его к начальному и конечному состояниям газа:

где М – молярная масса газа; m и m1 – начальная и конечная массы газа; T и T1 – термодинамические температуры газа в начальном и конечном состоянии (в K); R = 8,31 Дж/(моль∙K) – универсальная газовая постоянная.
Приравнивая оба уравнения через
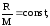 получаем:
получаем:
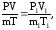
откуда искомое соотношение давлений
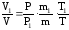 .
.
Учитывая условия задачи (P/P1 = 5, m1 = 0,8m), получаем, что

Предполагая, что в условии начальное (t) и конечное (t1) значение температуры указаны в градусах Цельсия, выполним пересчёт того и другого значения в K:
Т = t + 273 = 293 K;
Т1 = t1 + 273 = 2t + 273 = 313 K;
следовательно,

Ответ: объём газа возрастет в 4,3 раза.
