
Физика, 1 курс 1 семестр ТГМУ / Семинар 4. Особенности молекулярного строения жидкостей
.docxСеминар 4
Особенности молекулярного строения жидкостей
1) Особенности молекулярного течения жидкостей. Время оседлой жизни. Энергия активации.
2) Свойства поверхностного слоя жидкости. Поверхностное натяжение. Зависимость поверхностного натяжения жидкостей от температуры.
3) Методы определения поверхностного натяжения. Метод отрыва кольца.
4) Смачивание и несмачивание. Мениск. Краевой угол.
5) Гидрофобные и гидрофильные жидкости. Идеальное смачивание.
6) Изменение давления под искривленной поверхностью. Формула Лапласа.
7) Капиллярные явления. Высота поднятия жидкости в капилляре. Формула Жюрена.
8) Испарение жидкости. Скорость испарения.
9) Кипение жидкости Точка кипения. Удельная теплота парообразования. Зависимость температуры кипения от давления.
1) Особенности молекулярного течения жидкостей. Время оседлой жизни. Энергия активации.
Особенности молекулярного строения жидкостей: •Обычные жидкости изотропны, структурно они являются аморфными телами. • Для внутреннего строения жидкостей характерен ближний порядок в расположении молекул (упорядоченное расположение ближайших частиц). •Расстояния между молекулами невелики, силы взаимодействия значительны •жидкости мало сжимаемы и обладают большой плотностью •принимают форму сосуда, в котором находятся. Такой характер свойств жидкостей связан с особенностями теплового движения их молекул. По теории Я. И. Френкеля молекулы жидкости колеблются около положений равновесия, однако эти положения равновесия не являются постоянными.
Среднее время «оседлой жизни» молекулы называют временем релаксации т. С повышением температуры и понижением давления время релаксации сильно уменьшается, что обусловливает большую подвижность молекул жидкости и меньшую ее вязкость.
Энергия активации- минимальное количество энергии, которое потребуется сообщить системе, чтобы произошла реакция.
2) Свойства поверхностного слоя жидкости. Поверхностное натяжение. Зависимость поверхностного натяжения жидкостей от температуры.
 Измеряется в Дж/м2.
Измеряется в Дж/м2.
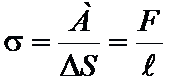 где
A-работа,
затраченная на создание некоторой
поверхности жидкости при постоянной
температуре
S-площадь
поверхности
F-сила
поверхностного натяжения
L-длина
отрезка, на который действует эта сила
где
A-работа,
затраченная на создание некоторой
поверхности жидкости при постоянной
температуре
S-площадь
поверхности
F-сила
поверхностного натяжения
L-длина
отрезка, на который действует эта сила
Поверхностное натяжение зависит от природы жидкости, т.е. от сил притяжения между молекулами данной жидкости и от температуры (с увеличением температуры поверхностное натяжение уменьшается).
С увеличением температуры величина поверхностного натяжения уменьшается и равна нулю при критической температуре.
3) Методы определения поверхностного натяжения. Метод отрыва кольца.
1.Статистические методы- поверхностное натяжение определяется у сформировавшейся поверхности, находящейся в равновесии.
•Метод поднятия в капилляре- Основан на определении высоты столба жидкости h в капилляре радиуса r при полном смачивании;
![]() =
= ![]() ghr/2,
ghr/2,
![]() -
плотность жидкости;
-
плотность жидкости;
g - ускорение свободного падения
•Метод Вильгельми- Измеряется усилие, возникающее в процессе отрыва стеклянной пластины от поверхности жидкости
![]() ,
,
где G0- вес сухой пластины, L- периметр сечения
• Метод вращающейся капли
|
|
Сущностью
метода является измерение диаметра
капли жидкости, вращающейся в более
тяжелой жидкости. Капля жидкости
плотностью r1помещается
в трубку с более тяжелой (плотность
r2)
жидкостью. При вращении трубки с
угловой скоростью w капля вытягивается
вдоль оси, принимая приближенно форму
цилиндра радиуса r. Расчетное ур-ние:
|
2.Динамические методы- связаны с разрушением поверхностного слоя.
• Метод Дю Нуи (метод отрыва кольца).
Платиновое
кольцо поднимают из жидкости, смачивающей
его, усилие отрыва и есть сила поверхностного
натяжения и может быть пересчитано в
поверхностную энергию.
Для отрыва
проволочного кольца радиусом R от пов-сти
жидкости требуется сила
![]()
• Сталагмометрический, или метод счета капель
Метод основан на определении объема капли, вытекающей из капилляра с известным радиусом
![]() (ур-ние
Тейта),
(ур-ние
Тейта),
где G-общий вес n капель, оторвавшихся под действием силы тяжести от среза капиллярной трубки радиусом r.
• Метод максимального давления пузырька (метод Ребиндера)
При выдавливании пузырька в жидкость через калиброванный капилляр радиусом г перед моментом отрыва давление
![]()
• Метод осциллирующей струи
• Метод стоячих волн
• Метод
бегущих волн
![]() ,
,
где:
σ — поверхностное натяжение;
ρ — плотность жидкости;
λ — длина волны;
ν — вынуждающая частота;
g — ускорение свободного падения.
4) Смачивание и несмачивание. Мениск. Краевой угол.
Смачивание наблюдается в том случае, когда силы взаимодействия между молекулами жидкости и твердого тела больше, чем силы взаимодействия между молекулами самой жидкости (вода и стекло).
Сма́чивание — это поверхностное явление, заключающееся во взаимодействии жидкости с поверхностью твёрдого тела или другой жидкости.
Несмачивание наблюдается в том случае, когда силы взаимодействия между молекулами самой жидкости больше чем силы взаимодействия между молекулами жидкости и твёрдого тела (парафин и вода).
Изогнутую поверхность жидкости называют мениском.
Краевой угол-угол между смачиваемой поверхностью и касательной к поверхности жидкости.
5) Гидрофобные и гидрофильные жидкости. Идеальное смачивание.
Гидрофильность- характеристика интенсивности молекулярного взаимодействия вещества с водой, способность хорошо впитывать воду, а также высокая смачиваемость поверхностей водой.
Гидрофобность-это физическое свойство молекулы, которая «стремится» избежать контакта с водой.
6) Изменение давления под искривленной поверхностью. Формула Лапласа.
Под искривленной поверхностью жидкости помимо внутреннего давления создается еще дополнительное давление, обусловленное кривизной поверхности.
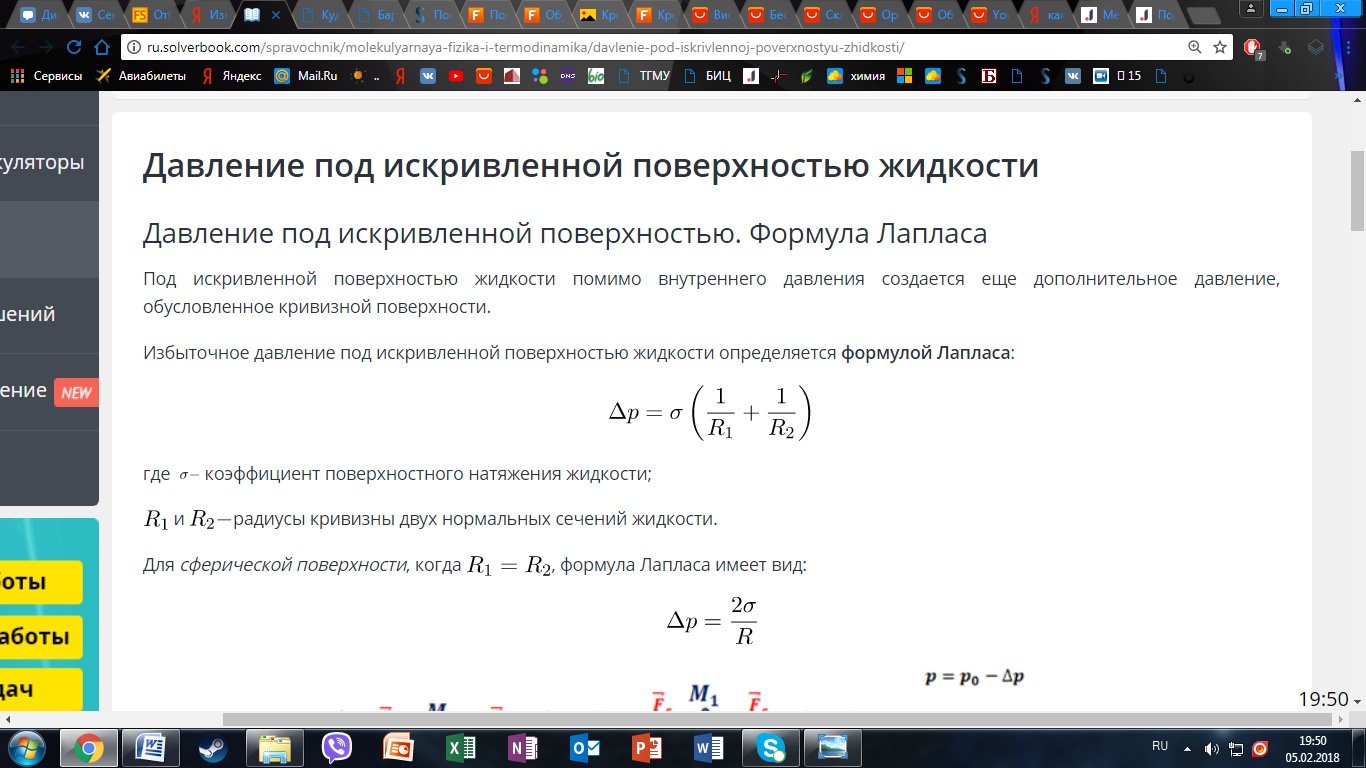
7) Капиллярные явления. Высота поднятия жидкости в капилляре. Формула Жюрена.
Капиллярные явления – это подъем или опускание жидкости в капиллярах по сравнению с уровнем жидкости в широких трубках.
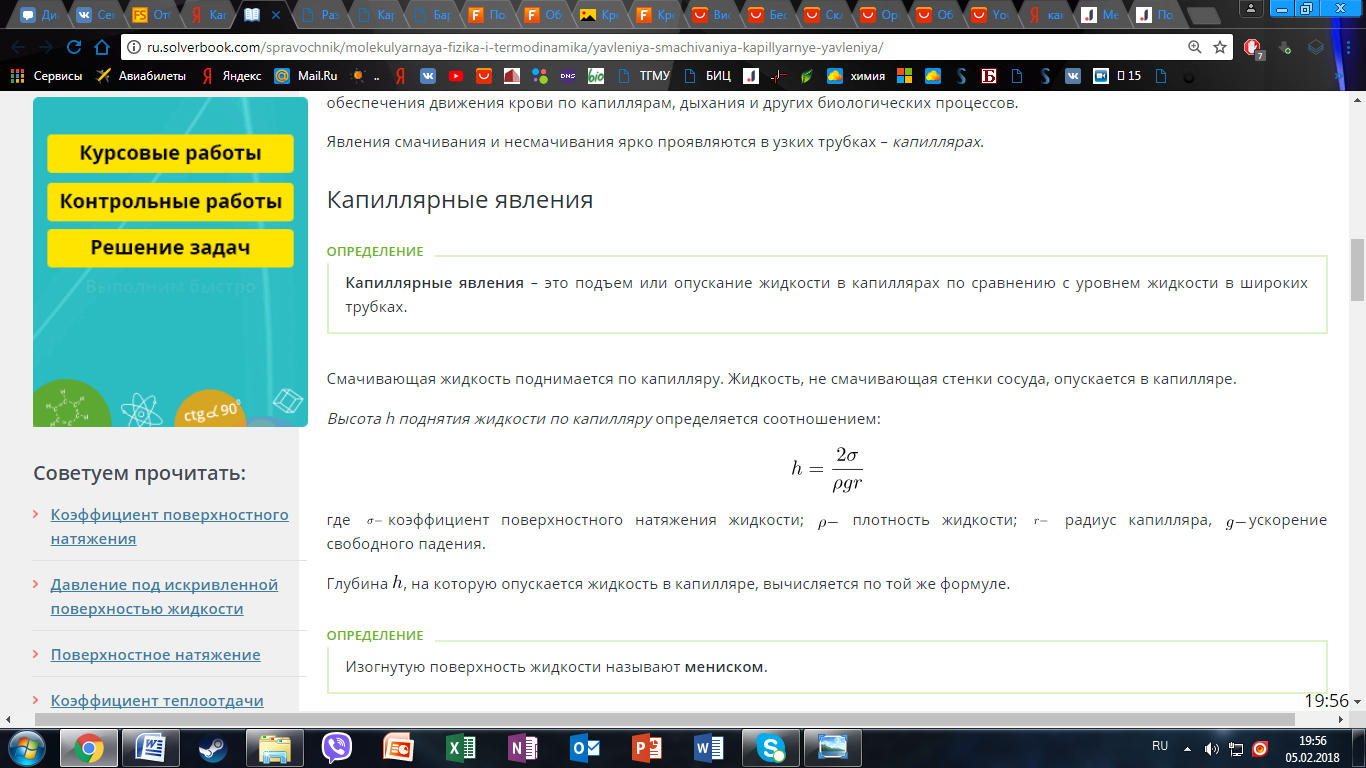
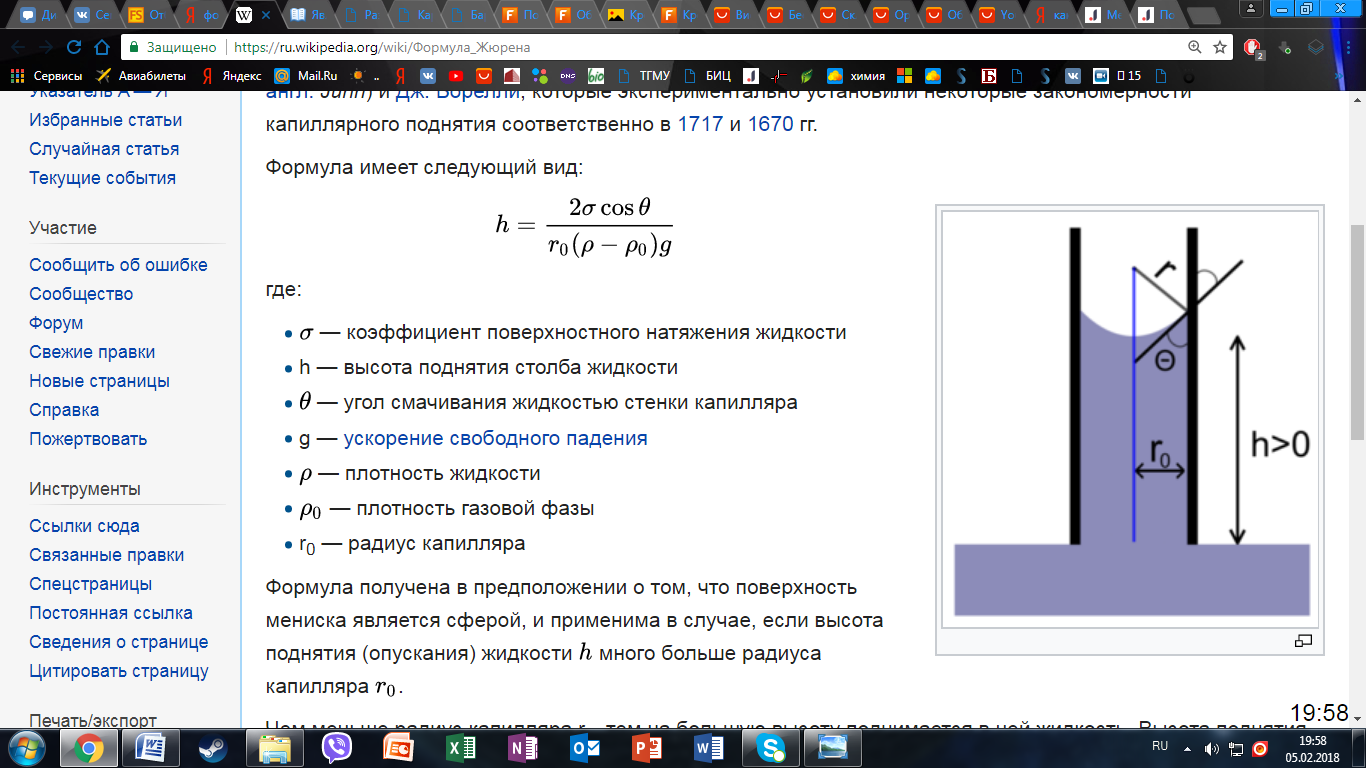
Формула Жюрена- формула, определяющая высоту поднятия жидкости в капиллярах:
Формула
имеет следующий вид:
8) Испарение жидкости. Скорость испарения.
Испарение жидкости- фазовый переход жидкого состояния в газообразное.
Скорость испарения- количество жидкости , испаряющейся со свободной поверхности в единицу времени.
9) Кипение жидкости. Точка кипения. Удельная теплота парообразования. Зависимость температуры кипения от давления.
Кипение жидкости- интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре.
Точка кипения- точка, при которой жидкость кипит.
Удельная теплота парообразования- физическая величина, показывающая , какое количество теплоты необходимо для обращения жидкости в пар при данной температуре и без ее изменения.
С увеличением температуры удельная теплота понижается; при критической температуре она равна нулю.
Предел тякучести характеризует напряжение , при котором деформации продолжают расти без повышения нагрузки.
