
задачи 2 решение
.docx15.21. Из медной руды массой 8 т получили технический металл массой 325 кг (массовая доля меди 98,46%). Определите массовую долю халькозина Cu2S в руде, если других медьсодержащих компонентов в ней нет.
m(Cu) = 325*0,9846 = 319,995 кг
m(Cu2S) = 0,5*m(Cu)*M(Cu2S)/M(Cu) = 400 кг
ω(Cu2S) = (400/8000)*100% = 5%
Ответ: 5%
15.22. Рассчитайте массовую долю меди в ее рудах, одна из которых содержит минерал халькопирит CuFeS2 (массовая доля 6%), а другая – минерал ковелин CuS (массовая доля 4,5%). Вычислите массу меди, которую можно выделить из образца каждой руды массой 100 кг.
ω(Cu в халькопирите) = (M(Cu)/M(CuFeS2))*6% = 2,09%
m(Cu из халькопирита) = 100*0,0209 = 2,09 кг
ω(Cu в ковелин) = (M(Cu)/M(CuS))*4,5% = 3%
m(Cu из ковелина) = 100*0,03 = 3 кг
Ответ: 2,09% и 2,09 кг; 3% и 3 кг
15.17. Вычислите массовые доли минерала магнетита Fe3O4 и пустой породы в железной руде, если из образца этой руды массой 500 г получили железо массой 200 г.
m(Fe3O4) = m(Fe)*M(Fe3O4)/(3*M(Fe))
ω(Fe3O4) = (m(Fe)*M(Fe3O4)/(3*M(Fe)*m(руды)))*100% = 55,2%
ω(пустой породы) = 100 – 55,2 = 44,8%
Ответ: 55,2% магнетита и 44,8% пустой породы
15.13. Медная руда содержит минерал малахит CuCO3 ∙ Cu(OH)2 (массовая доля 7%) и другие компоненты, в состав которых медь не входит. Какую массу меди можно получить из 300 кг такой руды?
m(Cu) = m(малахита)*ω(меди в малахите) = m(руды)*ω(малахита)*2*M(Cu)/M(CuCO3 ∙ Cu(OH)2) = 300*0,07*2*M(Cu)/M(CuCO3 ∙ Cu(OH)2) = 12,1 кг
Ответ: 12,1 кг
15.25. Медная руда содержит минералы куприт Cu2O, тенорит CuO и пустую породу (массовая доля пустой породы 80%). Из образца такой руды массой 20 кг выделили металлическую медь массой 3,328 кг. Вычислите массовые доли куприта и тенорита в руде.
n(Cu) = 3,328*1000/M(Cu) = 52 моль
ω(Cu2O + CuO) = (1 – 0,8)*20 = 4 кг
Пусть m(Cu2O) = x кг. Тогда:
n(Cu из куприта) = 2*n(Cu2O) = 2*x/144 = x/72 моль
n(Cu из тенорита) = 52 – x/72
m(CuO) = n(Cu из тенорита)*80 = 4160 – (10/9)*x
4000 = x + 4160 – (10/9)*x
x = 160*9 = 1440
m(CuO) = 4000 – x = 2560 г
ω(Cu2S) = (1440/20000)*100% = 7,2%
ω(CuO) = (2560/20000)*100% = 12,8%
Ответ: 7,2% Cu2O, 12,8% CuO
14.36. Реакция разложения карбоната кальция является эндотермической:
CaCO3 = CaO + CO2 – 180 кДж
Рассчитайте, сколько теплоты поглотится при разложении карбоната кальция массой 20 г.
n(CaCO3) = 20/100 = 0,2 моль
1 моль – 180 кДж
0,2 моль – x кДж
x = 0,2*180 = 36
Ответ: 36 кДж
13.27. Аммиак объемом 1,12 л (нормальные условия) прореагировал с галогеноводородом. При этом образовалась соль аммония массой 4,9 г. Определите, какой галогеноводород реагировал с аммиаком.
n(NH3) = 1,12/22,4 = 0,05 моль
NH3 + HX = NH4X
n(NH4X) = n(NH3) = 0,05 моль
M(NH4X) = 4,9/0,05 = 98
M(X) = 98 – 14 – 4 = 80
X – бром
Ответ: HBr
13.20. При разложении галогенида аммония массой 4,9 г получен аммиак объемом 1,12 л (объем приведен к нормальным условиям). Какой галогенид был взят?
NH4X = NH3 + HX
n(NH3) = 1,12/22,4 = 0,05 моль
n(NH4X) = n(NH3) = 0,05 моль
M(NH4X) = 4,9/0,05 = 98
M(X) = 98 – 14 – 4 = 80
X – бром
Ответ: NH4Br
20.75. Рассчитайте массу бромной воды (массовая доля Br2 3,2%), которая обесцвечивается ацетиленом, полученным из карбида кальция массой 40 г. Карбид содержит посторонние примеси, массовая доля которых равна 4%.
CaC2 + 2H2O = Ca(OH)2 + C2H2↑
n(C2H2) = n(CaC2) = 40*(1 – 0,04)/64 = 0,6 моль
C2H2 + 2Br2 = C2H2Br4
n(Br2) = 2n(C2H2) = 1,2 моль
m(Br2) = 1,2*160 = 192 г
m(бромной воды) = 192*100/3,2 = 6000 г = 6 кг
Ответ: 6 кг
20.31. 2-метилпропен объемом 0,784 л (нормальные условия) сожгли. Выделившийся оксид углерода (IV) полностью нейтрализовали водным раствором гидроксида натрия (массовая доля NaOH 15%, плотность 1,17 г/мл). Рассчитайте объем раствора щелочи, затраченного на нейтрализацию.
C4H8 + 6O2 = 4CO2 + 4H2O
n(C4H8) = 0,784/22,4 = 0,035 моль
n(CO2) = 4*n(C4H8) = 0,14 моль
CO2 + 2NaOH = Na2CO3 + H2O
n(NaOH) = 2n(CO2) = 0,28 моль
m(NaOH) = 0,28*40 = 11,2 г
m(NaOH, 15%) = 11,2*100/15 = 74,67 г
V(NaOH, 15%) = 74,67/1,17 = 63,8 мл
Ответ: 63,8 мл
20.29. При термическом крекинге пропана объемом 13,44 л (нормальные условия) получена смесь метана и этилена. Рассчитайте массу бромной воды, которую могут обесцветить продукты крекинга (массовая доля Br2 в бромной воде равна 3,2%).
CH3CH2CH3 = CH4 + C2H4
C2H4 + Br2 = C2H4Br2
n(Br2) = n(C3H8) = 13,44/22,4 = 0,6 моль
m(Br2) = 0,6*160 = 96 г
m(бромной воды) = 96*100/3,2 = 3000 г = 3 кг
Ответ: 3 кг
21.27. Смесь бензола и стирола обесцветила бромную воду массой 500 г (массовая доля Br2 в бромной воде равна 3,2%). При сгорании смеси той же массы выделился оксид углерода (IV) объемом при нормальных условиях 44,8 л. Определите массовую долю бензола в смеси со стиролом.
n(Br2) = 500*0,032/160 = 0,1 моль
n(CO2) = 44,8/22,4 = 2 моль
n(C) = 2 моль = 6n(C6H6) + 8n(C6H5CHCH2)
n(Br2) = n(C6H5CHCH2)
2 моль = 6n(C6H6) + 8*0,1 моль
n(C6H6) = 0,2 моль
m(C6H6) = 0,2*78 = 15,6 г
m(C6H5CHCH2) = 0,1*104 = 10,4 г
ω(C6H6) = (15,6/(15,6 + 10,4))*100% = 60%
Ответ: 60%
22.16. Природный газ содержит метан (объемная доля 90%), этан (6%), азот (2%), оксид углерода (IV) и другие негорючие примеси (2%). Рассчитайте объем воздуха (объемная доля кислорода 21%), который потребуется для сгорания образца этого газа объемом 840 л (все объемы отнесены к нормальным условиям).
CH4 + 2O2 = CO2 + 2H2O
C2H6 + 3,5O2 = 2CO2 + 3H2O
V(O2) = 840*(0,9*2 + 0,06*3,5) = 1688,4 л
V(воздуха) = 1688,4*100/21 = 8040 л = 8 м3
Ответ: 8 м3
5.34. Соляная кислота используется для удаления ржавчины и оксидов с поверхности металлов. Рассчитайте массу раствора, в котором массовая доля HCl равна 20%, который потребуется для удаления 69,6 г железной окалины Fe3O4. При решении учтите, что в результате реакции образуется смесь хлоридов железа (II) и (III).
Fe3O4 + 8HCl = FeCl2 + 2FeCl3 + 4H2O
n(Fe3O4) = 69,6/232 = 0,3 моль
m(HCl) = 8*0,3*36,5 = 87,6 г
m(HCl, 20%) = 87,6*100/20 = 438 г
Ответ: 438 г
9.18. Рассчитайте объем хлороводорода, приведенный к нормальным условиям, который содержится в 200 г соляной кислоты с массовой долей HCl 14,6%.
m(HCl) = 200*0,146 = 29,2 г
n(HCl) = 29,2/36,5 = 0,8 моль
V(HCl) = 0,8*22,4 = 17,92 л
Ответ: 17,92 л
9.22. К цинку массой 6,5 г прибавили 150 г раствора соляной кислоты с массовой долей HCl 20%. Какой объем водорода, измеренный при нормальных условиях, может быть получен при этом?
Zn + 2HCl = ZnCl2 + H2↑
n(Zn) = 6,5/65 = 0,1 моль
n(HCl) = 150*0,2/36,5 = 0,82 моль
HCl в избытке.
n(H2) = n(Zn) = 0,1 моль
V(H2) = 0,1*22,4 = 2,24 л
Ответ: 2,24 л
9.25. К 60 мл раствора соляной кислоты с массовой долей HCl 20% и плотностью 1,1 г/мл добавили избыток цинка. Рассчитайте, какую массу хлорида цинка можно будет выделить из полученного раствора.
Zn + 2HCl = ZnCl2 + H2↑
n(HCl) = 60*1,1*0,2/36,5 = 0,36 моль
n(ZnCl2) = 0,5n(HCl) = 0,18 моль
m(ZnCl2) = 0,18*136 = 24,6 г
Ответ: 24,6 г
11.25. При образовании сероводорода из простых веществ выделяется теплота в количестве 21 кДж. Определите, сколько выделится теплоты при взаимодействии 70,4 г серы с избытком водорода.
S + H2 = H2S + 21 кДж
n(S) = 70,4/32 = 2,2 моль
Q = 21*2,2 = 46,2 кДж
Ответ: 46,2 кДж
5. Какую массу железа (в г) можно получить из:
а) 2,30 г оксида железа (III);
б) 5,30 г Fe(NO3)3 ∙ 7H2O;
в) 4,8 г магнетита Fe3O4;
г) 1,20 г пирита FeS2?
а) m(Fe) = 2,30*2*56/(56*2 + 16*3) = 1,61 г;
б) m(Fe) = 5,30*56/(56 + 62*3 + 7*18) = 0,8 г;
в) m(Fe) = 4,8*3*56/(56*3 + 16*4) = 3,48 г;
г) m(Fe) = 1,20*56/(56+32*2) = 0,56 г
Ответ: а) 1,16; б) 0,8; в) 3,48; г) 0,56
8. Рассчитайте химическое количество атомарного кислорода в:
а) 1,5 моль бертолетовой соли KClO3;
б) 5,6 дм3 (н. у.) SO2;
в) 14,2 г Na2SO4;
г) 12,04∙1024 молекулах CO2.
а) n(O) = 3*1,5 = 4,5 моль;
б) n(O) = 2*5,6/22,4 = 0,5 моль;
в) n(O) = 4*14,2/142 = 0,4 моль;
г) n(O) = 2*120,4/6,02 = 40 моль.
Ответ: а) 4,5 моль; б) 0,5 моль; в) 0,4 моль; г) 40 моль
36. Найдите массовую долю нитрита натрия NaNO2 в водном растворе, если известно, что в 15,0 г такого раствора содержится 4,8∙1023 атомов кислорода.
n(O) = 4,8/6,02 = 0,797342 моль
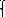 Пусть
в 15 г раствора содержится x
моль NaNO2
и y
моль H2O.
Тогда:
Пусть
в 15 г раствора содержится x
моль NaNO2
и y
моль H2O.
Тогда:
2x + y = 0,797342
69x + 18y = 15
69x + 18*(0,797342 – 2x) = 15
33x = 0,648
x = 0,0196
m(NaNO2) = 69x = 1,355 моль
ω(NaNO2) = (1,355/15)*100% = 9,03%
Ответ: 9,03%
27. Массовая доля нитрата аммония в смеси с некоторой солью Me(NO3)2 составляет 60%, а массовая доля атомов элемента азота в этой же смеси равна 27,83%. Установите металл Me.
Пусть в смеси x моль Me(NO3)2, а масса смеси 100 г.
m(NH4NO3) = 60 г
m(Me(NO3)2) = 40 г
x = 40/(M(Me) + 124)
n(NH4NO3) = 60/80 = 0,75 моль
m(N) = 27,83 г
n(N) = 27,83/14 = 1,99 моль
x = (n(N) – 2*n(NH4NO3)/2 = 0,24393
0,24393 = 40/(M(Me) + 124)
0,24393*M(Me) = 9,752857
M(Me) = 40 г/моль
Ответ: Ca - кальций
15. Смесь равных по массе Zn и CaCO3 обработали избытком соляной кислоты. Найдите плотность полученной смеси газов, равную отношению суммарной массы газов к их суммарному объему.
m(Zn) = m(CaCO3) = m
Zn + 2HCl = ZnCl2 + H2↑
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
n(H2) = n(Zn) = m/65
n(CO2) = n(CaCO3) = m/100
m(H2) = 2m/65
m(CO2) = 44m/100
V(H2) = 22,4m/65
V(CO2) = 22,4m/100
ρ(смеси газов) = (2/65 + 44/100)/(22,4*(1/65 + 1/100)) = 0,828 г/л
Ответ: 0,828 г/л
6. При сжигании пирита и сульфида цинка массой 251,2 г в избытке кислорода получено 71,68 дм3 SO2 (н. у.). Определите массы веществ в исходной смеси.
4FeS2 + 11O2 = 2Fe2O3 + 8SO2↑
2ZnS + 3O2 = 2ZnO + 2SO2↑
n(SO2) = 71,68/22,4 = 3,2 моль
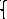 Пусть
в исходной смеси было x
моль FeS2
и y
моль ZnS.
Тогда:
Пусть
в исходной смеси было x
моль FeS2
и y
моль ZnS.
Тогда:
2x + y = 3,2
120x + 97y = 251,2
120x + 97(3,2 – 2x) = 251,2
74x = 59,2
x = 0,8
y = 1,6
m(FeS2) = 0,8*120 = 96 г
m(ZnS) = 1,6*97 = 155,2 г
Ответ: m(FeS2) = 96 г; m(ZnS) = 155,2 г
6. Сульфид железа (II) массой 176 г обработали избытком соляной кислоты, а полученный газ сожгли в избытке воздуха. Какой объем раствора KOH (ω = 40%, ρ = 1,4 г/см3) нужен для полной нейтрализации полученного при сжигании газа?
FeS + 2HCl = FeCl2 + H2S↑
H2S + 1,5O2 = SO2 + H2O
2KOH + SO2 = K2SO3 + H2O
n(KOH) = 2n(SO2) = 2n(FeS) = 2*176/88 = 4 моль
m(KOH) = 4*56 = 224 г
m(KOH, 40%) = 224*100/40 = 560 г
V(KOH, 40%) = 560/1,4 = 400 мл
Ответ: 400 мл
38. Хлор объемом 6,72 дм3 (н. у.) пропустили через 250 см3 (ρ = 1,11 г/см3) горячего раствора с ω(KOH) = 12,1%. Хлорат калия был выделен и использован для получения кислорода. Найдите массовые доли солей в растворе после пропускания хлора. Какой объем кислорода (н. у.) получен?
3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
KClO3 = KCl + (3/2)O2 (кат. MnO2)
n(Cl2) = 6,72/22,4 = 0,3 моль
n(KOH) = 250*1,11*0,121/56 = 0,6 моль
Количества веществ Cl2 и KOH соответствуют уравнению реакции.
m(р-ра) = m(р-ра KOH) + m(Cl2) = 250*1,11 + 71*0,3 = 298,8 г
n(KCl) = (5/3)*0,3 = 0,5 моль
n(KClO3) = (1/3)*0,3 = 0,1 моль
m(KCl) = 0,5*74,5 = 37,25 г
m(KClO3) = 0,1*122,5 = 12,25 г
ω(KCl) = (37,25/298,8)*100% = 12,5%
ω(KClO3) = (12,25/298,8)*100% = 4,1%
n(O2) = (3/2)*0,1 = 0,15 моль
V(O2) = 0,15*22,4 = 3,36 л
Ответ: ω(KCl) = 12,5%, ω(KClO3) = 4,1%; 3,36 л
39. Избыток хлора пропустили через 200 г горячего раствора KOH. При разложении одной из полученных солей получили 4 дм3 (н. у.) кислорода. Какой была ω(KOH) в растворе?
3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
KClO3 = KCl + (3/2)O2 (кат. MnO2)
n(KOH) = 6n(KClO3) = (2*6/3)n(O2) = 4n(O2) = 16/22,4 моль
m(KOH) = 16*56/22,4 = 40 г
ω(KOH) = (40/200)*100% = 20%
Ответ: 20%
49. При обработке избытком хлорной воды смеси FeBr2 и CuBr масса сухого остатка, полученного после выпаривания раствора, уменьшилась в 1,20 раза по сравнению с массой исходной смеси солей. Вычислите массовые доли веществ в конечной смеси.
FeBr2 + 1,5Cl2 = FeCl3 + Br2
2CuBr + 2Cl2 = 2CuCl2 + Br2
Пусть в смеси x моль FeBr2 и y моль CuBr. Тогда:
(m(FeBr2) + m(CuBr))/(m(FeCl3) + m(CuCl2)) = 1,2
 Пусть
масса смеси равна 100 г:
Пусть
масса смеси равна 100 г:
x*216 + y*144 = 100
1,2*(x*162,5 + y*135) = 100
x = 0,261 моль
y = 0,302 моль
m(конеч. смеси) = 100/1,2 = 83,33 г
ω(FeCl3) = (0,261*162,5/83,33)*100% = 50,9%
ω(CuCl2) = 100 – 50,9 = 49,1%
Ответ: ω(FeCl3) = 50,9%, ω(CuCl2) = 49,1%
50. Нагревание соляной кислоты с 30°С до 50°С снижает массовую долю хлороводорода втрое. Какая масса газа выделится при нагревании от 30°С до 50°С раствора массой 250 г с ω(HCl) = 24,0%?
m(HCl улет.) = x г
24,0/3 = 8
0,08 = (250*0,24 – x)/(250 - x)
20 – 0,08x = 60 – x
0,92x = 40
x = 43,5
Ответ: 43,5 г
5. Найдите массовую долю серной кислоты, если при полном растворении меди в 78,4 г горячего раствора этой кислоты выделяется газ, взаимодействие которого с избытком сероводорода дает 19,2 г серы.
Cu + 2H2SO4 = CuSO4 + SO2↑ + 2H2O
SO2 + 2H2S = 3S + 2H2O
n(H2SO4) = 2n(SO2) = 2n(S)/3 = 2*19,2/(3*32) = 0,4 моль
m(H2SO4) = 0,4*98 = 39,2 г
ω(H2SO4) = (39,2/78,4)*100% = 50%
Ответ: 50%
13. Смесь меди и оксида меди (II) обработали 100,85 см3 раствора хлороводородной кислоты с ω = 36,5% (ρ = 1,19 г/см3). Осадок отфильтровали и растворили в концентрированной серной кислоте, при этом выделилось 11,2 дм3 газа (н. у.). Фильтрат нейтрализовали раствором (ρ = 1,28 г/см3) с ω(NaOH) = 25%, при этом образовалось 39,2 г осадка. Рассчитайте массовые доли компонентов в исходной смеси и объем использованного раствора гидроксида натрия.
Cu + HCl → ×
CuO + 2HCl = CuCl2 + H2O
Cu + 2H2SO4 = CuSO4 + SO2↑ + 2H2O
HCl + NaOH = NaCl + H2O
CuCl2 + 2NaOH = Cu(OH)2 + 2NaCl
n(HCl) = 100,85*1,19*0,365/36,5 = 1,2 моль
n(Cu) = n(SO2) = 11,2/22,4 = 0,5 моль
n(CuO) = n(Cu(OH)2) = 39,2/98 = 0,4 моль
m(Cu) = 0,5*64 = 32 г
m(CuO) = 0,4*80 = 32 г
ω(Cu) = ω(CuO) = 50%
HCl в избытке. В фильтрате осталось 1,2 – 2*0,4 = 0,4 моль HCl.
На нейтрализацию HCl и осаждение Cu(OH)2 необходимо 0,4 + 2*0,4 = 1,2 моль NaOH.
m(NaOH) = 1,2*40 = 48 г
m(NaOH, 25%) = 48*4 = 192 г
V(NaOH, 25%) = 192/1,28 = 150 мл
Ответ: ω(Cu) = ω(CuO) = 50%; 150 мл
18. Имеется смесь карбоната кальция, сульфида цинка и хлорида натрия. Если на 40 г этой смеси подействовать избытком соляной кислоты, выделится 6,72 дм3 газов (н. у.), при взаимодействии которых с избытком оксида серы (IV) образуется 9,6 г осадка. Определите массы компонентов в смеси.
CaCO3 + 2HCl =CaCl2 + H2O + CO2↑
ZnS + 2HCl = ZnCl2 + H2S↑
NaCl + HCl → ×
CO2 + H2S → ×
2H2S + SO2 = 3S + 2H2O
n(ZnS) = n(H2S) = (2/3)n(S) = (2/3)*9,6/32 = 0,2 моль
m(ZnS) = 0,2*97 = 19,4 г
m(CaCO3) + m(NaCl) = 40 – 19,4 = 20,6 г
n(CO2) + n(H2S) = 6,72/22,4 = 0,3 моль
n(CaCO3) = n(CO2) = 0,3 – 0,2 = 0,1 моль
m(CaCO3) = 0,1*100 = 10 г
m(NaCl) = 20,6 – 10 = 10,6 г
Ответ: 10 г CaCO3, 19,4 г ZnS и 10,6 г NaCl
7. Смесь меди, железа и алюминия массой 17,8 г обработали при комнатной температуре азотной кислотой и получили 4,48 дм3 (н. у.), бурого газа. При действии на такую же смесь соляной кислотой получили 8,96 дм3 (н. у.) водорода. Чему равны массы металлов в смеси?
Cu + 4HNO3 (конц.) = Cu(NO3)2 + 2NO2↑ + 2H2O
Fe + HNO3 (конц.) → ×
Al + HNO3 (конц.) → ×
n(Cu) = n(NO2)/2 = 4,48/(22,4*2) = 0,1 моль
m(Cu) = 0,1*64 = 6,4 г
m(Fe) + m(Al) = 17,8 – 6,4 = 11,4 г
Cu + HCl → ×
Fe + 2HCl = FeCl2 + H2↑
Al + 3HCl = FeCl3 + (3/2)H2↑
n(H2) = 8,96/22,4 = 0,4 моль
 Пусть
в смеси x
моль Fe
и y
моль Al.
Тогда:
Пусть
в смеси x
моль Fe
и y
моль Al.
Тогда:
56x + 27y = 11,4
x + (3/2)y = 0,4
56(0,4 – 1,5y) + 27y = 11,4
11 = 57y
y = 11/57 = 0,19
x = 0,11
m(Fe) = 56x = 11,4 – 11*27/57 = 6,2 г
m(Al) = 11,4 – 6,2 = 5,2 г
Ответ: 6,4 г меди, 6,2 г железа и 5,2 г алюминия
