
- •Карбоновые кислоты
- •Классификация карбоновых кислот:
- •Номенклатура. Рациональная: к названию
- •производят от соответствующего углеводорода, добавляя суффикс -овая, атом углерода карбоксильной группы
- •Названия кислот
- •Способы получения
- •-ЖЕСТКОЕ ОКИСЛЕНИЕ боковой
- •- ЖЕСТКОЕ ОКИСЛЕНИЕ СПИРТОВ:
- •2. Гидролиз геминальных трига-
- •3. Гидролиз нитрилов
- •4. Через металлоорганические соединения
- •ФИЗИЧЕСКИЕ СВОЙСТВА С1С9 - бесцветные жидкости.
- •Низшие члены гомологического ряда алифатических монокарбоновых кислот смешиваются с водой в любых пропорциях.
- •Химические свойства
- •Качественная реакция на карбоновые кислоты – реакция с содой → выделение углекислого газа
- •Химические свойства солей карбоновых кислот:
- •б) декарбоксилирование солей карбоновых кислот (см. алканы)
- •в) пиролиз солей Са и Ва
- •2) Реакции с разрывом связи С-ОН идут с образованием функциональных производных
- •1. Получение галогенангидридов.
- •Химические свойства галогенангидридов:
- •2. Получение ангидридов кислот : а) из кислот
- •б) из соли кислоты и галогенангидрида кислоты
- •Химические свойства ангидридов кислот:
- •3. Образование сложных эфиров.
- •б) реакции галогенангидридов кислот со спиртами
- •Химические свойства сложных эфиров – реакции гидролиза
- •4. Образование амидов кислот
- •б) Из ангидридов кислот:
- •Химические свойства амидов кислот:
- •2. Реакции по α-углеродному атому - идут с образованием замещенных кислот.
- •- Реакции по ароматическому кольцу- карбоксильная группа ориентант II рода.
- •Ароматические кислоты Бензойная кислота: содержится в клюкве, бруснике
- •Ненасыщенные кислоты
- •Метакриловая кислота – в
- •Двухосновные кислоты -
- •COOH COOH
- •Химические свойства: 1. Кислотные – образуют с
- •Терефталевая кислота
- •Высшие жирные кислоты Пальмитиновая- С15Н31СООН,
- •Жиры - сложные эфиры глицерина и высших кислот
- •Физические свойства: не имеют определенной Тпл, не растворимы в воде, с водой образуют
- •Химческие свойства:
Карбоновые кислоты
Карбоновые кислоты – производные углеводородов, которые содержат в молекуле функциональную группу:
карбоксильную O
C OH
Общая формула: CnH2nO2
Классификация карбоновых кислот:
По числу карбоксильных групп:
-монокарбоновые- одноосновные
-дикарбоновые - двухосновные
-трикарбоновые и т.д.
Номенклатура. Рациональная: к названию
углеводородных радикалов добавляется название основы – уксусная кислота
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
CH3 |
O |
CH2 |
Ñ |
|||||
ÑH3 |
|
|
|
|
|
|
C |
|
Î H |
|||
|
|
|
|
|
|
|
||||||
|
|
|
CH |
|
OH |
ф ен илуксусн ая |
||||||
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||
äèì åòèëуксусн ая |
||||||||||||
кисло т а |
|
|
кисло та |
|||||||||
CH2 |
|
CH |
|
|
CH2 |
O |
âèí èëуксусн ая кисло та |
|||||
|
|
Ñ |
||||||||||
|
|
|||||||||||
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
Î H |
|
|
производят от соответствующего углеводорода, добавляя суффикс -овая, атом углерода карбоксильной группы
начинает нумерацию: |
2 |
1 O |
||
4 |
3 |
|||
ÑH2 |
|
CH |
CH2 |
C |
|
||||
|
||||
|
||||
|
||||
|
|
|
|
Î H |
бут-3-ен о вая кисло та |
||||
5 |
4 |
3 |
2 |
1 O |
|||||
ÑH3 |
|
|
CH |
CH2 |
|
CH |
C |
||
|
|||||||||
|
|||||||||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
Î H |
|
|
|
|
|
|
Cl |
|||
|
OH |
|
|||||||
4-гидро ки-2-хло рп ен тан о вая
кисло та
Названия кислот
Название кислоты |
Формула |
Метановая |
Н–СООН |
(муравьиная) |
СН3–СООН |
Этановая |
|
(уксусная) |
СН3–СН2–СООН |
Пропановая |
|
(пропионовая) |
СН3–СН2–СН2–СООН |
Бутановая |
|
(масляная) |
СН3–СН2–СН2–СН2–СООН |
Пентановая |
|
(валериановая) |
СН3–СН2–СН2–СН2–СН2–СООН |
Гексановая |
|
(капроновая) |
(СН3)2СН2–СООН |
Изомасляная |
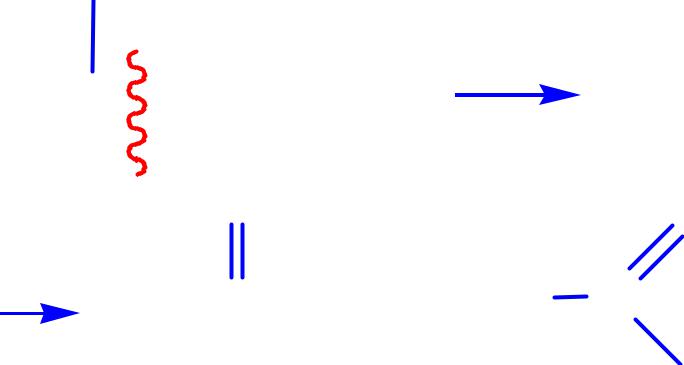
Способы получения
1. ЖЕСТКОЕ ОКИСЛЕНИЕ УВ: -АЛКАНОВ, АЛКЕНОВ, АЛКИНОВ
CH3 |
|
|
KMnO4 |
|
CH3-C=CH2-CH3 |
||||
H2SO4 |
||||
|
O |
|
||
|
|
O |
||
CH |
-C-CH |
|
+ H3C C |
|
-MnO2 3 |
|
3 |
OH |
|
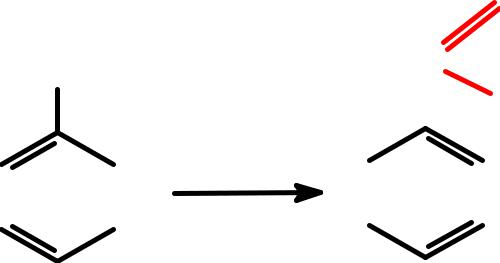
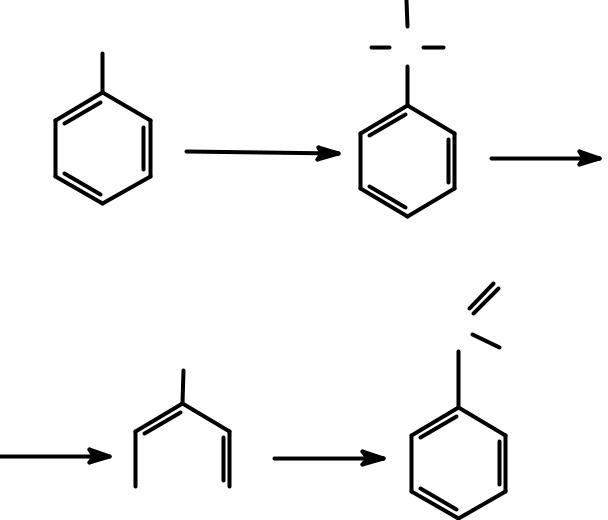
-ЖЕСТКОЕ ОКИСЛЕНИЕ боковой
цепочки аренов
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
CH3 |
|
|
CH-CH3 |
|
|
|
C |
|
OH |
||||||||
|
|
||||||||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
KMnO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ CO2+ MnO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
H2SO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
изо п ро п илбен зо л |
|
|
|
|
|
|
|
|
|||||||||
êóì î ë |
|
|
|
|
|
|
|
|
|
|
|
|
|||||

- ЖЕСТКОЕ ОКИСЛЕНИЕ СПИРТОВ:
CH3 CH2 CH2 OH Na2Cr2O7/H2SO4
O CH3 CH2 C Î H
Î H
2. Гидролиз геминальных трига-
логензамещенных УВ |
Cl |
CH3 |
Cl C Cl |
3Cl2/hv |
H2O |
|
-3HCl |
OH O
|
|
|
|
|
|
OH |
C OH |
HO |
|
C |
|
||||
|
|
||||||
|
|
||||||
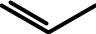 -H2O ãåì òðèî ë
-H2O ãåì òðèî ë
3. Гидролиз нитрилов
CH3-CH2-C N H2O/H
н итрил п ро п ан о во й кисло ты
O  CH3-CH2-C
CH3-CH2-C
OH
CH3-CH2-C O H2O/H àì èä NH2-NH3
O H2O/H àì èä NH2-NH3
п ро п ан о во й кисло ты
