
- •Биоорганическая химия
- •Теория строения органических соединений а.М.Бутлерова.
- •Классификация и номенклатура органических соединений.
- •Основные классы органических соединений
- •Образование и типы химических связей в органических соединениях.
- •Классификация органических реакций.
- •По характеру изменений связей в субстрате и реагенте.
- •Э электрофил лектрофильная реакция:
- •Н Нуклеофил уклеофильная реакция:
- •В соответствии с конечным результатом.
- •Электрофильное замещение se
- •Электрофильное присоединение аe
- •По числу частиц, принимающих участие в элементарной стадии.
- •Взаимное влияние атомов в молекулах органических соединений и способы его передачи.
- •Сопряжение.
- •Кислотность и основность органических соединений
- •Кислотность и основность по Бренстеду.
- •Кислоты и основания Льюиса.
- •Жесткие и мягкие кислоты и основания.
- •План описания органических соединений:
- •Алканы (предельные, насыщенные углеводороды, парафины)
- •Физические свойства.
- •Способы получения.
- •Промышленные
- •Лабораторные
- •Химические свойства.
- •Реакции галогенирования
- •Нитрование (реакция Коновалова)
- •3. Сульфирование и сульфохлорирование.
- •4. Окисление.
- •5. Изомеризация.
- •6. Дегидрирование.
- •7. Крекинг.
- •I. Промышленные.
- •Лабораторные.
- •Дегидратация спиртов:
- •Химические свойства.
- •Реакции присоединения.
- •3) Присоединение галогеноводородов (гидрогалогенирование):
- •4) Присоединение воды (гидратация):
- •2. Реакции окисления.
- •4) Озонолиз (окисление озоном):
- •3. Реакции полимеризации.
- •I. Промышленные.
- •II. Лабораторные.
- •Дегалогенирование тетрагалогенпроизводных:
- •Химические свойства.
- •Реакции электрофильного присоединения.
- •Присоединение галогенов (галогенирование):
- •Присоединение галогеноводородов:
- •Присоединение воды (реакция Кучерова):
- •Реакции нуклеофильного присоединения.
- •Реакции окисления-восстановления.
- •Реакции полимеризации.
- •Реакции замещения.
- •Алкадиены (диеновые углеводороды)
- •Способы получения.
- •Дегидратация двухатомных спиртов:
- •Химические свойства.
- •Электронное строение бутадиена-1,3.
- •Реакции присоединения.
- •Гидрирование:
- •Галогенирование:
- •Гидрогалогенирование:
- •Реакции полимеризации.
- •Галогенпроизводные алифатического ряда.
- •Физические свойства.
- •Способы получения.
- •Электронное строение и химические свойства.
- •Реакции нуклеофильного замещения.
- •Реакции элиминирования.
- •Ароматические углеводороды (арены)
- •Изомерия.
- •Способы получения.
- •Переработка угля и нефти:
- •Электронное строение бензола.
- •Химические свойства.
- •Реакции присоединения.
- •Реакции окисления.
- •Реакции замещения.
- •Галогенирование:
- •Сульфирование:
- •Алкилирование (реакция Фриделя-Крафтса):
- •Ацилирование:
- •Правила ориентации заместителей.
- •Спирты (алкоголи)
- •Физические свойства.
- •Способы получения.
- •Гидратация алкенов:
- •2. Гидролиз галогенпроизводных:
- •3. Спиртовое брожение сахаров:
- •Электронное строение и химические свойства.
- •1. Кислотные и основные свойства.
- •Реакции с участием нуклеофильного центра.
- •Образование простых эфиров (межмолекулярная дегидратация):
- •Образование сложных эфиров:
- •Реакции с участием электрофильного центра.
- •Реакции с участием сн-кислотного центра (реакции элиминирования).
- •5. Реакции окисления.
- •4. Восстановление:
- •Классификация.
- •Способы получения.
- •Химические свойства.
- •1. Кислотные и основные свойства.
- •2. Реакции с участием нуклеофильного центра.
- •3. Реакции с участием электрофильного центра.
- •4. Реакции электрофильного замещения в ароматическом ядре.
- •5. Реакции окисления-восстановления.
- •Карбонильные соединения (альдегиды и кетоны).
- •Бутаналь бутанон-2 Физические свойства.
- •Способы получения.
- •Электронное строение и химические свойства.
- •Реакции присоединения.
- •Гидратация:
- •Присоединение спиртов:
- •Присоединение тиолов:
- •2. Реакции конденсации.
- •3. Реакции окисления.
- •1. Окисление кислородом воздуха:
- •2. Окисление аммиачным раствором оксида серебра (реакция «серебряного зеркала»):
- •4. Реакции полимеризации.
- •Карбоновые кислоты.
- •Предельные одноосновные карбоновые кислоты. Номенклатура.
- •Способы получения.
- •Электронное строение и химические свойства.
- •Кислотные свойства.
- •Реакции нуклеофильного замещения.
- •Реакция этерификации:
- •Образование ангидридов:
- •Образование галогенангидридов:
- •Образование амидов:
- •Реакции по углеродному атому.
- •Реакции декарбоксилирования.
- •Функциональные производные карбоновых кислот
- •Галогенангидриды.
- •Ангидриды.
- •Сложные эфиры.
- •Тиоэфиры.
- •Классификация.
- •Номенклатура.
- •Способы получения.
- •Восстановление нитросоединений:
- •Аммонолиз и аминолиз галогенпроизводных:
- •Химические свойства.
- •Основные свойства.
- •Кислотные свойства.
- •3. Нуклеофильные свойства.
- •Ацилирование аминов:
- •4. Реакции с азотистой кислотой.
- •1 . Первичные алифатические амины
- •2. Первичные ароматические амины:
- •3. Вторичные алифатические и ароматические амины:
- •Электрофильное замещение в ароматических аминах.
Сопряжение.
Ковалентная связь может быть локализованной и делокализованной. Локализованной называют связь, электроны которой поделены между двумя ядрами связываемых атомов. В тех случаях, когда электроны поделены более чем между двумя ядрами, говорят о делокализованной связи. Делокализованные связи практически всегда являются -связями. Они характерны для сопряженных систем – соединений, содержащих кратные связи, отделенные одной простой связью от соседнего атома, имеющего р-орбиталь.
Участвующие в сопряжении делокализованные р-орбитали могут принадлежать либо двум и более -связям, либо -связи и одному атому с р-орбиталью. В соответствии с этим различают ,-сопряжение и р,-сопряжение.
,-Сопряжение
Н2С=СНСН=СН2 Н2С=ССН=СН2 Н2С=СНСН=СНСН=СН2
СН3
Бутадиен-1,3 изопрен гексатриен-1,3,5
Н2С=СНСН Н2С=СНССН Н2С=СНСN
О
Акролеин бензол винилацетилен акрилонитрил
р,-Сопряжение
Н2С=СНОСН3 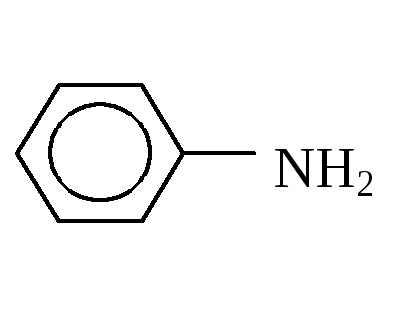 СН3С=О
СН3С=О
винилметиловый эфир анилин ацетат-ион Н
+
Н2С=СНСН2 Н2С=СНСН2 Н2С=СНСН2
Аллил-радикал аллил-катион аллил-анион
Простейшим представителем ,-сопряженных систем с углеродной цепью служит бутадиен-1,3, в молекуле которого все атомы углерода находятся в состоянии sp2-гибридизации. Было установлено, что все атомы углерода и водорода бутадиена-1,3 лежат в одной плоскости, следовательно, и все -связи лежат в одной плоскости, образуя плоский -скелет. Негибридизованные р-АО каждого атома углерода расположены перпендикулярно плоскости -скелета и параллельно друг другу., что является необходимым условием их перекрывания. Перекрывание происходит между р-АО С-1 и С-2, С-3 и С-4, а также между р-АО С-2 и С-3. В результате образуется единая -система, охватывающая все четыре атома углерода, т.е. возникает делокализованная ковалентная связь.
Это находит отражение в изменении длин связей в молекуле. Длина связи С-1 – С-2, а также С-3 – С-4, в бутадиене-1,3 увеличена (по сравнению с обычной двойной связью), а расстояние между С-2 и С-3 укорочено (по сравнению с обычной одинарной связью), т.е. процесс делокализации электронов приводит к выравниванию длин связей.
Система сопряжения может включать и гетероатомы: акролеин.
р,-Сопряжение осуществляется в том случае, когда орбитали двойных или тройных -связей перекрываются с р-орбиталью соседнего атома и образуется единая делокализованная система -электронов. Сопряжение осуществляется в молекулах, содержащих фрагмент С=СХ, где Х – гетероатом, имеющий свободную пару электронов на р-АО.
В аллил-анионе СН2=СНСН2 sp2-гибридизованный атом углерода С-3 поставляет в общую сопряженную систему два электрона, а аллильном радикале СН2=СНСН2 - один, а в аллильном карбокатионе СН2=СНСН2+ не поставляет ни одного. В результате при перекрывании р-АО трех sp2-гибридизованных атомов углерода образуется делокализованная трехцентровая связь, содержащая четыре (в карбанионе), три (в свободном радикале) и два (в карбокатионе) электрона соответственно.
5
