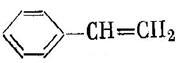МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное учреждение
«Российский химико – технологический университет
имени Д.И.Менделеева»
Расчетно – графическая работа на тему:
«Производство стирола методом дегидрирования этилбензола»
Выполнила:
студентка группы Н-46
Шелемей Алена Алексеевна
Проверил:
д.т.н., профессор Семенов Г.М.
Москва 2018
Содержание
РАЗДЕЛ I
1. Введение………………………………….………………..……...3
-
1.1 Физические свойства стирола…………………….……..…......3
-
1.2 Химические свойства стирола ………………………………...5
-
1.3 Физико-химические свойства стирола………………………...6
2. Сырье……………………………………………………………...7
3. Области использования стирола………………………………...9
4. Масштабы производства………………………………………...12
РАЗДЕЛ II
-
Химическая схема производства стирола ………………...…..13
-
Функциональная схема производства стирола………………..14
-
Индивидуальное задание……………………………………….17
Список литературы………………………………………………………..18
РАЗДЕЛ I
-
Введение
Стирол – бесцветная легко полимеризующаяся жидкость с характерным сладковатым запахом. Пары стирола способны вызывать раздражение слизистых оболочек глаз и дыхательных путей.

Рисунок 1. Структурная формула стирола
Был выделен в 1839 из стиракса (смола амбрового дерева) Симоном. Производство стирола началось в США после Второй мировой войны.
Существует несколько способов производства стирола:
-
Каталитическое дегидрирование этилбензола
-
Из этилбензола через его гидропероксид
-
Взаимодействие этилена со стильбеном
-
Экстрактивная ректификация из фракции пиролиза бензина в этилен
Основным методом производства является дегидрирование этилбензола с использованием катализатора. Таким образом получают 90% мирового производства стирола.
В данной РГР рассмотрена технологическая схема производства стирола каталитическим дегидрированием этилбензола, как наиболее распространенного способа его получения, описаны физико-химические параметры процесса.
-
Физические свойства
Стирол горюч и взрывоопасен. Представляет собой бесцветную жидкость. Пределы взрывоопасности в смеси с воздухом при комнатной температуре от 1,1 до 6,1 объемн. %. Допустимая концентрация паров в воздухе не выше 0,5 мг/м систематическое вдыхание паров стирола в концентрации выше допустимой приводит к хроническому заболеванию печени.
Важнейшие физические свойства стирола приведены ниже:
Таблица 1 – Физические свойства стирола
|
Структурная формула |
|
|
Т. кипения при 760 мм рт. ст., °C |
145,2 |
|
Градиент кипения, °C/мм рт. ст. |
0,049 |
|
Т. замерзания при 760 мм рт.ст., °C |
–30,628 |
|
Плотность при 20 °C, г/см3 |
0,90600 |
|
Дипольный момент, Кл×м |
0,37×10-30 |
|
Плотность при 20 оС |
906,0 кг/м3 |
|
Вязкость при 20 °C, Па×с |
0,078 |
|
Давление насыщенных паров при 20 оС |
4,9 мм. рт. ст. |
|
Теплота испарения при 20 °C, кДж/моль |
44,6 |
|
Температура плавления |
-30,63 оС |
|
Критическая температура, °C |
373 |
|
Критическое давление, МПа |
3,93 |
|
Коэффициент
преломления |
1,54682 |
|
Удельное объемное электрическое сопротивление |
10-11 Ом/м |