
1
.docxМИНОБРНАУКИ РОССИИ
Санкт-Петербургский государственный
электротехнический университет
«ЛЭТИ» им. В.И. Ульянова (Ленина)
Кафедра микро- и наноэлектроники
отчет
по лабораторной работе №1
по дисциплине «ФХОТ изделий электроники и наноэлектроники»
Тема: Моделирование диаграмм состояния полупроводниковых систем с неограниченной растворимостью компонентов в жидкой и твердой фазах
Студенты гр. 4209
__________________ Хабибулин А.Р.
|
|
|
Перякин И.В. |
|
Преподаватель |
|
Максимов А.И. |
Санкт-Петербург
2016
Цель работы.
Изучение фазовых равновесий в бинарных полупроводниковых системах с непрерывным твердым раствором методом компьютерного моделирования; расчет параметров межатомного взаимодействия; выбор моделей растворов, адекватно описывающих экспериментальную Т-х-проекцию диаграммы состояния.
Экспериментальные результаты и исходные данные:
Система: CdSe-ZnSe
Таблица 1. Координаты точек линий ликвидуса и солидуса для системы CdSe – ZnSe для построения Т-х проекции фазовой диаграммы состояния
|
T, К |
XlB, мол. доли |
XSB, мол. доли |
|
1573 |
0,26 |
0,38 |
|
1593 |
0,35 |
0,46 |
|
1613 |
0,43 |
0,55 |
|
1633 |
0,49 |
0,62 |
|
1653 |
0,56 |
0,68 |
|
1673 |
0,64 |
0,74 |
|
1693 |
0,68 |
0,78 |
|
1733 |
0,81 |
0,88 |
|
1753 |
0,86 |
0,91 |
|
1773 |
0,93 |
0,94 |
Температуры плавления:


Энтальпии плавления:


Рис.
1. Т-х проекция диаграммы состояния
системы CdSe-ZnSe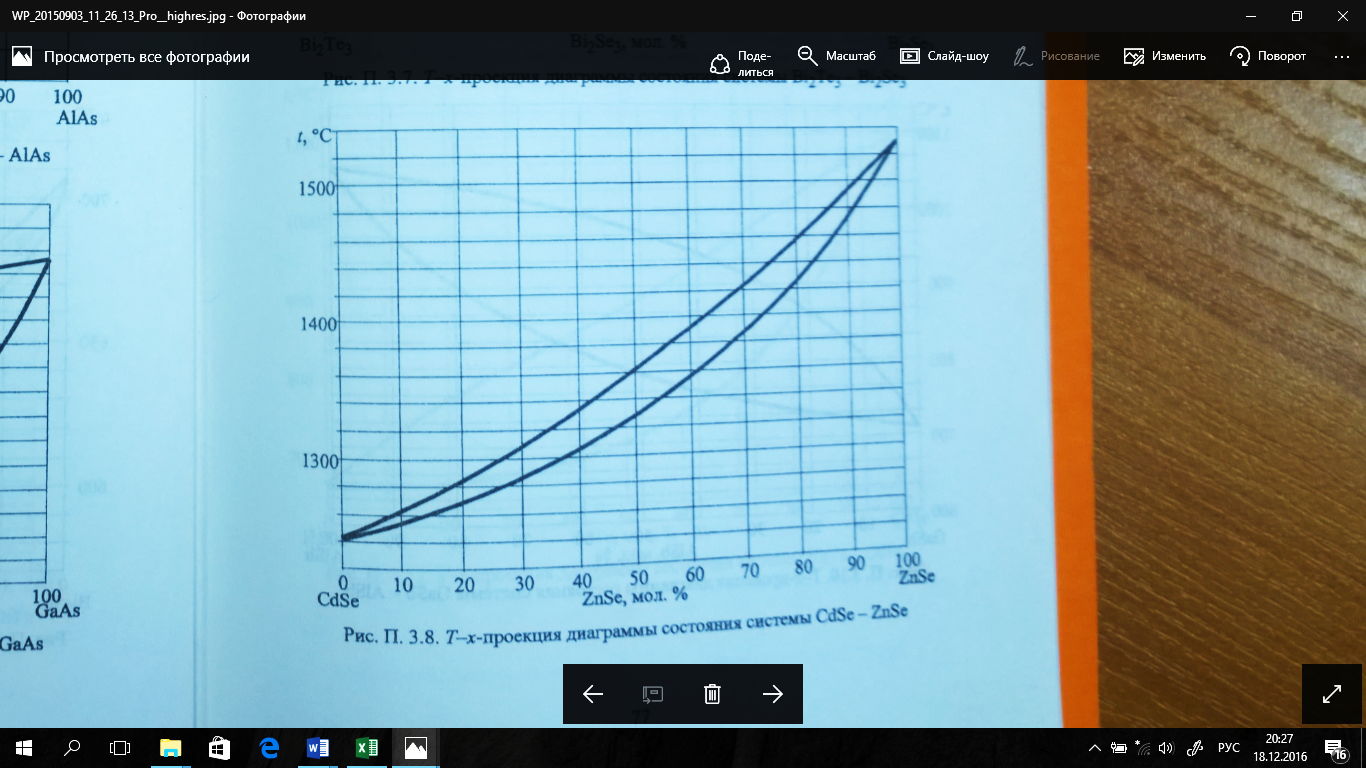
Обработка результатов эксперимента:
T, К
X, мол.
-
Приведем Т-х проекции диаграмм состояния (экспериментальной и теоретически рассчитанной), а также найденные значения параметров взаимодействия Wl opt и Ws opt:
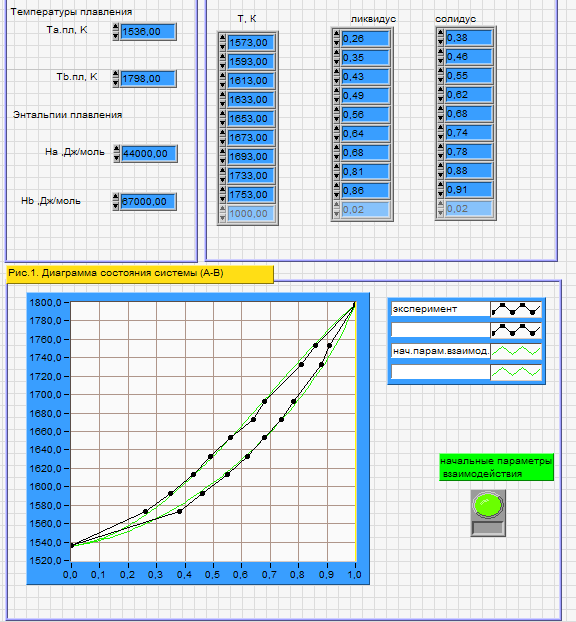
Рис. 2. Т-х проекция диаграммы состояния системы CdSe-ZnSe, построенная в среде LabView
T,
К X,
мол.
Рис. 3. Т-х проекция диаграммы состояния системы CdSe-ZnSe, при найденных параметрах взаимодействия
Таким
образом, найдены следующие оптимальные
параметры межатомного взаимодействия
в жидком (Wl)
и твердом (Ws)
растворах: 
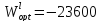

-
Приведем Т-х проекции диаграмм состояния, построенные в соответствии с п.11 методических указаний:
X, мол.
T,
К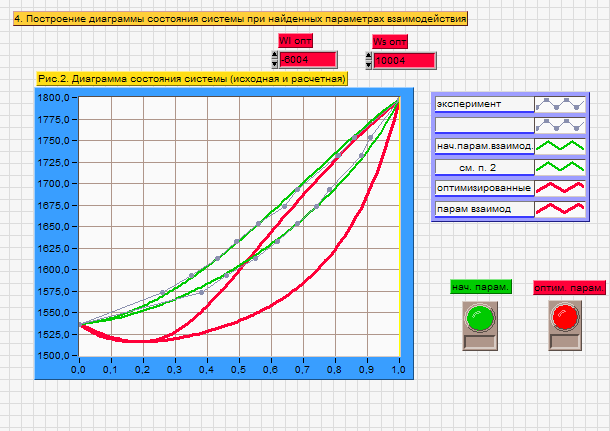
Рис.
4. Т-х проекция диаграммы состояния
системы CdSe-ZnSe,
при найденных параметрах взаимодействия,
отличающихся по знаку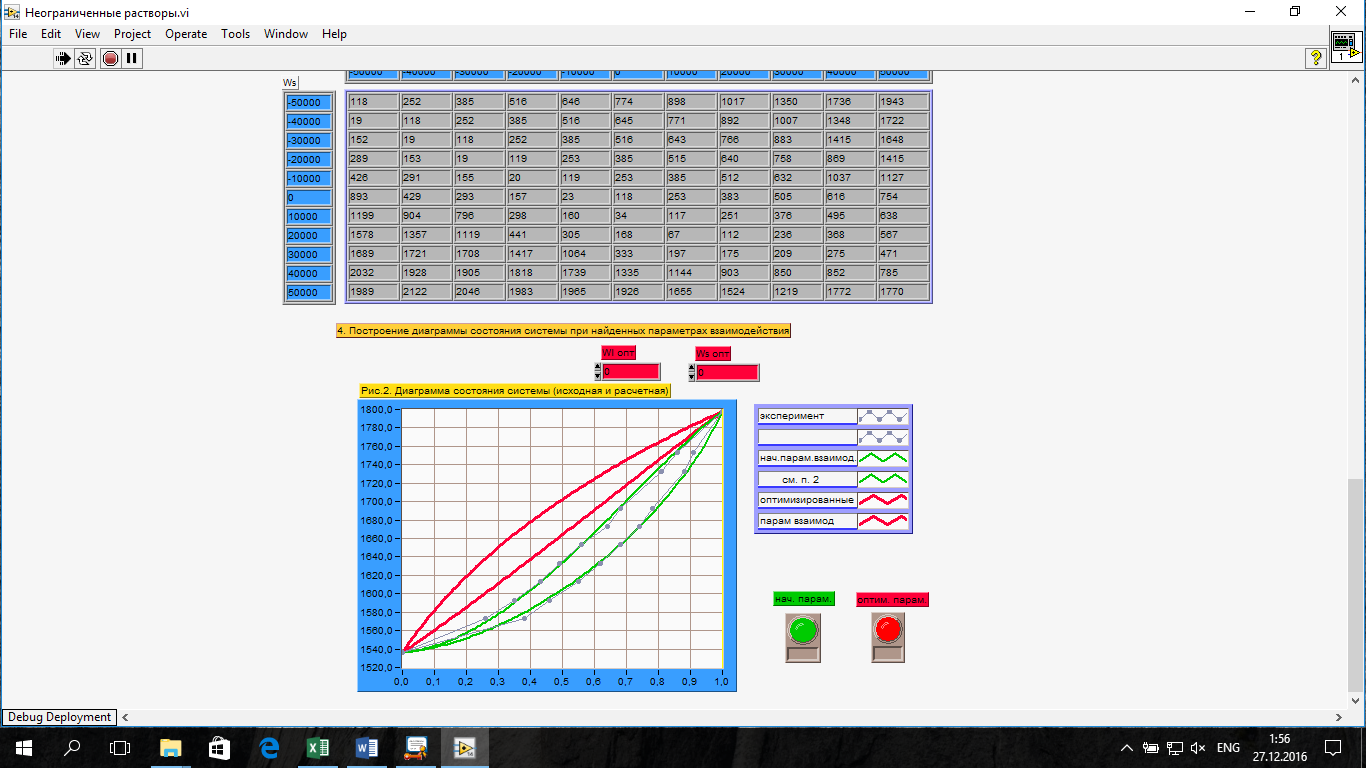
Рис. 5. Т-х проекция диаграммы состояния системы CdSe-ZnSe, при параметрах взаимодействия, равных нулю (модель идеального раствора)
-
Расчет и построение концентрационных зависимостей термодинамических функций смешения при T=const:
Энтальпия смешения:

Энтропия смешения:
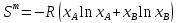
Свободная энергия смешения:

Для твердого раствора:
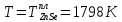
Таблица 2. Расчет энтальпии смешения для твердого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
Hm, Дж |
0 |
-1341,3 |
-2384,5 |
-3129,6 |
-3576,7 |
-3725,8 |
-3576,7 |
-3129,6 |
-2384,5 |
-1341,3 |
0 |
Таблица 3. Расчет энтропии смешения для твердого раствора
|
ХA |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
S, Дж/К |
0 |
2,70 |
4,16 |
5,08 |
5,59 |
5,76 |
5,59 |
5,08 |
4,16 |
2,70 |
0 |
|
XB |
1 |
0,9 |
0,8 |
0,7 |
0,6 |
0,5 |
0,4 |
0,3 |
0,2 |
0,1 |
0 |
Таблица 4. Расчет свободной энергии смешения для твердого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
Gm, Дж |
0 |
-6198,5 |
-9861,2 |
-12256,8 |
-13632,4 |
-14082,3 |
-13632,4 |
-12256,8 |
-9861,2 |
-6198,5 |
0 |
Для жидкого раствора:

Таблица 5. Расчет энтальпии смешения для жидкого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
Hm, Дж |
0 |
-2124 |
-3776 |
-4956 |
-5664 |
-5900 |
-5664 |
-4956 |
-3776 |
-2124 |
0 |
Таблица 6. Расчет свободной энергии смешения для жидкого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
G, Дж |
0 |
-6273 |
-10163 |
-12753 |
-14254 |
-14747 |
-14254 |
-12753 |
-10163 |
-6273 |
0 |

 Рис.
6. График зависимости энтальпии смешения
Hm(x)
Рис.
6. График зависимости энтальпии смешения
Hm(x)
Рис. 7. График зависимости энтропии смешения Sm(x)
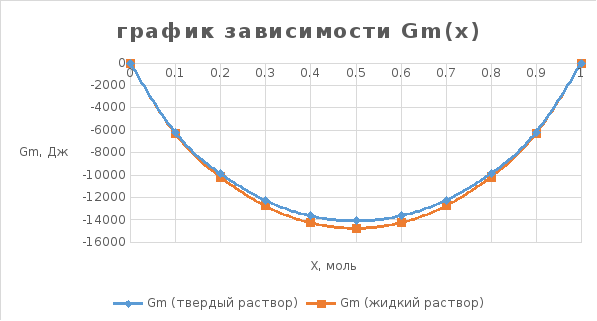
Рис. 8. График зависимости свободной энергии смешения Gm(x)
-
Расчет концентрационных зависимостей коэффициентов активностей и активностей компонентов:
Активность компонентов:


Коэффициент активности:
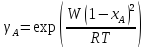

Для твердого раствора:
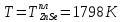
Таблица 7. Расчет активности компонента A твердого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
α A (тв. р-р) |
0 |
0,02 |
0,06 |
0,12 |
0,21 |
0,31 |
0,45 |
0,59 |
0,74 |
0,88 |
1 |
Таблица 8. Расчет активности компонента B твердого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
α B (тв. р-р) |
1 |
0,88 |
0,74 |
0,59 |
0,45 |
0,31 |
0,21 |
0,12 |
0,06 |
0,02 |
0 |
Таблица 9. Расчет коэффициента активности компонента А твердого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
ϒ A (тв. р-р) |
0 |
0,22 |
0,31 |
0,40 |
0,51 |
0,63 |
0,74 |
0,85 |
0,93 |
0,98 |
1 |
Таблица 10. Расчет коэффициента активности компонента B твердого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
ϒ B (тв. р-р) |
1 |
0,98 |
0,93 |
0,85 |
0,74 |
0,63 |
0,51 |
0,40 |
0,31 |
0,22 |
0 |

Рис. 9. График концентрационной зависимости активности компонентов твердого раствора
Для жидкого раствора:
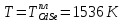
Таблица 11. Расчет активности компонента A жидкого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
α A (ж. р-р) |
0 |
0,04 |
0,11 |
0,18 |
0,28 |
0,39 |
0,51 |
0,64 |
0,77 |
0,89 |
1 |
Таблица 12. Расчет активности компонента B жидкого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
α B (ж. р-р) |
1 |
0,88 |
0,74 |
0,59 |
0,45 |
0,31 |
0,21 |
0,12 |
0,06 |
0,02 |
0 |
Таблица 13. Расчет коэффициента активности компонента А жидкого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
ϒ A (ж. р-р) |
0 |
0,45 |
0,53 |
0,61 |
0,70 |
0,78 |
0,85 |
0,91 |
0,96 |
0,99 |
1 |
Таблица 14. Расчет коэффициента активности компонента B жидкого раствора
|
Х |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
ϒ B (ж. р-р) |
1 |
0,98 |
0,93 |
0,85 |
0,74 |
0,63 |
0,51 |
0,40 |
0,31 |
0,22 |
0 |
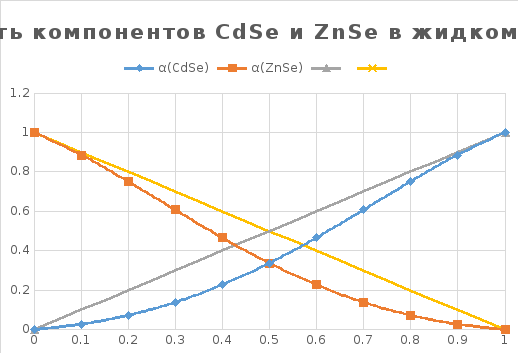
Рис. 10. График концентрационной зависимости активности компонентов жидкого раствора
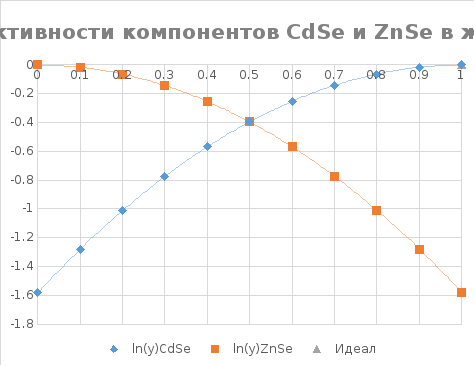
Рис. 11. График концентрационной зависимости коэффициента активности компонентов жидкого раствора
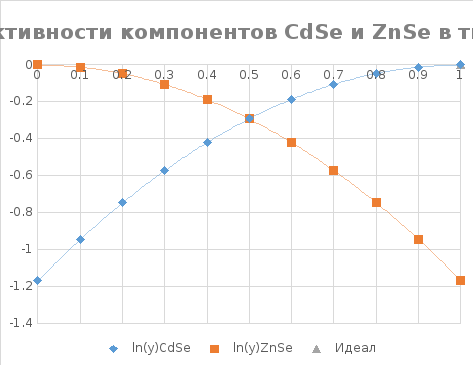
Рис. 12. График концентрационной зависимости коэффициента активности компонентов твердого раствора
Расчет мольной свободной энергии Гиббса:
|
X |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
|
GM |
-4311,2 |
-9738 |
-12781 |
-14525 |
-15179 |
-14826 |
-13486 |
-11138 |
-7701,5 |
-2965,13 |
4154,89 |

Рис. 13.
