
Общие вопросы / Хосева 2014 Диссертация
.pdf121
Заключение по главе 3
Таким образом, проведенный нами комплексный анализ показателей государственного контроля качества, эффективности и безопасности ЛС,
выпускаемых отечественными фармацевтическими предприятиями,
свидетельствует о высокой доле недоброкачественных (70%) и
фальсифицированных ЛС (20-30%); большом количестве рекламаций,
поступающих на ЛС отечественного производства, давно присутствующие на фармацевтическом рынке, доступные по стоимости и часто употребляемые населением (Мукалтин, Парацетамол, Анальгин, Корвалол, Аскорбиновая кислота
идр.).
Впоследние годы отмечается тенденция к снижению в 2,4 раза доли недоброкачественных ЛС отечественного производства по некритичным показателям (упаковка и маркировка). При этом в 1,4 раза увеличилась доля недоброкачественных ЛС по критичным показателям (описание,
микробиологическая чистота, количественное определение, цветность,
распадаемость и др.).
Среди забракованной продукции отечественного производства в последние годы отмечается двукратное (1,9 раза) увеличение доли выявленных
недоброкачественных твердых ЛФ |
и уменьшение (в 1,3 раза) |
недоброкачественных жидких ЛФ. |
|
Проблемы качества ЛС отечественного производства, в большей степени,
обусловлены отсутствием стандартов надлежащей производственной практики
(GMP).
Контрольно-надзорные мероприятия, проводимые Росздравнадзором в отношении ряда отечественных производителей, позволили снизить в последние годы долю забракованной продукции от 2 до 6 раз по количеству торговых наименований и в 4-8 раз по количеству серий.
Впоследние 5 лет отмечается увеличение общего числа спонтанных сообщений,
поступающих в базу данных АИС-Росздравнадзора в 2,9 раза (65%). В указанный
122
период времени число СС от учреждений практического здравоохранения,
территориальных управлений Росздравнадзора и региональных центров мониторинга безопасности возросло в 1,3 раза (23%), от фармацевтических компаний - в 2,9 раза (65%). Количество ПОБЛС, поступающих от фармацевтических производителей в базу данных Росздравнадзора увеличилось в
7,0 раз (86%), вместе с тем общее число ПОБЛС составляет лишь 30% от общего числа торговых наименований ЛС, зарегистрированных на территории РФ.
В течение 2009-2013 гг наибольшее число СС поступало на антибактериальные препараты цефалоспоринового, пенициллинового ряда и фторхинолоны,
пиразинамид, а так же антибиотики для системного введения (более 30%) и
сердечно-сосудистые препараты (16%).
Случаи отсутствия терапевтической эффективности ЛС регистрировались в среднем в 9% в 2011-2013 гг.
Мониторинг качества проводимых в России клинических исследований по изучению эффективности и безопасности ЛС отечественного производства в рамках регуляторных процедур показал, что число исследований с нарушением правил Надлежащей клинической практики (GCP) за последние 4 года остается высоким и составляет в среднем 60% от числа КИ, подвергшихся проверкам со стороны регуляторных органов.
Нарушения в деятельности ЛЭК при ЛПУ, являющихся клиническими базами исследований отечественных препаратов в ходе проверок составляют в среднем
49%.
123
ГЛАВА 4. ОЦЕНКА ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ ВОСПРОИЗВЕДЕННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ ОТЕЧЕСТВЕННОГО ПРОИЗВОДСТВА В ПОСТМАРКЕТИНГОВЫХ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ
4.1. Этические и организационные аспекты проведения постмаркетинговых клинических исследований воспроизведенных лекарственных средств отечественного производства
В настоящее время в портфеле отечественного фармацевтического производителя ОАО «Акрихин», согласно перечню препаратов, опубликованному на сайте компании www.akrikhin.ru (по состоянию на 25.11.2013 г.) [59],
присутствует 143 торговых наименования ЛС (с учетом всех лекарственных форм и дозировок), БАД к пище и средств косметического ухода за кожей
[Приложение 1].
Среди этого числа на долю препаратов отечественного производства непосредственно самого предприятия ОАО «Химико-фармацевтический комбинат «Акрихин» приходится 103 (72%) наименования, на долю препаратов и продуктов зарубежного производства (стратегических партнеров - Польфарма АО, Медана Фарма АО, Непентес и др.) приходится 40 (28%) торговых наименований ЛС; 55% препаратов из всего продуктового портфеля компании приходится на ЛС, входящие в Перечень ЖНВЛП [139].
В период с 1997 г. по 2012 г. из 146 торговых наименований в активной промоции находилось чуть больше половины портфеля препаратов - 79 (54,1%)
ТН, в 2013 г. на продвижении, с точки зрения маркетинговой политики, было оставлено менее половины продуктов - 59 (40,4%) ТН. За этот период времени 3
торговых наименования ЛС были выведены из портфеля компании/сняты с производства, что связано с маркетинговой политикой.
В клинических и фармакоэпидемиологических исследованиях эффективность и безопасность изучалась только у 68 (46,6%) торговых наименований в различных лекарственных формах и дозировках (рис. 4.1.1.).
124
146 |
68 |
|
46,6% |
|
|
ТН в портфеле |
|
|
|
||||
|
|
|
||||
|
|
|
|
|||
|
|
|
|
ТН изучались в КИ |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 4.1.1. Доля торговых наименований продуктов из портфеля ОАО «Акрихин», изучавшихся в исследованиях (1997-2012 гг.).
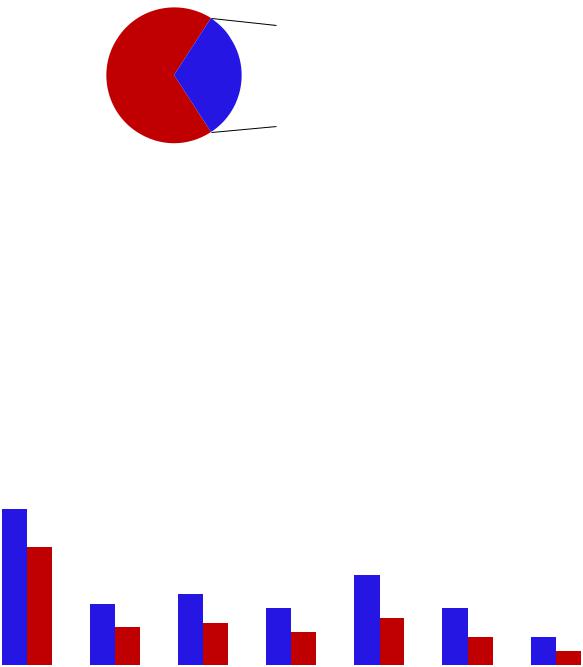
Применительно к клинико-терапевтическим группам, из имеющихся в портфеле торговых наименований ЛС, изучались в постмаркетинговых исследованиях (ПмИс) 75,8% препаратов из группы дерматология; 61,5% - из группы гинекология; 60% - из группы противотуберкулезных препаратов; 58,3% -
из группы эндокринология; 52,6% - из группы кардиология и по 50% - из групп неврология и педиатрия (рис. 4.1.2.).
75,8%
19
25
|
|
61,5% |
60,0% |
|
|
|
|
52,6% |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
58,3% |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
12 |
19 |
|
|
12 |
50,0% |
|
|
|
|
||||||||||
|
|
13 |
|
|
|
|
|
|
|
||||||||||||
|
|
|
15 |
|
|
|
|
|
|
|
|
|
6 |
|
|
50,0% |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|||
|
|
8 |
|
9 |
|
|
7 |
|
|
|
6 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Дерматол. |
|
Гинекол. |
|
|
Туберкул. Эндокринол. |
|
Кардиол. |
Неврол. |
|
Педиатр. |
||||||||||
|
|
|
|
|
ТН в портфеле |
|
ТН изучались в КИ |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Рис. 4.1.2.Соотношение имеющихся в портфеле и изучавшихся в КИ торговых наименований препаратов из различных клинико-терапевтических групп (абс.
чис., %)
На первом этапе ретроспективного анализа, включенные в обработку материалы результатов исследований, были распределены нами в зависимости от клинико-терапевтических групп (КТГ) и торговых наименований (ТН) ЛС, были
125
проанализированы фазы, дизайн, временной период исследований и исследовательские центры [Приложение 2].
Основными клиническими базами, в которых были выполнены исследования,
являлись ведущие научные, учебные и лечебные учреждения РФ (рис. 4.1.3.).
4 |
|
|
|
87 |
||
4 4 |
|
|
|
|||
4 4 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
6 |
|
|
|
|
|
|
6 |
|
|
|
18 |
||
6 |
|
|
|
|||
|
|
|
|
|
||
7 |
|
|
|
|
|
|
|
|
11 |
16 |
|
|
|
|
Первый МГМУ |
|
РГМУ |
|
РМАПО |
|
|
|
|
|
|||
|
|
|
|
|||
|
ВолгГМУ |
|
МГМСУ |
|
|
Красноярская ГМА |
|
|
|
|
|||
|
|
|
|
|||
|
НЦАГиП им. И.В.Кулакова |
|
ФЦСКЭ им. В.А.Алмазова |
|
Новосибирская ГМА |
|
|
|
|
||||
|
|
|
||||
|
Башкирский ГМУ |
|
Нижегородский КВД |
|
ГНЦ ЛС |
|
|
|
|
||||
|
|
|
||||
|
ГНИЦ ПМ |
|
ВНЦ БАВ |
|
|
Первый СПб им. Павлова |
|
|
|
|
|||
|
|
|
|
|||
|
Томский ГУНИИ кардиологии |
|
Другие |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
||
Рис. 4.1.3. Ведущие исследовательские центры и количество выполненных в них исследований (1997 - 2013 гг), n=197 (абс.чис.)
Среди материалов, подвергнутых ретроспективному анализу, было 11 отчетов
(5,6%) с результатами доклинических исследований;10 (5,1%) отчетов с результатами исследований биоэквивалентности (БЭ); 171 (86,8%) -
постмаркетинговых КИ;5 (2,5%) - фармакоэпидемиологических исследований
(ФЭИ).
Из общего числа постмаркетинговых клинических исследований только 18 (10,5%) КИ по направлениям кардиология, эндокринология и фтизиатрия,
проведенные преимущественно в период после 2007 г., имели указания на одобрение локальным этическим комитетом, во всех остальных данная информация отсутствовала.
Относительно качества отчетов проводимых в России локальных исследований,
литературные данные согласуются с результатами нашего анализа [1,164]. Среди отчетов, отобранных нами для ретроспективного анализа, были такие, в которых
126
отсутствовала или была некорректной информация о критериях включения/исключения пациентов; промежуточных и конечных точках; описание дизайна исследования; методов рандомизации; методов статистического анализа;
сведения о распределении пациентов по полу и возрасту; данные о продолжительности активного лечения и наблюдения пациентов в исследовании;
о терапии в группах сравнения; информация по выявленным в ходе исследования НПР, их описание, критерии серьезности, мероприятия по купированию; ошибки в расчетах, отсутствие указаний на достоверность полученных результатов.
По дизайну среди ПмИс (n=176) большую часть составляли несравнительные,
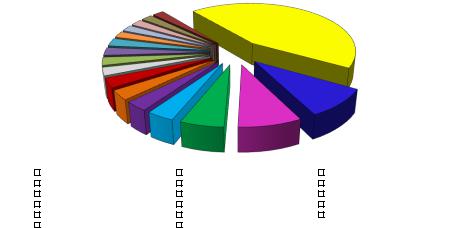
открытые, проспективные КИ - 111 (63,1%); сравнительных, рандомизированных КИ было проведено 60 (34,1%); ФЭИ - 5 (2,8%)(рис.4.1.4.).
2,8 %
34,1 %
многоцентровое - 9,1 %
терапевтическая эквивалентность - 1,7 %
слепое - 1,7 %
перекрестное - 1,7 %
63,1 %
плацебо - 0,6 %
|
несравнительное |
|
сравнительное |
|
фармакоэпидемиологическое |
|
|
|
|||
|
|
|
Рис. 4.1.4. Распределение постмаркетинговых исследований ЛС по дизайну, n =
176 (доля, %)
Из их общего числа на долю многоцентровых КИ приходилось 9,1% (16 КИ);
изучение терапевтической эквивалентности (ТЭ) - 1,7% (3 КИ); слепых -1,7 % (3
КИ); перекрестных - 1,7 % (3 КИ), плацебо-контролируемых - 0,6% (1 КИ).
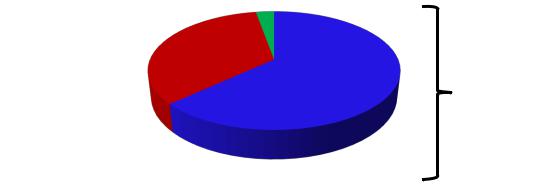
Согласно нашим данным, наиболее часто изучалась в ПмИс эффективность и безопасность препаратов, применяемых в кардиологии - 31,3% (55 исследований),
дерматологии/аллергологии - 25,0% (44), гинекологии - 15,9% (28); значительно
127
реже - применяемых в эндокринологии - 9,1% (16), педиатрии - 7,4% (13);
неврологии - 5,7% (10), фтизиатрии - 5,7% (10) (рис. 4.1.5.).
5,7% |
|
|
|
Кардиология |
7,4% |
31,3% |
|
|
|
|
|
|||
|
|
|
||
|
|
|
|
|
|
|
|
|
Эндокринология |
|
|
|
|
|
|
|
|
|
|
25% |
|
|
|
Неврология |
|
|
|
||
|
|
|
||
|
|
|
Гинекология |
|
|
|
|
|
|
|
|
|
|
|
|
|
9,1% |
|
Дерматология/Аллергология |
|
|
|
||
|
|
|
||
|
5,7% |
|
Педиатрия |
|
|
|
|||
|
|
|
||
15,9% |
|
|
Туберкулез |
|
|
|
|||
|
|
Рис. 4.1.5. Распределение постмаркетинговых исследований по клинико-
терапевтическим группам, n = 176 (доля, %)
В таблице 4.1.1. приведены консолидированные данные по видам и дизайну анализируемых исследований в соответствии с клинико-терапевтическими группами ЛС.
Таблица 4.1.1.
Распределение исследований по КТГ, видам и дизайну
КТГ
Вид исследования
Доклиническое
БЭ
Несравнительное
Сравнительное
ФЭИ
Многоцентровое
ТЭ
Слепое
Плацебоконтрол.
Прекрестное
Кардиология (ТН=10/Ис=63)
3
5
31
21
3
6
3
2
0
3

 Эндокриноло-
Эндокриноло-
гия |
(ТН=6/Ис=20) |
Неврология |
(ТН=6/Ис=12) |
Гинекология |
(ТН=5/Ис=28) |
Дерматология/ |
Аллергология |
(ТН=10/Ис=51) |
Педиатрия |
(ТН=3/Ис=13) |
Фтизиатрия |
(ТН=5/Ис=10) |
ИТОГО |
(ТН=45,Ис=197) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
0 |
0 |
7 |
|
0 |
0 |
11 |
||||||
3 |
|
2 |
0 |
0 |
|
0 |
0 |
10 |
||||||
7 |
|
5 |
22 |
37 |
9 |
0 |
111 |
|||||||
9 |
|
5 |
6 |
7 |
|
3 |
9 |
60 |
||||||
0 |
|
0 |
0 |
0 |
|
1 |
1 |
5 |
||||||
0 |
|
1 |
6 |
2 |
|
1 |
0 |
16 |
||||||
0 |
|
0 |
0 |
0 |
|
0 |
0 |
3 |
||||||
0 |
|
0 |
0 |
1 |
|
0 |
0 |
3 |
||||||
0 |
|
0 |
0 |
1 |
|
0 |
0 |
1 |
||||||
0 |
|
0 |
0 |
0 |
|
0 |
0 |
3 |
||||||
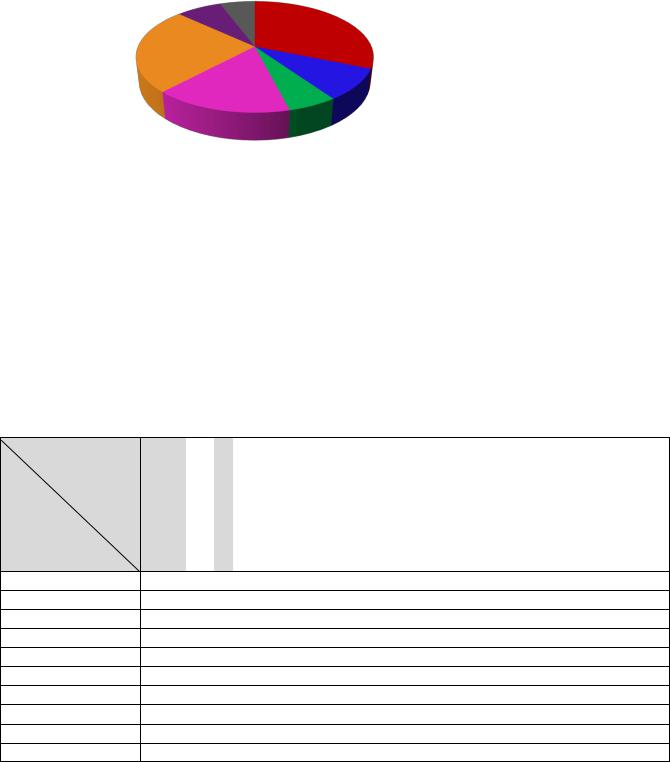
Как видно из таблицы, среди анализируемых исследований, наиболее часто несравнительные проводились при изучении препаратов, применяемых в

128
дерматологии/аллергологии - 37(33,3%), кардиологии - 31 (27,9%) и гинекологии
- 22 (19,8%); значительно реже в педиатрии - 9 (8,1%), эндокринологии - 7 (6,3%),
неврологии - 5 (4,5%) (рис. 4.1.6.).
|
8,1% |
0 |
|
|
|
|
|
|
|
|
|
27,9% |
|
|
33,3% |
|
|
|
Кардиология |
|
|
|
||
|
|
|
||
|
|
|
|
|
|
|
|
|
Эндокринология |
|
|
|
|
|
|
|
|
|
|
|
|
6,3% |
|
Неврология |
|
|
|
||
|
|
|
||
|
|
|
Гинекология |
|
|
|
|
|
|
|
|
|
|
|
|
|
4,5% |
|
Дерматология/Аллергология |
|
|
|
||
|
|
|
||
|
|
|
Педиатрия |
|
|
|
19,8% |
|
|
|
|
|
||
|
|
|
|
Рис. 4.1.6. Распределение несравнительных КИ по клинико-терапевтическим группам, n = 111 (доля, %)
По данным нашего анализа, среди всех исследований, сравнительные по дизайну преобладали в кардиологии - 21 (35,0%), реже в эндокринологии - 9 (15,0%), фтизиатрии - 9 (15,0%), дерматологии/аллергологии - 7 (11,7%),
гинекологии - 6(10,0%), неврологии - 5 (8,3%), педиатрии - 3 (5,0%) (рис. 4.1.7.).
|
15,0% |
|
|
|
5,0% |
|
35,0% |
|
Кардиология |
|
|
|||
|
|
|||
|
|
|
|
Эндокринология |
|
|
|
|
|
|
|
|
|
|
11,7% |
|
|
|
Неврология |
|
|
|
||
|
|
|
||
|
|
|
|
|
|
|
|
|
Гинекология |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дерматология/Аллергология |
|
|
|
|
|
|
|
|
|
|
10,0% |
|
|
|
Педиатрия |
|
|
|
||
|
|
|
||
|
8,3% |
15,0% |
|
Туберкулез |
|
|
|||
|
|
|||
|
|
|
|
Рис. 4.1.7.Распределение сравнительных КИ по клинико-терапевтическим группам, n = 60 (доля, %)
Фармакоэпидемиологических исследований было только 3 в группе
«Кардиология» и по 1 - в группах «Педиатрия» и «Фтизиатрия».
129
Многоцентровых КИ было выполнено по 6 в «Кардиологии» и «Гинекологии»,
2 - в «Дерматологии/Аллергологии» и по 1 - в «Неврологии» и «Педиатрии»; 3
исследования имели перекрестный дизайн («Кардиология»); 2 были ослеплены
(«Кардиология», «Дерматология/Аллергология»).
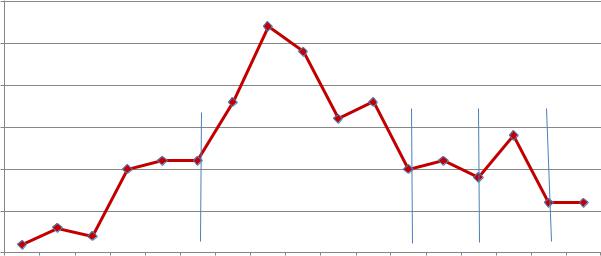
Детальный анализ архивных материалов позволил нам проследить годовую динамику числа проводимых исследований (рис. 4.1.8.).
30 |
|
|
|
27 |
|
|
|
|
|
|
|
|
|
|
|
25 |
|
|
|
|
24 |
|
|
20 |
|
|
|
18 |
18 |
|
|
|
|
|
|
|
|
||
|
|
|
|
16 |
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
14 |
|
|
|
|
|
|
|
|
|
|
|
11 |
11 |
|
10 |
11 |
|
|
|
10 |
|
|
9 |
|
|
10 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
6 |
5 |
|
3 |
|
|
|
|
|
|
1 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
1997г 1998г 1999г 2000г 2001г 2002г |
2003г 2004г 2005г 2006г 2007г 2008г 2009г 2010г 2011г 2012г 2013г |
|||||
Рис. 4.1.8.Годовая динамика |
количества |
проводимых |
исследований |
ОАО |
|||
«Акрихин» (n = 197) |
|
|
|
|
|
||
На представленном графике отчетливо прослеживаются два временных интервала планомерного увеличения и снижения числа проводимых исследований: 2002 - 2008 гг с пиком, приходящимся на 2004 г., когда число КИ достигло своего максимума - 27 (13,7% от общего числа всех Ис за 16 лет) и 2010
- 2012 гг с пиком увеличения проводимых исследований в 2011 г. до 14 (7,1%).
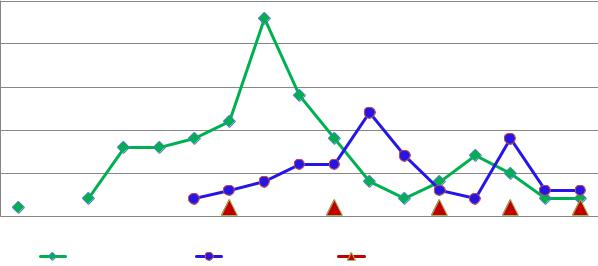
На рисунке 4.1.9. представлена динамика количества ежегодно проводимых сравнительных, несравнительных и фармакоэпидемиологических исследований.
|
|
|
|
130 |
|
|
|
|
|
|
|
25 |
|
|
|
23 (85,2%) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
14 |
12 |
(75,0%) |
|
|
|
|
|
|
|
|
|
11 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
8 |
9 |
|
9 |
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
8 |
|
6 |
6 |
7 |
|
|
7 |
|
|
|
|
|
|
|
4 |
|
5 |
|
|
||
5 |
|
|
|
4 |
4 |
|
|
|
|
||
|
|
|
|
|
|
3 |
3 |
||||
|
|
2 |
3 |
|
|
3 |
|
|
|||
|
1 |
2 |
|
2 |
|
2 |
|||||
|
|
|
|
|
|
2 |
|||||
|
|
|
|
|
|
|
|
|
|
||
0 |
|
|
|
1 |
1 |
|
|
1 |
1 |
2 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1997г 1998г 1999г 2000г 2001г 2002г 2003г 2004г 2005г 2006г 2007г 2008г 2009г 2010г 2011г 2012г 2013г |
||||||||||
|
|
несравнительное |
|
сравнительное |
фармакоэпидемиологическое |
|
|
||||
Рис. 4.1.9. Годовая динамика количества проводимых КИ, распределенных по |
|||||||||||
дизайну (n = 176) |
|
|
|
|
|
|
|
|
|
||
На графике видно, что с 2002 по 2006 гг проводились преимущественно несравнительные КИ, с максимальным увеличением в 2004 г до 23 (85,2% от общего числа исследований, проведенных в данном году) и постепенным спадом к 2008 г до 2 (18,2% от общего числа исследований, проведенных в данном году).
В этот же период времени заметна волна роста сравнительных по дизайну КИ в
4,5 раза от исходного (2002 г. - 2 Ис, 2006 г. - 6 Ис). В 2007 г. было проведено самое большое число сравнительных исследований (12), что составило 75,0% от общего числа Ис этого года. В последние 3 года сравнительные КИ проводились почти в 2 раза чаще, чем все остальные (2011 г. - 9 сравнительных и 5
несравнительных; 2012 г. - 3 сравнительных и 2 несравнительных; 2013 г - 3
сравнительных и 2 несравнительных).
ФЭИ начали впервые проводиться с 2003 г, в последние годы отмечается тенденция к более частому проведению исследований такого рода.
На рисунке 4.1.10. представлена годовая динамика проводимых исследований в зависимости от производителя (отечественный / зарубежный).
