
Адсорбционная спектроскопия пигментов растений
.docxФедеральное государственное автономное
образовательное учреждение
высшего профессионального образования
«СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ»
Институт фундаментальной биологии и биотехнологии
институт
кафедра
Отчёт по лабораторной работе
“Адсорбционная спектроскопия пигментов растений”
____________________________________________________
____________________________________________________
Преподаватель:
Студент:
Красноярск 2019
Цель работы: Освоение метода адсорбционной спектроскопии при помощи спектрофотометра Genesis 105.
Теоретическая часть:
Электронные состояния принята обозначать как σ, П, n, П*, σ*. В соответствии с этим электронные переходы обозначаются: σ > σ*, П > П* и тд. Кроме того, σ, П, n, П*, σ*, могут отличаться по спиновой мультипл. M: M*2|S|+1, где S-суммарное спиновое квантовое число.
Состояния с мультипл. 1 называют синм. и обозначают S. Возрастание цифрового индекса соответствует увеличению энергии состояния.
Правила отбора. Переходы не могут происходить м.у любыми уровнями энергии в молекуле. Переходы, удовлетворяющие правилам – разрешённые, неудовл. – запрещённые. Запрещённые делятся на: запрещённые по спину, запрещённые по симметрии.
Количественные меры интенсивности перехода – дипольный момент перехода: μij= ∫ ψi*μ*ψj*dτ μij= μijx+ μijy+ μijz
где, ψi и ψj – волновые функции i-го и j-го состояний, а μ – вектор дипольного момента, dτ – элемент обьёма, μijx, μijy, μijz – проекции вектора μij на координатные оси.
При переходе молекулы из основного состояния в возбужденное происходит перераспределения зарядов, связанное с поглощением света.
Поглощение электромагнитного излучения – свойство всей системы связей молекулы. Влияние растворителей на эл. спектр оценивает понятия: батохормный сдвиг, гипсохромный сдвиг, гипо и гиперхромия.
Энергия возбуждения электронов различных типов соответствует характерной области поглощения.
Помимо взаимодействия с растворителем изменения в спектре могут быть вызваны взаимодействиями растворенных молекул.
Законы ослабления излучения. Поглощение и рассеивание излучения происходит селективно. Количественные характеристики определяют при монохроматическом облучении. Лучистый поток Ф заменяется спектральной интенсивностью в формулах: I=Dф/dλ.
Уменьшение интенсивности света при его прохождении через тонкий слой: -dIx~Ix*dx=K*Ix*dx,
где k-постоянная, зависит от природы поглощающего вещества.
После преобразования получим: dIx/Ix=-kdx; lnIx=-kx+c, где C-постоянная интегрирования.
Уравнение Бугера-Бера: -lgT=D, где T (T=I/Io) – пропускание.
Ход работы:
1) Регистрация спекторв поглощения пигментов. Берём лист растения, делим на 3 части. Из одной части готовим водный гомогенат, из другой – ацентоновый экстракт.
Проводим регистрацию спектров поглощения пигментов в образцах:
- В целом листе (кусок листа) - В водной гомогенате (2 мл.) - В ацетановой экстракте (2мл.) Условия регистрации: диапозон скапирования = 400-750нм, шаг сканирования = 2 нм/с. 2) Проверка закона Бугера-Ламберта-Бера. Измеряем спектры люминисценции пигментов в ацетоновом экстракте разведённом в 2/4/8/16/32 раза.
3) Вычисление концентрации хлорофиллов а и б. Выбираем из отснятых ранее спектров тот, у которого Dmax<1. Используем его для вычисления концентрации хл. а и б. Исходя из значений рассчитывается концентрации для остальных экстрактов. С хл.а. = 11.63*0.32-2.39*0.195 = 3.27 мкг/л С хл.б. = 26.11*0.195-5.18*0.32 = 2.27 мкг/л
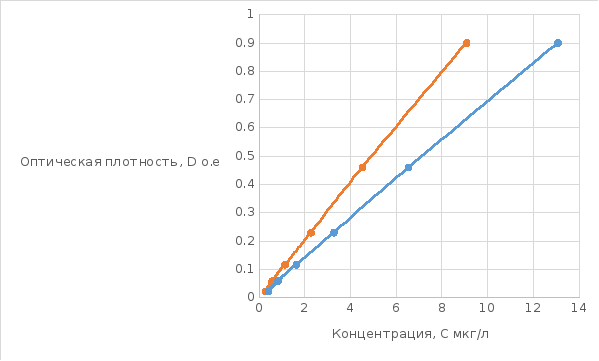
Таблица 1: Зависимость оптической плотности от концентрации.
(λ= 662 нм )
|
D, о.е |
С хл.а, мкл/л |
C хл.б. мкл/л |
|
1,291 |
13,08 |
9,08 |
|
0,702 |
6,54 |
4,52 |
|
0,361 |
3,27 |
2,27 |
|
0,182 |
1,635 |
1,135 |
|
0,122 |
0,8175 |
0,5675 |
|
0,065 |
0,40875 |
0,28375 |
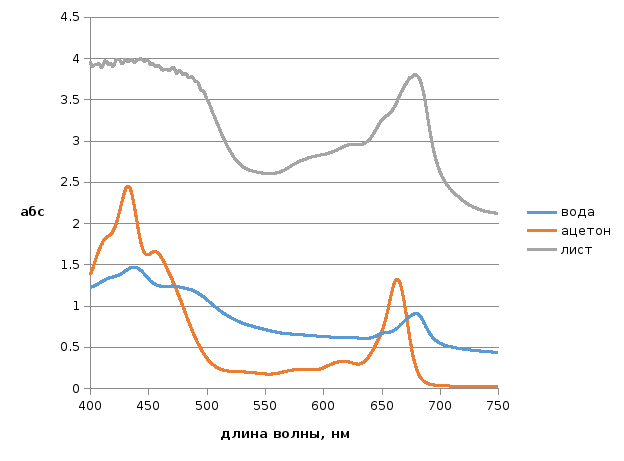

Вывод: В эксперименте наблюдались спектры следующищих длинны волныпигментов: хл.а на длинне волны 670 нм. , хл.б = 650 нм.
Форма спектров поглощения вещества зависит от типа вещества и его состояния. Сдвиг спектров в воде и ацетоне обьясняется тем, что в ацетоне электроны находятся в более возбёжденном состоянии.
Наблюдается соблюдение закона Бугера-Ламберта-Бэра с паданием пропорционально падает оптической плотности вещества.
