
3 КУРС / Разобранные билеты на экзамен по биологии микроорганизмов
.pdf
1.Фосфорилирование глюкозы •Фермент – гексокиназа
2.Изомеризация глюкозо-6-фосфата •Фермент – глюкозофосфатизомераза
3.Фосфорилирование фруктозо-6-фосфата •Фермент – фосфофруктокиназа
4.Фруктозо-1,6- дифосфат разрывается на две триозы •Фермент – фруктозо1,6- дифосфатальдолаза
5.Изомеризация фосфодиоксиацетона •Фермент – триозофосфатизомераза
6.Окисление глицеральдегид-3- фосфата •Фермент – дегидрогеназа
7.Первое субстратное фосфорилирование •Фермент – фосфоглицераткиназа
8.Перенос фосфатной группы •Фермент – фосфоглицератмутаза
9.Дегидратация 2-фосфоглицерата •Фермент – енолаза
10.Второе субстратное фосфорилирование •Фермент – пируваткиназа
Итого: 1глюкоза + 2НАД+ + 2АДФ + 2Фн → → 2 пируват + 2 НАД-Н2 + 2АТФ + 2Н2О
18. Пути превращения гексоз: окислительный пентозофосфатный путь.
Использование пентоз как субстрата Синтез нуклеиновых кислот и пентозосодержащих коферментов
1. Дегидрирование глюкозо-6-фосфата •Фермент – глюкозо-6- фосфатдегидрогеназа
•Кофермент – НАДФ+ 2. 6-фосфоглюконат дегидрируется и декарбоксилируется •Фермент – фосфоглюконат-
дегидрогеназа
3.Взаимопревращения пентозофосфатов •Ферменты – изомераза и эпимераза
4.Транскетолазная реакция

5. Трансальдолазная реакция
6. Транскетолазная реакция
Итог: 6 Глюкозо-6-фосфат + 7Н2О + 12 NADP+ =) 5 Глюкозо-6-фосфат + 6СО2 + Рi + 12 NADPH + 12Н+
19. Пути превращения гексоз: путь Энтнера-Дудорова.
Используется в том случае, когда необходимо получить пировиноградную кислоту более коротким путем. Первые стадии аналогичны ПФП:
Дегидрирование глюкозо-6-фосфата(глюкоза-6-фосфат превращается в 6- фосфоглюконовую кислоту) •Фермент – глюкозо-6- фосфатдегидрогеназа •Кофермент – НАДФ+ Следующие реакции специфичны для пути Энтнера-Дудорова:
1) Дегидратирование 6- фосфоглюконовой кислоты, приводящее к образованию КДФГ кислоты Фермент: 6-фосфоглюконатдегидратаза
2) Расщепление продукта первой реакции на два C3-фрагмента. Фермент: КДФГальдолаза

3-ФГА окисляется в пировиноградную кислоту так же, как в гликолитическом пути.
Итого: Глюкоза → пируват + АТФ + НАД-H2 + НАДФ-H2
20. Гомоферментативное молочнокислое брожение: химизм, энергетический выход, характеристика возбудителей.
Брожение – это способ получения энергии, при котором АТФ образуется в процессе анаэробного окисления органических субстратов в реакциях субстратного фосфорилирования.
Характеризуется сопряженным окислительновосстановительным превращением органических соединений в анаэробных условиях.
Сахара сбраживаются через гликолиз, и около 90% конечного продукта приходится на молочную кислоту.Субстраты: лактоза, ди и трисахариды, орган.кислоты.
1) Пируват превращается в лактат под действием лактадегидрогеназы и НАД+Н+
Суммарная реакция гомоферментативного брожения: глюкоза + 2ФН + 2АДФ → 2 лактат + 2АТФ + 2H2O (фермент лактатдегидрогеназа)
Осуществляют представители: Enterococcus faecalis, Lactobacillus lactis, Lactococcus lactis
21. Гетероферментативное молочнокислое брожение: химизм, энергетический выход, характеристика возбудителей.
Сахара сбраживаются через пентофосфатный путь, конечные продукты при этоммолочная кислота 50%, остальное ацетат,этанол,углек.газ. Основной субстратмальтоза.

Суммарная реакция гетероферментативного брожения:
1)глюкоза + ФН + АДФ → → лактат + АТФ + этанол + СО2
2)глюкоза + 2ФН + 2АДФ + НАД+ → → лактат + 2АТФ + ацетат + СО2+ НАДН2
Представители: Leuconostoc lactis, Leuconostoc mesenteroides, Lactobacillus fermentum
22. Спиртовое брожение: химизм, энергетический выход, характеристика возбудителей. Эффект Пастера.
Сбраживание дитрисахаридов с образованием этанола и углек.газа. Окислительный этап идет по пути гликолиза. Восстановительный:
Итог: глюкоза + 2ФН + 2АДФ = 2 этанол + 2 АТФ + 2 СО2
Представители: •Saccharomyces – пекарские дрожжи, Erwinia amylovora
«Эффект Пастера»: в условиях свободного доступа кислорода воздуха процесс спиртового брожения ингибируется и активируется дыхание.
Химический выход: Брожение = -196 кДж Дыхание = -2870 кДж
23. Маслянокислое брожение: химизм, энергетический выход, характеристика возбудителей. Двухфазность брожения.

Маслянокислые бактерии:
-бактерии рода Clostridium
-облигатные анаэробы
24. Пропионовокислое брожение: химизм, энергетический выход, характеристика возбудителей. Фумаратное дыхание.
1)Пируват карбоксилируется, (донором С02-группы служит метилмалонил-КоА) с
образованием ЩавелевоУксуснойКислоты и пропионил-КоА
2)ЩУК в результате трех ферментативных этапов (аналогичных реакциям 6, 7, 8 цикла трикарбоновых кислот) превращается в янтарную кислоту(сукцинат).
3)Следующая реакция заключается в переносе КоА-группы с пропионил-КоА на янтарную кислоту (сукцинат), в результате образуются сукцинил-КоА и пропионовая кислота:
4)Пропионовая кислота накапливается в клетке, а сукцинил-коа превращается в метилмалонил-коа.

Основные продукты брожения: пропионовая кислота, уксусная, янтарная кислоты и CO2 .
Побочные продукты: молочная, муравьиная, изовалериановая кислоты, этиловый и пропиловый спирты, уксусный и пропионовый альдегиды, ацетоин, диацетил.
Состав конечных продуктов брожения зависит от культуры бактерий, состава среды и условий культивирования.
Энергетический выход: 1,5 глюкозы → 4 АТФ.
Источником дополнительных молекул АТФ, возможно, является этап восстановления фумаровой кислоты до янтарной, катализируемый фумаратредуктазой.
Восстановление фумарата до сукцината — процесс, в результате которого синтезируется АТФ по механизму фосфорилирования, сопряженного с переносом электронов.
Пропионовокислые бактерии
- Propionibacterium acnes, P. Jensenii -Факультативные анаэробы -Хемоорганотрофы
Фумаратное дыхание – вид анаэробного дыхания, конечным акцептором электронов которого является фумарат. К нему способны практически все микроорганизмы, имеющие сукцинатдегидрогеназу, осуществляющую реакцию: 2[Н+] + фумарат —» сукцинат.
В этом случае формируется короткая ЭТЦ с одним пунктом сопряжения, в котором происходит окислительное фосфорилирование Дегидрогеназы в начале ЭТЦ выделяют протоны в периплазму, затем осуществляется перенос электронов с дегидрогеназ на фумаратредуктазу через мембранный пул менохинонов,а после фумаратредуктаза связывает протоны в цитоплазме.

25. Характеристика полной аэробной дыхательной цепи.
Дыхание – это способ получения энергии, при котором донорами электронов служат органические или неорганические соединения, а акцепторами – неорганические:
кислород – аэробное дыхание сульфаты, нитраты, карбонаты, фумарат – анаэробное дыхание
АТФ образуется в процессе окислительного фосфорилирования в дыхательной цепи.
Пируват занимает центральное положение в промежуточном метаболизме: окислительное декарбоксилирование пирувата ЦТК – цикл Кребса – имеет двоякое назначение:
1. полное окисление органического субстрата и отщепление водорода (энергетическая функция), 2. снабжение клетки предшественниками для биосинтетических процессов (биосинтетическая функция).
Итог ЦТК:
–2 CO2
–3 НАД-H2
–1 ФАД-H2
–1 АТФ
Синтез АТФ за счет энергии транспорта электронов через мембрану называют окислительным фосфорилированием или фосфорилированием в дыхательной цепи. Дыхание – более эффективный путь регенерации АТФ:
-электронтранспортная цепь
-фермент АТФ-синтаза
Обе системы у прокариот находятся в плазматической мембране, а у эукариот – во внутренней мембране митохондрий.

Акцепторы электронов – неорганические или органические соединения (анаэробное дыхание).
Цитохромы – могут отсутствовать. Цепь –разветвленная или укороченная.
В анаэробных дыхательных цепях цитохромоксидазы заменены соответствующими редуктазами.
Суть дыхания сводится к передаче водорода с дегидрогеназ (НАД и ФАД) на кислород (О2) по дыхательной (электротранспортной) цепи - ЭТЦ.
НАД(Ф)-зависимые дегидрогеназы катализируют отрыв водорода от молекул субстратов и передают его на стартовый переносчик дыхательной цепи – НАД(Ф)-H2-дегидрогеназу. Акцептором водорода от НАД(Ф)-H2 являются флавиновые дегидрогеназы (ФАД).
Водород с них поступает в дыхательную цепь на уровне хинонов (убихинон – Q). Далее,стоящий первым в цепи цитохром отрывает электрон от атома водорода и передает на систему цитохромов. Протоны не принимают участия в дальнейшем транспорте дыхательной цепи и выделяются в среду. По цепочке цитохромов, набор которых специфичен для каждого вида микроорганизмов, электроны передаются на конечный цитохром (a+a3), называемый цитохромоксидазой. Последний передает электроны на молекулярный кислород с образованием ионов О2. Выделенные в среду протоны водорода связываются с ионами О2 и образуют воду.
Таким образом, в результате полного расщепления глюкозы в клетке аэробов выделяется в среду углекислый газ и вода.
Компоненты ЭТЦ располагаются в мембранах в порядке увеличения окислительного потенциала.
В трех местах этой цепи выделяется энергии столько, что становится возможным синтез макроэргической связи АТФ. При полно м окислении НАД•Н2 образуется 3 молекулы АТФ; ФАД•Н2 = 2 АТФ. К моменту завершения второй фазы дыхания в наличии имеется 10 молекул НАД•Н2 (8 образовались на этапе цикла Кребса, 2 – из гликолиза), 2 молекулы ФАД•Н2 (образовались в цикле Кребса). Расчет энергетического выхода аэробной фазы дыхания: 10 НАД•Н2 х 3 АТФ образуется 30 АТФ; 2 ФАД•Н2 х 2 АТФ = 4 АТФ. Всего в ЭТЦ образуется 34 моль АТФ. К ним следует прибавить 2 молекулы АТФ из цикла Кребса и 2 молекулы - из гликолиза. Итого – 38 АТФ – результат полного окисления одной молекулы глюкозы.
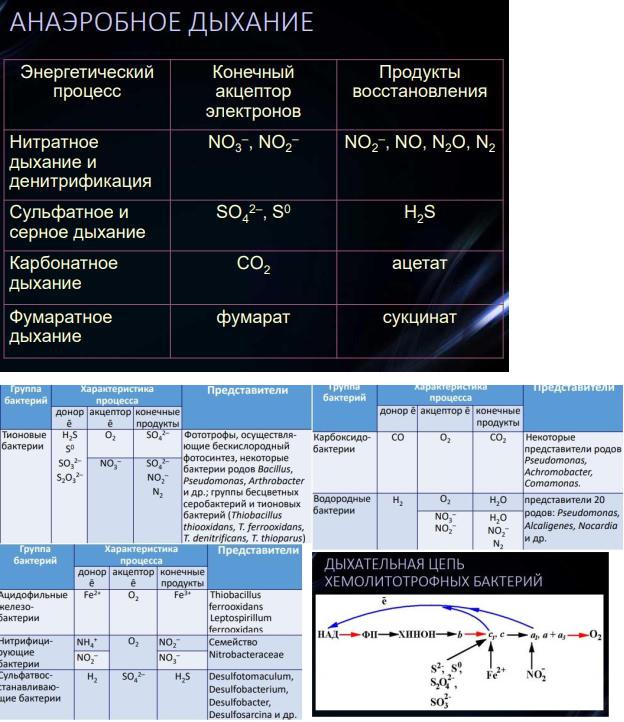
26. Типы анаэробного дыхания.
27. Особенности фотосинтеза прокариот.
Фотосинтез – это способ образования АТФ, при котором в качестве источника энергии используется энергия света.
АТФ образуется при переносе энергии света, поглощенного фотосинтетической пигментной системой – фотофосфорилировании.
Электроны проходят по электроннотранспортной цепи.
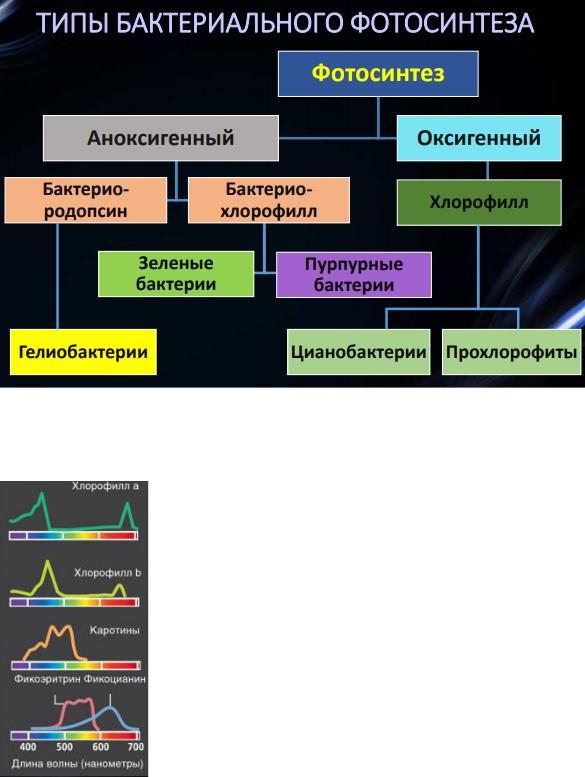
Фотосинтетические пигменты обеспечивают поглощение света с длиной волны в области
300-1100 нм.
Пигменты:
28. Характеристика оксигенных фототрофных бактерий.
Оксигенный (аэробный) фотосинтез осуществляют цианобактерии и прохлорофиты. У них, как и у растений, в качестве донора водорода образуется вода и выделяется кислород. Обладают хлорофиллом а, фикобилинами и каротиноидами. Прохлорофиты — одноклеточные неподвижные сферические грамотрицательные прокариоты, которые являются экзосимбионтами асцидий. В отличие от цианобактерий, тилакоиды про-
