
Глава 17. Нервно-мышечные заболевания
Наследственные нервно-мышечные заболевания - большая гетерогенная группа болезней, в основе которых лежит генетически детерминированное поражение нервно-мышечного аппарата (рис. 17.1, 17.2). Заболевание проявляется прогресирующими мышечными атрофиями, мышечной слабостью, парезами мускулатуры.
При диагностике учитывают возраст дебюта клинических проявлений, локализацию и прогрессирование миодистрофического процесса (наличие или отсутствие псевдогипертрофий, фасцикулярных подергиваний, эпизодов мышечной слабости, нарушений чувствительности), отягощенность семейного анамнеза, тип наследования заболевания.
К наследственным нервно-мышечным заболеваниям относят прогрессирующие мышечные дистрофии (первично-мышечные заболевания), наследственные мотосенсорные полинейропатии или невральные амиотрофии (заболевания с преимущественным первичным поражением двигательных волокон периферических нервов), а также спинальные амиотрофии (заболевания с первичным поражением мотонейронов спинного мозга).
17.1. Прогрессирующие мышечные дистрофии
В основе большинства миодистрофий лежат дефекты генов, кодирующих различные структурные белки мышечных волокон.
Прогрессирующая мышечная дистрофия Дюшенна
Заболевание связано с патологией гена, локализующегося на коротком плече Х-хромосомы в локусе Хр21 и ответственного за выработку дистрофина. До 60% всех случаев заболевания связано с делециями, в остальных случаях причинами заболевания являются дупликации или точечные мутации. Около 50% всех мутаций приходится на экзоны 5-20 или 45-53, что предположительно связано со структурой хроматина в этих областях. Продуктом гена является белок дистрофин, синтезирующийся в скелетных мышцах, миокарде и головном мозге. Дистро-
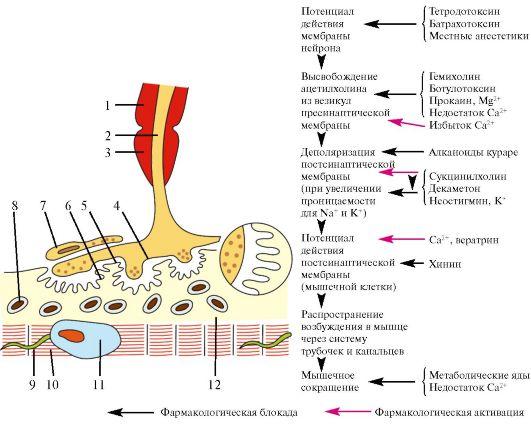 Рис.
17.1. Мионевральный
синапс. 1 - миелиновая оболочка; 2 - аксон;
3 - перехват Ранвье; 4 - пресинаптическая
мембрана; 5 - синаптическая щель; 6 -
постсинаптическая мембрана; 7- леммоцит
(шванновская клетка); 8 - митохондрия; 9
- поперечная система трубочек и канальцев;
10 - миофибриллы; 11 - ядро; 12 - саркоплазма
Рис.
17.1. Мионевральный
синапс. 1 - миелиновая оболочка; 2 - аксон;
3 - перехват Ранвье; 4 - пресинаптическая
мембрана; 5 - синаптическая щель; 6 -
постсинаптическая мембрана; 7- леммоцит
(шванновская клетка); 8 - митохондрия; 9
- поперечная система трубочек и канальцев;
10 - миофибриллы; 11 - ядро; 12 - саркоплазма
фин выполняет структурную функцию, а также различные модулирующие и сигнальные функции, связываясь с белками внеклеточного матрикса, плазматической мембраны, цитоскелета и других внутриклеточных структур. Отсутствие дистрофина в миофибриллах приводит к дезинтеграции дистрофингликанопротеинового комплекса, обеспечивающего структурно-функциональную организацию цитоскелета миофибрилл, утрате их устойчивости к циклическим актам сокращения и расслабления, разрывам. Его отсутствие повышает проницаемость мембраны для ионов кальция, что приводит к активации кальциевых протеаз, нарушению функционирования клетки и в конечном итоге к некрозу мышечных волокон.
Рис.
17.2. Основные
типы мышечных атрофий. 1 - спинальная
прогрессирующая детская амиотрофия
Верднига-Гоффманна; 2 - интерстициальная
гипертрофическая невропатия Дежерина-Сотта;
3 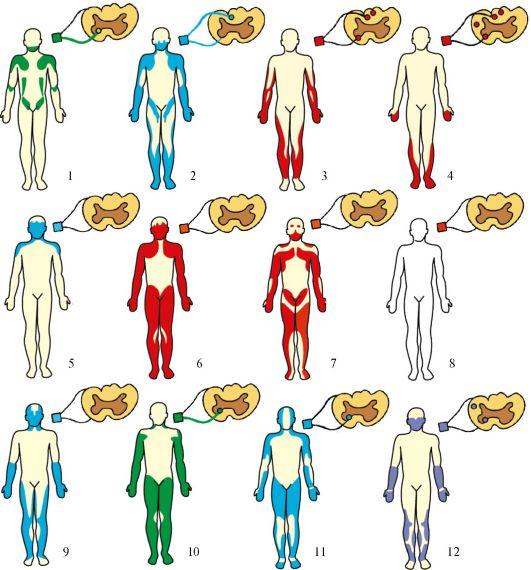
- невральная амиотрофия (прогрессирующая невральная перонеальная мышечная атрофия Шарко-Мари-Тута); 4 - болезнь Фридрейха (семейная спинно-мозжечковая атаксия); 5 - миастения; 6 - пароксизмальная миоплегия (семейный периодический паралич); 7 - прогрессирующая мышечная дистрофия; 8 - врожденная миотония Томсена (неатрофическая); 9 - атрофическая миотония; 10 - врожденная амиотония Оппенгейма; 11 - хроническая прогрессирующая семейная спинальная амиотрофия взрослых Арана-Дюшенна; 12 - боковой амиотрофический склероз Шарко. Зеленым цветом обозначен дебют заболевания в детстве, красным - в подростковом возрасте, синим - в зрелом возрасте, фиолетовым - в пожилом
Мозговая изоформа экспрессируется в коре больших полушарий, гиппокампе и клетках Пуркинье. В головном мозге дистрофин участвует в процессах нейрональной пластичности, синаптической стабильности и интеграции сигнала на клеточном уровне. Кроме того, дистрофин принимает участие в нормальном функционировании глии. Снижение интеллекта, наблюдаемое примерно у 10-20% больных с формой Дюшенна, связано с нарушением синтеза этой изоформы дистрофина.
Частота заболевания составляет 3,3 на 100 000 населения, 14 на 100 000 родившихся. В большинстве случаев болеют мальчики. Случаи заболевания у девочек редки и возможны при кариотипе Х0, мозаицизме Х0/ХХ, Х0/ХХХ, Х0/ХХХ/ХХХ и при структурных аномалиях хромосом.
Патоморфология. Разрушение мышечных волокон, их замещение соединительной и жировой тканью.
Клинические проявления. Признаки заболевания проявляются на 1-3 годах жизни. Уже на 1-м году жизни обращает на себя внимание отставание детей в моторном развитии. Они с задержкой начинают садиться, вставать, ходить. Движения неловкие, при ходьбе дети неустойчивы, часто спотыкаются, падают. В 2-3 года появляются мышечная слабость, изменения походки по типу «утиной», что связано с поражением ягодичных мышц. Наблюдается своеобразная «стереотипная» динамика движений детей во время вставания из горизонтального положения, из положения на корточках или со стула. Вставание происходит поэтапно, с активным использованием рук - «взбирание лесенкой» или «взбирание по самому себе».
Атрофии мышц всегда симметричны. Сначала они локализуются в проксимальных группах мышц нижних конечностей и в мышцах тазового пояса, в 1-3 года распространяются на проксимальные группы мышц верхних конечностей - плечевой пояс, мышцы спины. Вследствие атрофий появляются лордоз, «крыловидные» лопатки, «осиная» талия (рис. 17.3). Типичным симптомом заболевания является псевдогипертрофия икроножных мышц. При пальпации мышцы плотны, безболезненны. Мышечный тонус снижен преимущественно в проксимальных группах мышц. Сухожильные рефлексы изменяются с различной последовательностью: в ранних стадиях заболевания исчезают коленные рефлексы, затем рефлексы с двуглавой и трехглавой мышц. Ахилловы рефлексы могут долго оставаться сохранными.
Одной из отличительных особенностей формы Дюшенна является патология костносуставной, сердечно-сосудистой и нейроэндокринной систем. Костно-суставные нарушения включают в себя деформации
Рис.
17.3. Мышечная
дистрофия. а -
гипотрофия мышц плечевого и тазового
пояса, проксимальных отделов конечностей;
«крыловидные» лопатки, «осиная»
талия; б -
вставание с корточек «лесенкой» (прием
миопата); в -
псевдогипертрофия мышц икроножной
группы
позвоночника, стоп, грудины.
У многих больных в результате избирательного и неравномерного поражения различных групп мышц рано возникают мышечные контрактуры и ретракции сухожилий. Сердечнососудистые расстройства проявляются дилатационной кардиомиопатией, которая может быть одной из причин неблагоприятного исхода заболевания. На ЭКГ регистрируются изменения миокарда (блокада пучка Гиса и др.). Среди нейроэндокринных расстройств чаще встречаются синдромы Иценко-Кушинга, Бабинского-Фрелиха.
Снижение интеллекта разной выраженности отмечается у большинства больных и, как правило, не соотносится с тяжестью поражения скелетной мускулатуры и тяжестью самого заболевания. Наиболее часто у детей выявляются относительно неспецифические изменения в виде затруднения концентрации внимания, сложности в воспроизведении недавно полученной информации, нарушения слуховой памяти, произношения, усвоения материала.
При позитронной эмиссионной томографии и при 31Р МР-спектроскопии наиболее выраженные изменения, отражающие нарушение утилизации глюкозы (по данным ПЭТ) и изменение соотношения неорганического фосфора, АТФ, фосфомоноэстеров и фосфокреатинина (МР-спектроскопия), отмечаются в коре лобных долей больших полушарий и в мозжечке, в меньшей степени - в гиппокампе.
Форма Беккера является аллельным вариантом миодистрофии Дюшенна и также связана со структурным дефектом гена дистрофина. Наследуется по рецессивному типу, сцепленному с Х-хромосомой. Первые клинические проявления отмечаются позднее, чем при форме Дюшенна, чаще в возрасте 10-15 лет, а само заболевание протекает значительно мягче. Мышечная слабость, повышенная мышечная утомляемость при физической нагрузке, псевдогипертрофии икроножных мышц не достигают такой выраженности, как при форме Дюшенна. Мышечный тонус снижен незначительно. Сухожильные рефлексы долго остаются сохранными. В поздних стадиях болезни могут наблюдаться изменения походки по типу «утиной», компенсаторные миопатические приемы при вставании. Заболевание прогрессирует медленно на протяжении многих лет. Сердечно-сосудистые расстройства выражены умеренно. Иногда наблюдается блокада ножек пучка Гиса. Эндокринные нарушения проявляются гинекомастией, снижением либидо, импотенцией. Выраженных изменений интеллекта не отмечается. Больные долго сохраняют работоспособность.
Диагностика и дифференциальная диагностика. Диагноз устанавливают на основании клинических проявлений, данных биохимических исследований (повышение в крови активности КФК, ЛДГ), электромиографии (признаки первичного мышечного поражения) и молекулярно-генетического анализа. Для уточнения аллельной формы заболевания проводится биопсия мышц для определения дистрофина (при форме Дюшенна в скелетных мышцах дистрофин не выявляется; при форме Беккера дистрофин синтезируется, но в большинстве случаев его уровень снижен). При обследовании матерей - носителей патологического гена (биопсия ворсин хориона на 8-9 неделе) выявляют заболевание у мальчиков.
Дифференцировать форму Дюшенна следует от спинальной амиотрофии Верднига-Гофмана, а форму Беккера - от прогрессирующих мышечных дистрофий Дюшенна, конечностно-поясных форм прогрессирующих мышечных дистрофий, спинальной амиотрофии Кугельберга-Веландера, метаболических и эндокринных миопатических синдромов.
|
|
Прогрессирующая мышечная дистрофия Эмери-Дрейфуса
Наследуется по рецессивному типу, сцепленному с Х-хромосомой. Первичный молекулярно-генетический дефект находится на локусе Хq28, который отвечает за синтез белка эмерина. Эмерин относится кбелкам ядра клетки и предположительно стабилизирует ядерную мембрану при повторных актах сокращения - расслабления.
Клинические проявления. Первые признаки заболевания проявляются в 5-7 лет. Развиваются ранние контрактуры в локтевых суставах, ретракции ахилловых сухожилий. Как и при других формах прогрессирующих мышечных дистрофий, заболевание начинается с мышечной слабости, повышенной мышечной утомляемости при физической нагрузке. Атрофии возникают симметрично и сначала локализуются в проксимальных группах мышц нижних конечностей: тазового пояса, бедер. Проксимальные группы мышц верхних конечностей вовлекаются значительно позднее. Заболевание медленно прогрессирует. У многих больных имеются кардиальные нарушения, выраженность которых является важным признаком при определении прогноза заболевания.
Диагностика и дифференциальная диагностика. Диагноз устанавливают на основании молекулярно-генетического исследования, а также особенностей клинической картины (ранние контрактуры локтевых суставов, ретракции ахилловых сухожилий, сердечно-сосудистые нарушения в виде аритмий, медленное прогрессирующее течение).
Дифференцировать болезнь следует от прогрессирующих мышечных дистрофий Беккера, Дюшенна, Эрба-Рота, спинальной амиотрофии Кугельберга-Веландер.
Конечностно-поясные формы прогрессирующих мышечных дистрофий
Конечностно-поясные формы (КПФ) прогрессирующих мышечных дистрофий - это генетически гетерогенная группа заболеваний, объединенная общим клиническим симптомокомплексом - нарастающей слабостью и атрофиями в проксимальных отделах конечностей. К настоящему времени выявлены варианты, наследуемые аутосомнодоминантно и аутосомно-рецессивно. Аутосомно-доминантный тип (тип I) передачи наблюдается в 5-10% случаев, аутосомно-рецессивный (тип II) - в 90-95% случаев. Аутосомно-доминантно передаются мышечные дистрофии, развивающиеся вследствие нарушения синтеза белков плазматической мембраны (кавеолин-3), белков саркомеры (миотилин) и ядерных белков (ламин А/С). Аутосомно-рецессивно наследуются варианты КПФ, при которых нарушается выработка саркогликанов α, β, γ, δ - белков, входящих в состав плазматической мембраны. Эта группа прогрессирующих мышечных дистрофий носит
название саркогликанопатий. Также аутосомно-рецессивно передаются мышечные дистрофии, связанные с нарушением синтеза дисферилина - белка плазматической мембраны, калпаина-3 и TRIM32 - белков цитозоля клетки, а также титина и телетонина - белков саркомеры. Форма прогрессирующей мышечной дистрофии, описанная Эрбом и Ротом, по современной классификации относится к типу IIА, и ген, ответственный за ее развитие, картирован на хромосоме 15 (15q15.1-21.1).
Клинические проявления. Первые признаки заболевания проявляются преимущественно в 14-16 лет, редко - в 5-10-летнем возрасте. При аутосомно-доминантной передаче дебют наблюдается позднее - в 20-25 лет. Необходимо отметить, что каждая из форм прогрессирующей мышечной дистрофии имеет определенные клинические особенности. Так, наиболее тяжело обычно протекают саркогликанопатии. Это связано с тем, что саркогликаны объединены в комплекс, участвующий вместе с дистрофином в поддержании целостности мембраны мышечной клетки при повторных актах сокращения-расслабления. Вовлечение в патологический процесс одного из саркогликанов нарушает структуру всего комплекса и приводит ко вторичному нарушению функционирования других саркогликанов. При всех вариантах заболевания начальными симптомами являются мышечная слабость, патологическая мышечная утомляемость при физической нагрузке, изменение походки по типу «утиной». В начале болезни атрофии локализуются в проксимальных группах мышц нижних конечностей (форма Эрба-Рота), в более поздних стадиях в процесс вовлекаются мышцы спины и живота. Иногда миодистрофический процесс одновременно поражает мышцы тазового и плечевого пояса. Вследствие атрофий возникают лордоз, «крыловидные» лопатки, «осиная» талия. При вставании больные применяют вспомогательные приемы (вставание «лесенкой»). Псевдогипертрофии мышц, контрактуры суставов, сухожильные ретракции, как правило, выражены умеренно. Характерно снижение сухожильных рефлексов (коленных, с двуглавой и трехглавой мышц плеча).
|
|
Диагностика и дифференциальная диагностика. Вследствие генетической гетерогенности этой группы прогрессирующих мышечных дистрофий основным при установлении диагноза является ДНК-анализ, что позволяет установить форму заболевания и определить прогноз. При необходимости проводят электромиографию и биопсию мышц. Дифференцировать эту группу заболеваний следует от прогрессирующей мышечной дистрофии Беккера, спинальной амиотрофии Кугельберга-Веландера, миопатических синдромов.
Лицелопаточно-плечевая мышечная дистрофия Ландузи-Дежерина
Частота составляет 4-5 на 100 000 населения. Наследуется по аутосомно-доминантному типу с очень высокой пенетрантностью (до 95% к 20-25 годам жизни). До 20-30% заболевших не имеют положительного генеалогического анамнеза, и эти случаи рассматриваются как новые мутации. Заболевание развивается вследствие делеции на длинном плече хромосомы 4 (4q35), реже его развитие связано с локусом 10q26. Делеция локализуется в области, непосредственно прилегающей к теломере, и не захватывает смысловых последовательностей гена. Предполагается, что мутация в этой области приводит к изменению структуры хроматина, а это, в свою очередь, изменяет активность близлежащих генов (так называемый эффект положения), в частности генов, кодирующих транскрипционные факторы миогенеза.
Клинические проявления. Первые признаки появляются преимущественно в возрасте 10-20 лет. Мышечная слабость, атрофии затрагивают мимическую мускулатуру лица, лопаток, плеч. Вследствие атрофии лицо становится гипомимичным, типичны «полированный» лоб, лагофтальм, «поперечная» улыбка, толстые, иногда вывороченные губы («губы тапира»). Атрофии двуглавой и трехглавой мышц плеча, большой грудной, передней зубчатой, трапециевидной мышц обусловливают возникновение симптомов «свободных надплечий», «крыловидных» лопаток, появление широкого межлопаточного промежутка, уплощения грудной клетки, сколиоза. В ряде случаев атрофии распространяются на мышцы тазового пояса и ног. Псевдогипертрофии отмечаются в икроножных и дельтовидных мышцах. Мышечный тонус в ранних стадиях заболевания снижен в проксимальных группах мышц, затем - диффузно. Сухожильные рефлексы снижены преимущественно с двуглавой и трехглавой мышц плеча. Заболевание медленно прогрессирует, больные долго сохраняют работоспособность.
|
|
Диагностика и дифференциальная диагностика. Диагноз устанавливают на основании клинической картины (преимущественно лицелопаточно-плечевая локализация миодистрофического процесса) и результатов молекулярно-генетического анализа. Дифференцировать заболевание следует от других прогрессирующих мышечных дистрофий.
