
- •Химическая схема
- •Задание
- •Расчётная часть
- •Описательная часть
- •Обосновать использование 2-х ступенчатой системы конверсии метана с точки зрения возможностей реализации оптимального технологического режима
- •Функциональная схема производства аммиака из природного газа методом паровоздушной конверсии
- •Структурная схема хтс производства аммиака
- •Технологическая схема хтс производства аммиака
- •Список литературы
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
ФГБОУ ВО «Российский химико-технологический университет имени Д. И. Менделеева»
КАФЕДРА ОБЩЕЙ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
Расчётно-графическая работа
«Материальные и тепловые расчёты процесса 2-х ступенчатой конверсии метана в производстве
аммиака»
Вариант 321455
Работу принял к.т.н., доц. Иванов И.И.
Работу выполнила студент группы … Фёдоров Ф.Ф.
Москва
2019
ОГЛАВЛЕНИЕ
Задание……………………………………………………………………………..1
Расчётная часть……………………………………………………………………3
Описательная часть……………………………………………………………...12
Список литературы………………………………………………………………21
ЗАДАНИЕ
-
Схема процесса
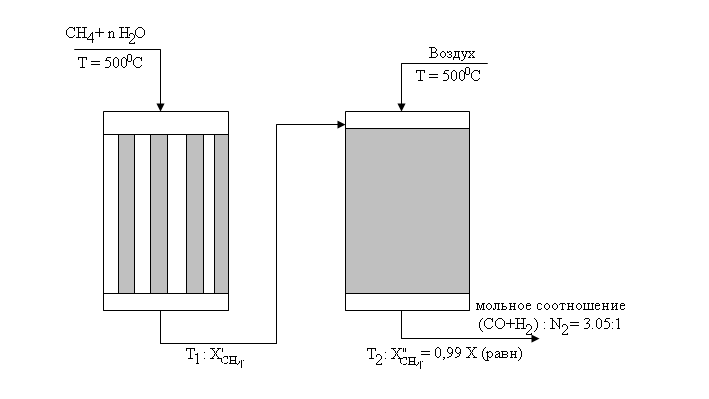
-
Таблица исходных данных
|
№ |
Наименование параметра |
Размерность |
|
|
1 |
Температура, Т1 |
°С |
820 |
|
2 |
Температура, Т2 |
°С |
1020 |
|
3 |
Производительность,
|
т NH3/сутки |
1000 |
|
4 |
Концентрация
N2
в природном газе,
|
% об. |
5.0 |
|
5 |
Потери АВС с продувным газом |
% об. |
9 |
|
6 |
Коэффициент избытка H2O |
|
4 |
|
7 |
Давление на стадии конверсии метана |
атм |
1 |
АВС – азотоводородная смесь
-
Химическая схема
В I-ом реакторе:
СH4 + H2O = 3Н2 + СО – 206,4 кДж/моль
(1)
В II-ом реакторе:
а) СH4 + H2O = 3Н2 + СО – 206,4 кДж/моль
(2)
б) H2 + ½ O2 = H2O + 242,0 кДж/моль
(3)
-
Задание
а) Расчётная часть:
1) Рассчитать исходные потоки всех компонентов системы;
2)
Составить тепловой баланс II-ого
реактора и рассчитать степень превращения
метана (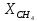 )
после I-го реактора;
)
после I-го реактора;
3) Составить покомпонентный материальный баланс процесса, результаты расчётов представить в виде таблицы.
б) Описательная часть:
1) ОПЕРАЦИОННАЯ СХЕМА производства аммиака из природного газа методом паровоздушной конверсии (дать краткое описание каждой стадии);
2) Обосновать использование 2-х ступенчатой системы конверсии метана с точки зрения возможностей реализации оптимального технологического режима;
3) Изобразить схематично все типы каталитических химических реакторов, которые используются на различных стадиях производства аммиака с обоснованием их использования для данного типа реакции (с учётом особенностей технологического режима);
4) ФУНКЦИОНАЛЬНАЯ СХЕМА производства аммиака из природного газа методом паровоздушной конверсии;
5) СТРУКТУРНАЯ СХЕМА ХТС производства аммиака;
6) ТЕХНОЛОГИЧЕСКАЯ СХЕМА ХТС производства аммиака;
7) ОПЕРАТОРНАЯ СХЕМА подсистемы ХТС производства аммиака (5-6 элементов по индивидуальному заданию).
Расчётная часть
1. Расчёт исходных потоков всех компонентов системы
По условию задания производительность по аммиаку – 1000 т/сутки. Тогда производительность в кг/сутки и кмоль/сутки составит:
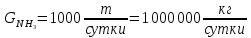
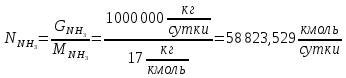
Известно, что аммиак получается в результате реакции:
N2 + 3 H2 = 2 NH3
На образование одного объёма аммиака расходуется два объёма азотно-водородной смеси (АВС) согласно уравнению реакции:

При продувке часть АВС теряется (потери составляют по условию задания 9% об.), тогда начальное количество АВС составляет:

Рассчитаем количество азота и водорода, необходимое для получения заданного количества АВС. Теоретически на образование 2 кмоль аммиака расходуется 3 кмоль водорода, который образуется в результате реакции:
СО + H2O = Н2 + СО2
Но данная реакция является обратимой, поэтому не идёт до полного израсходования монооксида углерода. Тогда коэффициент, учитывающий неполное превращения СО в водород, будет равен:
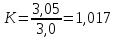 ,
т.к. по условию мольное соотношение
(CO+H2):N2
= 3,05:1
,
т.к. по условию мольное соотношение
(CO+H2):N2
= 3,05:1
Для водорода:

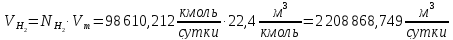

Для азота:
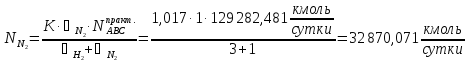

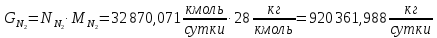
Для монооксида углерода:
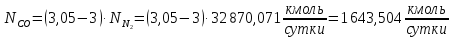

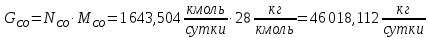
Далее рассчитаем количество исходного природного газа, воздуха и воды.
СH4 + H2O =3H2 + CO
СО + H2O = Н2 + СО2
Суммарно получаем:
СH4 + H2O + СО + H2O = 3H2 + CO + Н2 + СО2
СH4 + 2H2O = 4H2 + СО2
Также необходимо учесть, что подаваемый в составе воздуха кислород расходуется полностью на сгорание образованного водорода по реакции:
O2 + 2H2 = 2H2O
Степень превращения
исходного природного газа на выходе из
всей системы составит 0,99·Хpавн,
где Хpавн
– равновесная
степень превращения. Равновесная
степень превращения при температуре
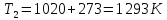 ,
давлении 1
ат (~ 0,1 МПа)
и соотношении пар : газ = 4:1:
,
давлении 1
ат (~ 0,1 МПа)
и соотношении пар : газ = 4:1:
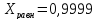
Тогда степень превращения метана после двух ступеней конверсии будет равна:

Составим систему уравнений для нахождения неизвестных величин. Азот не вступает в реакции, приходит из воздуха и природного газа.
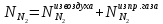
Водород образуется при газификации метана, а также расходуется на реакцию сгорания:
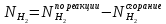
Приведём систему
уравнений к системе с двумя неизвестными
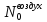 и
и
 – исходные количества воздуха и
природного газа, соответственно:
– исходные количества воздуха и
природного газа, соответственно:
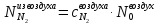
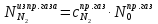
Из брутто-уравнения следует, что из одного моля CH4 образуется 4 моля H2, c учётом степени превращения:
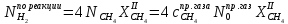
На сгорание 1 моля кислорода расходуется два моля водорода:

Получаем систему уравнений:
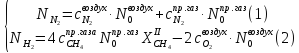
Для расчёта примем, что воздух сухой, состоит только из кислорода и азота, в соотношении 0,21:0,79 об. доли, соответственно.
Выразим
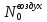 из уранения (1), подставим в (2):
из уранения (1), подставим в (2):
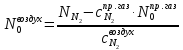
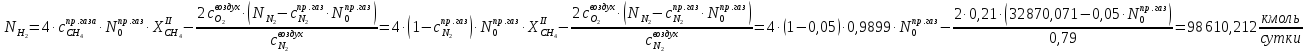

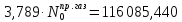

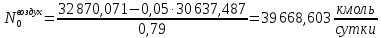
Найдём количество метана и азота в природном газе:
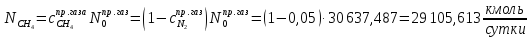

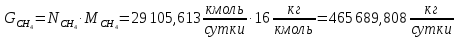
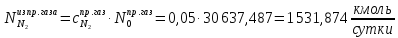
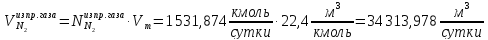

Рассчитаем количество исходное количество воды:
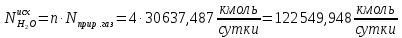
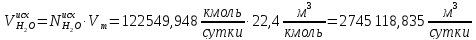

Найдём количество кислорода и азота в воздухе:
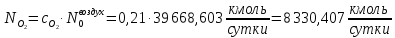
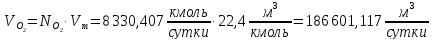
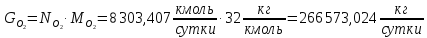
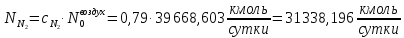
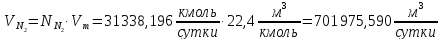

Вода в процессе расходуется по 1 реакции и образуется по 2 реакции:
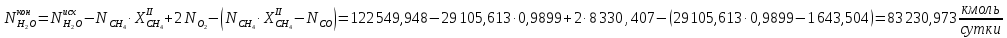
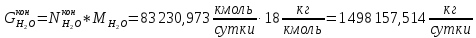
Образовавшийся диоксид углерода:
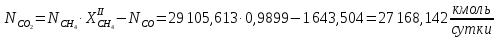

Количество метана, оставшегося после реакции:
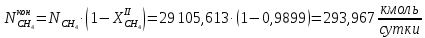
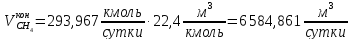
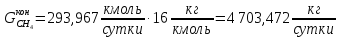
2.
Расчёт
теплового баланса II-го
реактора и степени превращения метана
(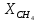 )
после I-го реактора
)
после I-го реактора
Таблица (основана на 1табл.6):
|
№ |
Вещество |
Уравнение для нахождения значения теплоёмкости Ср |
Значение Ср при Т=500°С (773 К),
|
Значение Ср при Т1=820°С (1093 К),
|
Значение Ср при Т2=1010°С (1283 К),
|
|
1 |
Азот ( |
|
31,17 |
32,54 |
33,35 |
|
2 |
Водород ( |
|
- |
30,89 |
31,49 |
|
3 |
Кислород ( |
|
33,45 |
34,85 |
- |
|
4 |
Монооксид углерода (CO) |
|
- |
32,85 |
33,64 |
|
5 |
Водяной пар ( |
|
38,33 |
41,73 |
43,76 |
|
6 |
Метан ( |
|
63,52 |
82,20 |
93,18 |
Рассчитаем тепловые потоки, входящие во второй реактор.
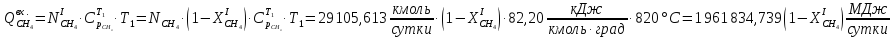

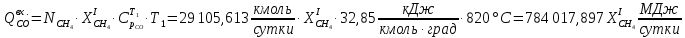
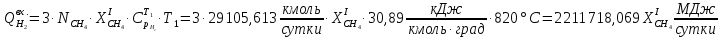
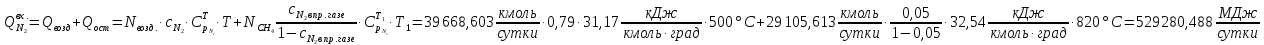

Рассчитаем массовые и тепловые потоки, выходящие из II-го реактора:
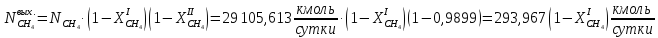

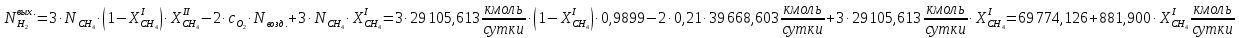

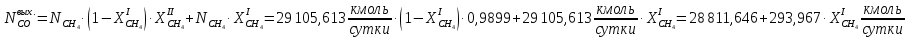
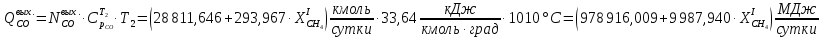
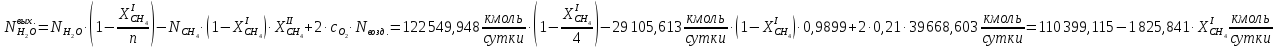
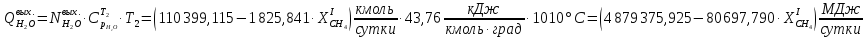

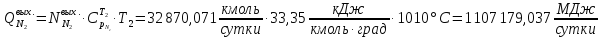
Система имеет дополнительные источники энергии в виде тепловых эффектов реакций:
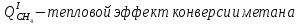
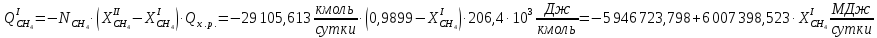
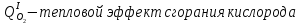
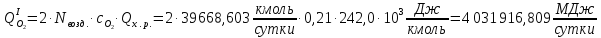
Рассчитаем степень
превращения
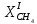 :
:
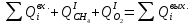

Подставим полученные выше выражения в уравнение, получим степень превращения метана после I-го реактора:
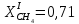
Тогда тепловой баланс II-го реактора:
|
Входящие потоки |
Выходящие потоки |
|||
|
Наименование компонента |
|
Наименование компонента |
|
|
|
Метан |
568 932,074 |
Метан |
8 023,072 |
|
|
Водяной пар |
3 449 143,593 |
Водород |
2 239 073,706 |
|
|
Монооксид углерода |
556 652,707 |
Монооксид углерода |
986 007,446 |
|
|
Водород |
1 570 319,829 |
Вода |
4 822 080,494 |
|
|
Азот |
529 280,488 |
Азот |
1 107 179,037 |
|
|
Кислород |
139 326,051 |
|
|
|
|
Тепловой эффект конверсии метана |
-1 681 470,847 |
|
|
|
|
Тепловой эффект сгорания кислорода |
4 031 916,809 |
|
|
|
|
|
|
|
|
|
|
Всего |
9 164 100,704 |
Всего |
9 162 363,755 |
|
3. Покомпонентный материальный баланс системы
Составим материальный баланс по рассчитанным выше данным:
|
Входящие потоки |
Выходящие потоки |
|||||||||
|
№ |
Наименование компонента |
кг/час |
|
№ |
Наименование компонента |
кг/час |
|
|||
|
1 |
Природный газ, в т.ч.: |
24 190,928 |
28 594,988 |
1 |
АВС, в т.ч.: |
|
|
|||
|
2 |
метан |
19 403,742 |
27 165,239 |
2 |
водород |
8 217,518 |
92 036,198 |
|||
|
3 |
азот |
1 787,186 |
1 429,749 |
3 |
азот |
38 348,416 |
30 678,733 |
|||
|
4 |
Водяной пар |
91 912,461 |
114 379,952 |
4 |
монооксид углерода |
1 917,421 |
1 533,937 |
|||
|
5 |
Воздух, в т.ч.: |
47 668,438 |
37 024,030 |
5 |
Метан |
195,978 |
274,369 |
|||
|
6 |
кислород |
11 107,209 |
7 775,047 |
6 |
Вода |
62 423,230 |
77 682,241 |
|||
|
7 |
азот |
36 561,229 |
29 248,983 |
7 |
Диоксид углерода |
49 808,260 |
25 356,933 |
|||
|
|
|
|
|
|
|
|
|
|||
|
Всего |
160 771,827 |
179 998,969 |
Всего |
160 910,823 |
227 562,411 |
|||||
Погрешность:
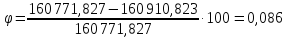

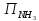
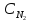
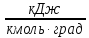
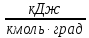
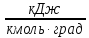
 )
)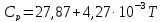
 )
)
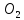 )
)
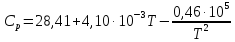
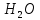 )
)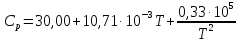
 )
)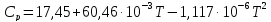
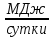
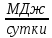
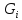 ,
,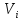 ,
,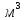 /час
(н.у.)
/час
(н.у.) ,
,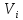 ,
,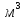 /час
(н.у.)
/час
(н.у.)