
ответы на коллоки / коллок бх2
.docx|
Пируватдегидрогеназный комплекс (ПДК) молекулярной массой 6*106 д., включает в себя три вида ферментов (Е1-Е3) и пять видов коферментов. При этом 2 кофермента (НАД и HS-КоА) находятся в свободном состоянии и входят в состав комплекса только в момент реакции. Общий вид реакции окислительного декарбоксилирования пирувата:
Ферменты пируватдегидрогеназного комплекса.Е1 – пируватдегидрогеназа декарбоксилирующая;Е2 – дигидролипоилацетилтрансфераза (трансацетилаза);Е3 – дигидролипоилдегидрогеназа. Коферменты пируватдегидрогеназного комплекса Тиаминдифосфат (ТДФ, ТПФ), содержащий витамин В1, кофактор пируватдегидрогеназы. Липоевая кислота, кофактор трансацетилазы. Кофермент ФАД, содержащий витамин В2, кофактор дегидрогеназы дигидролипоевой кислоты. Кофермент НАД, содержащий витамин РР. Кофермент НS-КоА, содержащий аденин, рибозу, два остатка фосфорной кислоты, пантотеновую кислоту (витамин В3). Окислительное декарбоксилирование ПВК протекает в несколько стадий, в процессе которых двухуглеродный фрагмент, образующийся из ПВК, переносится на липоевую кислоту, а затем на HS-КоА. Витамины, входящие в состав пируватдегидрогеназного комплекса В состав ПДК входит пять витаминов (РР. В2, липоевая кислота, В1, пантотеновая кислота). Липоевая кислота - витаминоподобное вещество, представляет собой восьмиуглеродную жирную кислоту с двумя -SH группами. Биологическая роль:является коферментом ПДК, участвует в окислении α - кетокислот. Пантотеновая кислота является витамином, который, в свою очередь, включает β - аланин и производное масляной кислоты. Она распространена в животных и растительных продуктах. Суточная потребность в пантотеновой кислоте составляет до 10 мг. Биологическая роль: входит в состав НS- КоА и участвует в окислительном декарбоксилировании α - кетокислот, участвует в активации жирных кислот. Авитаминоз проявляется дерматитом, депигментацией волос, поражением нервной системы. Витамин В1 включает в свой состав пиримидиновое кольцо, содержит аминогруппу. Суточная потребность в нём составляет 2 мг. Тиамин содержится в злаках, дрожжах. Биологическая роль: входит в состав кофермента ТДФ и участвует в окислительном декарбоксилировании α - кетокислот, а также является коферментом транскетолазной реакции в пентозофосфатном пути окисления глюкозы. Авитаминоз проявляется полиневритами (болезнь бери-бери). Регуляция пируватдегидрогеназного комплекса осуществляется путём фосфолирирования - дефосфолирирования пируватдегидрогеназы Активаторами ПДК служат АДФ и НАД окисленный. Ингибиторами этого комплекса являются АТФ и НАДН2.. Биологическая роль окислительного декарбоксилирования пирувата Биологическое значение процесса окислительного декарбоксилирования пировиноградной кислоты заключается в том, что оно является важным этапом катаболизма, позволяющим включаться в цикл Кребса тем веществам, при распаде которых образуется ПВК. Образовавшаяся молекула НАДН2 окисляется в длинной дыхательной цепи с образованием 3-х молекул АТФ. Окислительное декарбоксилирование пирувата протекает внутри митохондрий. |
субстратное фосфорилирование — процесс образования АТФ, не связанный с мембранами. В этом случае АТФ образуется За счет того, что фосфатная группа перемещается от (субстрата) к АДФ (например, образование АТФ при гликолизе). Этот способ связан с передачей макроэргического фосфата субстрата на АДФ. К таким веществам относятся метаболиты гликолиза (1,3-дифосфоглицериновая кислота, фосфоенолпируват), цикла трикарбоновых кислот (сукцинил-SКоА) и креатинфосфат. Энергия гидролиза их макроэргической связи выше, чем 7,3 ккал/моль в АТФ, и роль указанных веществ сводится к использованию этой энергии для фосфорилирования молекулы АДФ до АТФ. Отличия: разные источники энергии, для окислительного необходимы движение электронов в дых цепи, для субстратного необ-ма энергия макроэргической связи.оксилительное на мембране митохондрий, субстратное в цитозоле. |
|
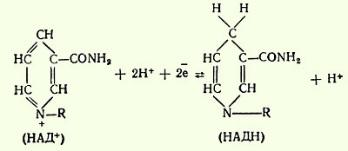
3. К числу пиридинзависимых дегидрогеназ относится свыше 150 ферментов, которые катализируют восстановление НАД и НАДФ различными органическими субстратами. Катализируемые пиридинзависимыми дегидрогеназами реакции можно изобразить так:
Способность НАД и НАДФ играть роль промежуточного переносчика водорода связана с наличием в их структуре амида никотиновой кислоты. В электронно-протонной форме обратимое гидрирование - дегидрирование (присоединение и отдача протонов и электронов) этих коферментов может быть представлено с помощью следующего уравнения
|
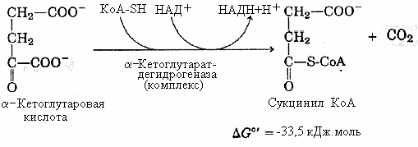
18.Взаимосвязь цикла Кребса и тканевого дыхания. Последние три реакции обратимы, но поскольку НАДН∙Н+ захватывается дыхательной цепью, равновесие реакции сдвигается вправо, т.е. в сторону образования оксалацетата. Как видно, за один оборот цикла происходит полное окисление, “сгорание”, молекулы ацетил-КоА. В ходе цикла образуются восстановленные формы никотинамидных и флавиновых коферментов, которые окисляются в дыхательной цепи митохондрий. Таким образом, цикл Кребса находится в тесной взаимосвязи с процессом клеточного дыхания. Для работы цикла Кребса и дыхательной цепи требуются следующие витамины: В1, В2, РР, Q, пантотеновая и липоевая кислоты. Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Особенностью регуляции ЦТК является зависимость всех четырех дегидрогеназ цикла (изоцитратдегидрогеназы, а-кетоглутаратдегидрогеназы, сукцинатдегидрогеназы, малатдегидрогеназы) от отношения [NADH]/[NAD + ]. Активность цитратсинтазы тормозится высокой концентрацией АТР и собственным продуктом — цитратом. Изоцитратдегидрогеназа ингибируется NADH и активируется цитратом. а-Кето- глутаратдегидрогеназа подавляется продуктом реакции — сукцинил-СоА и активируется аденилатами. Окисление сукцината сукцинатдегидрогеназой тормозится оксалоацетатом и ускоряется АТР, ADP и восстановленным убихиноном (QH2). Наконец, малатдегидрогеназа ингибируется оксалоацетатом и у ряда объектов — высоким уровнем АТР. |
|
|
19.Окислительное фосфорилирование.— метаболический путь, при котором энергия, образовавшаяся при окислении питательных веществ, запасается в митохондриях клеток в виде АТФ. Окислительное фосфорилирование состоит из процессов окисленияифосфорилирования, которые между собой сопряжены. Процесс окисления Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами. Этапы движения е- по дыхательной цепи: 2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). КоQ с 2е- забирает у воды 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II). КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство. Цитохром С переносит е- c III комплекса на IV комплекс. IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). Комплекс I – НАДН2 дегидрогеназный комплекс – самый большой из дыхательных ферментных комплексов – имеет молекулярную массу свыше 800КДа, состоит из более 22 полипептидных цепей, в качестве коферментов содержит ФМН и 5 железо-серных (Fe2S2 и Fe4S4) белков. Для биосинтеза АТФ необходимы 2 условия: 1)потенциал свыше 0,2 вольта, 2)наличие активного фермента – протонзависимой-АТФ-синтазы. |
|
20.Сопряжение тканевого дыхания и окислительного фосфорилирования в дых.цепи. Сопряжение в дыхательной цепи— это такое состояние, когда окисление (перенос электронов) сопровождается фосфорилированием, то есть синтезом АТФ. Разобщение— это состояние дыхательной цепи, когда окисление идет, а фосфорилирование не происходит, то есть пункты фосфорилирования выключены.Е в виде тепла. Разобщение вызывают липофиль-ные вещества, которые способны переносить протоны водорода с внешней стороны внутренней мембраны митохондрий на внутреннюю, минуя АТФ-синтетазу. 2,4-ДНФ (динитрофенол), яды промышленных производств, бактериальные токсины, набухание митохондрий, жирные кислоты, ионофоры (вещества, переносящие ионы через мембрану). Разобщители повышают скорость переноса электронов по дыхательной цепи и выводят ее из под контроля АТФ. Выделяют три основных группы ингибиторов: 1. действующие на I комплекс, например, амитал (производное барбитуровой кислоты), ротенон, прогестерон, 2. действующие на III комплекс, например, экспериментальный антибиотик антимицин А, 3. действующие на IV комплекс, например, сероводород (H2S), угарный газ (СО), цианиды (-CN). Окисление молекулы NADH в ЦПЭ сопровождается образованием 3 молекул АТФ; электроны от FAD-зависимых дегидрогеназ поступают в ЦПЭ на KoQ, минуя первый пункт сопряжения. Поэтому образуются только 2 молекулы АТФ. Отношение количества фосфорной кислоты (Р), использованной на фосфорилирование AДФ, к атому кислорода (О), поглощённого в процессе дыхания, называют коэффициентом окислительного фосфорилирования и обозначают Р/О. Бурый жир содержит много митохондрий. В мембране митохондрий имеется большой избыток дыхательных ферментов по сравнению с АТФ-синтазой. Около 10% всех белков приходится на так называемый разобщающий белок (РБ-1) - термогенин. Бурый жир имеется у новорождённых, но его практически нет у взрослого человека. |
21.Регуляция тканевого дыхания и окислительного фосфорилирования. Дыхательный контроль Окисление субстратов и фосфорилирование АДФ в митохондриях прочно сопряжены. Скорость использования АТФ регулирует скорость потока электронов в ЦПЭ. Если АТФ не используется и его концентрация в клетках возрастает, то прекращается и поток электронов к кислороду. С другой стороны, расход АТФ и превращение его в АДФ увеличивает окисление субстратов и поглощение кислорода. Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. Механизм дыхательного контроля характеризуется высокой точностью и имеет важное значение, так как в результате его действия скорость синтеза АТФ соответствует потребностям клетки в энергии. Запасов АТФ в клетке не существует. Относительные концентрации АТФ/АДФ в тканях изменяются в узких пределах, в то время как потребление энергии клеткой, т.е. частота оборотов цикла АТФ и АДФ, может меняться в десятки раз. Общее содержание АТФ в организме 30-50 г, но каждая молекула АТФ в клетке "живёт" меньше минуты. В сутки у человека синтезируется 40-60 кг АТФ и столько же распадается. Увеличение концентрации АДФ немедленно приводит к ускорению дыхания и фосфорилирования. |
|
22.Понятие о метаболизме,метаболических путях.. Метаболизм - совокупность химических превращений веществ от момента поступления их в клетку до выделения конечных продуктов. Сумма процессов катаболизма и анаболизма. Метаболические пути - пути это пути преобразования вещества путем катаболизма и анаболизма. Катаболизм - процесс расщепления органических молекул до конечных продуктов. Конечные продукты превращений органических веществ у животных и человека - СО2, Н2О и мочевина. В процессы катаболизма включаются метаболиты, образующиеся как при пищеварении, так и при распаде структурно-функциональных компонентов клеток. Реакции катаболизма сопровождаются выделением энергии (экзергонические реакции). Анаболизм объединяет биосинтетические процессы, в которых простые строительные блоки соединяются в сложные макромолекулы, необходимые для организма. В анаболических реакциях используется энергия, освобождающаяся при катаболизме (эндергонические реакции). конечныйпродукт метаболизма,-промежуточныйпродукт,-узловойметаболит. Узловой метаболит-вещество, которое имеет несколько путей образования и использования. Экзерогонические реакции – G < 0 и системой совершается работа (окисление глюкозы) Эндерогонические – G > 0 и над системой совершается работа. Если процесс катаболизма рассматривать с общей точки зрения, то можно выделить три основные его части: Расщепление в пищеварительном тракте. Это гидролитические реакции, превращающие сложные пищевые вещества в относительно небольшое число простых метаболитов: глюкоза, аминокислоты, глицерин, жирные кислоты. Специфические пути катаболизма. Простые метаболиты подвергаются специфическим реакциям расщепления, в результате которых образуется либо пировиноградная кислота, либо ацетил — КоА. Причем ацетил — КоА может образоваться из пирувата в результате окислительного декарбоксилирования. Могут также образоваться другие соединения, непосредственно включающиеся в цитратный цикл. Цитратный цикл и дыхательная цепь завершают расщепление пищевых веществ до конечных продуктов — СО2 и Н2О. Следовательно, начиная со стадии образования пирувата происходит унификация путей катаболизма. Из большого числа исходных соединений образуется всего два — пируват и ацетил — СоА. Процесс, начинающийся от пирувата, называется общим путем катаболизма и в свою очередь включает: окислительное декарбоксилирование пирувата и цитратный цикл. Именно в общем пути катаболизма образуется основная масса субстратов для реакций дегидрирования. Совместно с дыхательной цепью и окислительным фосфорилированием общий путь катаболизма является основным источником энергии в форме АТР. |
23.Понятие о макроэргических соединениях организма. Макроэргические соединения – органические соединения живых клеток, содержащие богатые энергией, или макроэргические связи. (сахарофосфаты, АТФ, УДФ и др.) АТФ (аденозинтрифосфорная кислота) – нуклеотид, образованный аденозином и тремя остатками фосфорной кислоты. Во всех живых организмах выполняет роль универсального аккумулятора и переносчика энергии. Под действием специальных ферментов концевые фосфатные группы отщепляются с освобождением энергии, которая идет на синтетические и другие процессы жизнедеятельности. Аденозиндифосфат (АДФ) – нуклеотид, образованный аденозоном и двумя остатками фосфорной кислоты. Участвует в энергетическом обмене живых организмов. АДФ получает энергию путем дефосфорилирование фосфоэнолпировиноградной кислоты под действием фермента трансфосфорилазы, которая переносит макроэргическую связь с кислоты на АДФ. Уридиндифосфорная кислота (УДФ) и ее производные принимают участие во взаимопревращении углеводов. В настоящее время известны три пути синтеза АТФ. I. Окислительное фосфорилирование. Это наиболее важный в количественном отношении источник АТФ у аэробных организмов. Свободная энергия, необходимая для образования макроэргической связи АТФ, генерируется в дыхательной цепи. II. Субстратное фосфорилирование – синтез АТФ при взаимодействии АДФ и другого макроэрга (субстрата: S~Ф): S~Ф + АДФ S + АТФ. III.Трансфосфорилирование («путь спасения») - синтез АТФ из двух молекул АДФ: АДФ + АДФ Аденилаткиназа АТФ + АМФ. Экспериментальные данные доказывают, что в условиях патологического разобщения окисления и фосфорилирования снижается функция различных органов (уменьшается выработка антител в условиях экспериментального гипотиреоза, снижается мышечная активность при α-динитрофеноловой интоксикации). Особенно серьезные сдвиги в энергетическом обмене возникают при бактериальной интоксикации. Дифтерийный и стафилококковый токсины, золотистый стафилококк, обладая разобщающим действием, приводят к резкому увеличению фактической продукции тепла. Еще более серьезные изменения энергетического обмена наблюдаются при тяжелых ожогах. Первичным пусковым механизмом этих изменений является уменьшение количества SH-групп белков, сопровождающееся снижением ферментативной активности митохондрий и разобщением окислительного фосфорилирования, что в конечном счете снижает выработку АТФ и ведет к нарушению функции внутренних органов. При ожогах уменьшение количества SH-групп белков связано с ингибированием их недоокисленными продуктами обмена и ожоговыми токсинами. Энергетические процессы в клетке находятся в тесной зависимости не только от концентрации и активности некоторых субстратов (продукты обмена), но и от функционального состояния систем, регулирующих обмен энергии, и в первую очередь нервной и эндокринной систем. Так, теплопродукция может значительно повыситься при эмоциональном возбуждении, в эректильной фазе травматического шока. Основными регуляторами проницаемости митохондрий и, следовательно, энергетического обмена являются гормоны шитовидной железы (тироксин и трийодтиронин). |

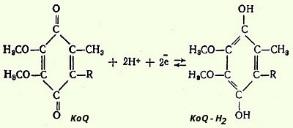 в
первую очередь, коэнзим Q10 является
мощнейшим антиоксидантом, молекулы
Q10 которого используются многократно,
а сам убихинон после окисления постоянно
регенерируется организмом. Вдобавок
вещество восстанавливает окисленный
токоферол, который, в свою очередь,
оберегает мембраны клеток от воздействия
свободных радикалов.Реакции
дегидрирования имеют огромное значение
в ЦТК: отщепляя углерод с веществ и
присоединяя его к НАД и ФАД, образуются
НАДН+Н+ и ФАД∙Н2, которые образуют в
дыхательной цепи АТФ.
в
первую очередь, коэнзим Q10 является
мощнейшим антиоксидантом, молекулы
Q10 которого используются многократно,
а сам убихинон после окисления постоянно
регенерируется организмом. Вдобавок
вещество восстанавливает окисленный
токоферол, который, в свою очередь,
оберегает мембраны клеток от воздействия
свободных радикалов.Реакции
дегидрирования имеют огромное значение
в ЦТК: отщепляя углерод с веществ и
присоединяя его к НАД и ФАД, образуются
НАДН+Н+ и ФАД∙Н2, которые образуют в
дыхательной цепи АТФ.