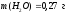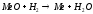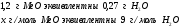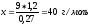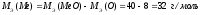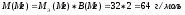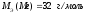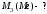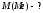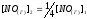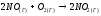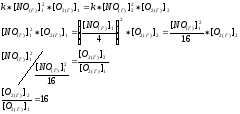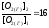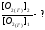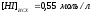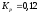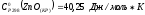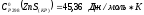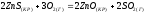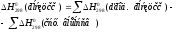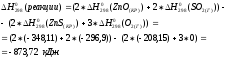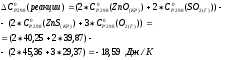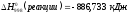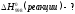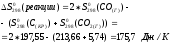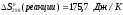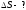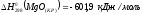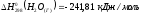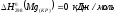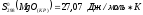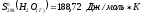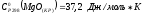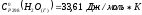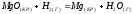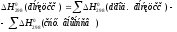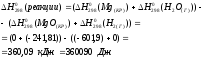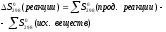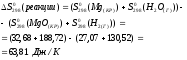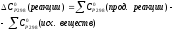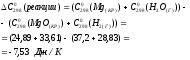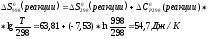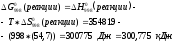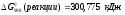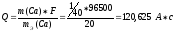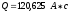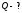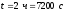химия 4 вариант для ФЗО
.docxЧасть 1
№ 21.
|
Дано:
|
Решение:
Ответ:
|
|
|
№ 124.
|
Дано:
|
Решение:
Ответ:
|
|
|
Константа скорости зависит от природы реагирующих веществ, температуры и от присутствия катализатора.
№ 149.
|
Дано:
|
Решение: 2HI → H2 + I2 - Q Пусть х - [H2]РАВН
Ответ:
|
|
|
Равновесие в данной реакции можно сместить вправо, повысив температуру (принцип Ле Шателье), либо увеличив концентрацию HI. Значение КС при этом увеличится.
№ 274.

№ 299.
Образование комплекса:
2KOH + Zn(OH)2 → K2[Zn(OH)4]
Гидроксид Гидроксид Тетрагидроксоцинкат калия
калия цинка
Первичная диссоциация (по типу сильного электролита):
K2[Zn(OH)4] → 2K+ + [Zn(OH)4]2-
Вторичная диссоциация (по типу слабого электролита):
[Zn(OH)4]2- ↔ [Zn(OH)3]-+ OH-
[Zn(OH)3]- ↔ [Zn(OH)2] + OH-
[Zn(OH)2] ↔ [Zn(OH)]++ OH-
[Zn(OH)]+ ↔ Zn2+ + OH-
|
Дано:
|
Решение:
Ответ:
|
|
|
|
|
|
|
|
|
|
|
|
№ 12.
№ 25.
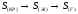
В данной цепочке энтропия возрастает с увеличением движения молекул в веществах.
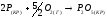
Энтропия уменьшается, т.к. в процессе реакции уменьшается число молей газообразных веществ.
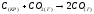
Энтропия увеличивается, т.к. в процессе реакции увеличивается число молей газообразных веществ.
|
Дано:
|
Решение:
Ответ:
|
|
|
№ 43.
|
Дано:
|
Решение:
Т.к.изменение энергии Гиббса больше 0, реакция не может идти самопроизвольно при данных условиях. Ответ:
|
|
|
|
|
|
|
|
|
|
|
|
№ 84
Pb | Pb2+ || H+| H2, Pt
K: Pb2+ + 2e- → Pb0
A: H20 - 2e- → 2H+
Суммарно: H2 + Pb2+ → Pb + 2H+
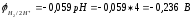
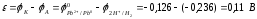
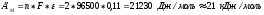
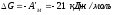
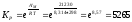
Если оба электрода будут стандартными, то водородный электрод будет катодом, а свинцовый - анодом.
№ 116
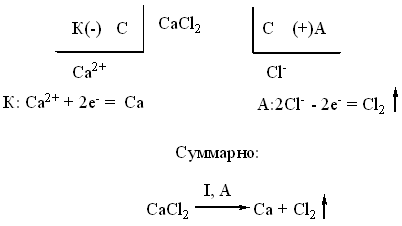
|
Дано:
|
Решение:
Ответ:
|
|
|
№ 128
Хромированное покрытие:
железо выступает в роли катода:
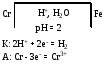
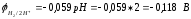
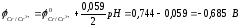
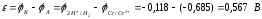
Никелированное покрытие:
железо выступает в роли анода:
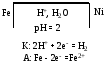
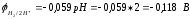
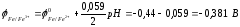
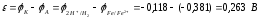
таким образом, хромированное покрытие более надежно, т.к. при его нарушении разрушается само покрытие.
|
Дано:
|
Решение:
Ответ:
|
|
|
№ 147
Схема аккумулятора:
Fe | Fe 2+ || Ni 2+ | Ni
Разрядка:
Fe + 2OH- = Fe(ОН)2 + 2е-
2NiOOH + 2H2O + 2e- = 2Ni(ОН)2 + 2ОН-
Суммарно:
2NiOOH + 2H2O + Fe = 2Ni(OH)2 + Fe (OH)2
Зарядка:
Fe (OH)2 + 2e- = Fe + 2OH-
2Ni(OH)2 + 2OH- = 2NiOOH + 2H2O + 2e-
Суммарно:
2Ni(OH)2 + Fe (OH)2 = 2NiOOH + 2H2O + Fe
железно-никелевые аккумуляторы обычно применяются в экстремальных условиях. Эти аккумуляторы действуют при температурах ниже –40оС Они могут обеспечивать больший ток и более глубокие и частые циклы по сравнению со свинцово-кислотными, AGM и гелевыми аккумуляторами. Срок службы железно-никелевых аккумуляторов может превышать 20 лет. Железно-никелевые аккумуляторы относятся к наиболее экологичным аккумуляторам. К недостаткам аккумуляторов этого типа можно отнести их высокую стоимость и низкий КПД зарядки.