
Химия-03 / himia_1
.pdf
mail to denny@studhelp.info
1
Контрольная работа № 1
108. Определите скорость реакции 2 SO3 (г) = 2 SO2 (г) + O2 (г)
при исходной концентрации SO3, равной 2,8 моль/л, и в момент времени, когда получится 1 моль/л O2. Какова концентрация получившегося SO2? Сформулируйте закон действия масс.
Зависимость скорости реакции от концентраций выражается законом действия масс (ЗДМ). Формулировка ЗДМ: скорость гомогенной реакции при постоянной температуре прямо
пропорциональна произведению концентраций (давлений) реагирующих веществ, fo
возведенных в степень, с показателями, равными стехиометрическим коэффициентам, стоящим в уравнении реакции.
На основании этого запишем выражение для скорости приведенной реакции при исходной
концентрации SO3, равной 2,8 моль/л: |
|
|
|
i |
||||||||||||||
v = k [SO3 ]2 = k ×2.82 |
= 7.84k |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
. |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Согласно уравнению реакции, на образование 1 моль/л O2 затрачивается 2 моль/л SO3, при |
||||||||||||||||||
этом образуется 2 моль/л SO2. |
|
|
|
P |
n |
|||||||||||||
В момент времени, когда получится 1 моль/л O2, концентрация SO3 будет составлять |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L |
|
|
|
2,8 – 2,0 = 0,8 (моль/л). Тогда выражение для скорости реакции имеет вид: |
|
|||||||||||||||||
v = k [SO3 ]2 = k ×0.82 |
= 0.64k |
|
|
|
E |
|
|
|
||||||||||
Ответ: 7.84k ; 0.64k ; 2 моль/л SO2 |
|
|
|
|
||||||||||||||
DH |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
128. При некоторой температуре равновесие в газовой системе 2NO2(г) ↔ 2NO(г)+О2(г) |
||||||||||||||||||
установилось |
при |
|
следующих концентрациях веществ: CNO2 = 0,006 моль/л; CNO = |
|||||||||||||||
0,024 моль/л; |
СО2 = 0,012 |
2 |
моль/л. Определите константу равновесия (КС) и исходную |
|||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
U |
|
|
|
|
|
||
концентрацию NO2. Как нужно изменить давление и концентрации веществ, чтобы довести |
||||||||||||||||||
реакцию до конца? |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Запишем выражение для константы равновесия приведенной реакции и найдем Kc |
||||||||||||||||||
K = |
[NO] |
[O2 ] |
; K |
|
= |
0.024 |
|
×0.012 |
= 0.192 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
c |
|
|
2 |
. |
|
|
2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
c |
|
|
|
|
|
|
|
|
|
|
|||
|
|
[NO2 ] |
|
|
|
|
|
|
0.006T |
|
|
|
концентрации [NO2 ] и |
|||||
Начальная |
w |
|
|
|
|
NO2 равна сумме равновесной |
||||||||||||
концентрация |
|
|||||||||||||||||
концентрации NO2, Sпошедшей на образование продуктов реакции. Согласно уравнению |
||||||||||||||||||
реакции, концентрации разложившегося NO2 и образовавшегося при этом NO равны, |
||||||||||||||||||
|
w |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
следовательно, Снач(NO2) = 0,006 + 0,024 = 0,030 (моль/л) |
|
|
|
|
||||||||||||||
Согласно принципу Ле-Шателье: если на систему, находящуюся в равновесии, оказывается wвнешнее воздействие, то оно благоприятствует реакции, ослабляющей это воздействие.
Таким образом, чтобы довести реакцию до конца можно уменьшать концентрацию продуктов реакции либо уменьшая давление. Тогда равновесие будет смещаться в сторону образования большего числа молей газообразных веществ, т.е. в сторону прямой реакции.
Ответ: 0,192; 0,030 моль/л
www.studhelp.info

mail to denny@studhelp.info
2
158. Рассчитайте молярность и нормальность 2,5%-го раствора NaOH ( ρ = 1,03 г/см3 )
Примем массу раствора NaOH равной 100 г. Тогда масса гидроксида натрия в 2,5%-м
растворе NaOH равна m |
|
= 100×2.5% = 2.5 (г). Количество вещества, содержащееся в 2.5 г |
|||||||||||||
|
|
|
|
|
|
NaOH |
|
100% |
|
|
|
|
|||
|
|
|
|
|
|
|
|
m |
|
|
|
|
|||
NaOH, следующее: nNaOH = |
|
= |
2.5 |
= 0.0625 (моль). |
|
|
|
|
|||||||
M |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|||
Объем 100 г раствора рассчитаем, зная плотность раствора: |
|
|
|
|
|||||||||||
V = m |
= 100 |
= 97.09 (см3) или 0.097 дм3 |
|
|
|
|
|||||||||
ρ |
1.03 |
|
|
|
|
|
|
|
|
|
|
||||
Молярность раствора NaOH равна |
|
|
|
|
n |
||||||||||
cNaOH = |
n |
= |
0.0625 |
= 0.644 (моль/дм3) |
|
|
|
||||||||
|
|
i |
|||||||||||||
|
|
|
|
||||||||||||
|
V |
0.097 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
. |
||||||
Поскольку для NaOH эквивалентная масса вещества равна мольной массе, то нормальнаяfo |
|||||||||||||||
концентрация раствора равна молярной концентрации (0.644 н) |
P |
|
|||||||||||||
|
|
|
|||||||||||||
Ответ: 0.644 моль/л; 0.644 н |
|
|
|
L |
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||
178. Определите концентрацию и количество ионов в 0,02 н растворе Na2CO3 (α = 1). Запишите уравнение диссоциации.
Na2CO3 → 2 Na+ + CO32– |
E |
Поскольку степень диссоциации Na2CO3 α = 1, то данная соль диссоциирует полностью с образованием двух ионов натрия и одного карбонат-иона:
Концентрация ионов в сильных электролитах определяется по формуле
C± = CM α ×n
где n – число ионов, на которые распадаетсяU одна молекула.
Фактор эквивалентности для Na2CO3 равен 1/2 (эквивалент равен 2), следовательно,
молярная концентрация Na2CO3 |
составляет 0,02 н / 2 = 0,01 моль/л |
||||||||||||||||
Концентрация ионов Na+ |
T |
DH |
|
||||||||||||||
и CO32– равны: |
|
||||||||||||||||
CNa+ |
= 0.01×1×2 = 0.02 (моль/л) |
|
|
|
|
|
|
|
|
|
|
|
3 |
||||
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|||
CCO2− = 0.01×1×1 = 0.01(моль/л) |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
3 |
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ответ: 0,02 моль/л; 0,01 моль/л |
|
|
|
|
|
|
|
|
|
|
|||||||
223. Определите рН 0,2%-го раствора плавиковой кислоты HF (ρ = 1 г/см ), если степень ее |
|||||||||||||||||
диссоциации равна 2%. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
w |
w |
|
|
|
|
|
|
|
|
|
|
|
100×0.2% |
= 0.2 (г). Количество вещества, |
|||
Масса HF в 100 г 0.2%-го раствора HF равна mHF = |
100% |
||||||||||||||||
содержащеесяw в 0.2 г HF |
|
|
|
m |
|
0.2 |
|
|
|
|
|
||||||
n |
|
= |
= |
|
= 0.01(моль). Учитывая, что ρ = 1 г/см3, рассчитаем |
||||||||||||
|
|
|
|||||||||||||||
|
|
|
|
HF |
|
M |
20 |
|
|
|
|
|
|
|
|
||
объем 100 г раствора: V = m |
|
|
|
|
|
|
|
|
|
|
|||||||
= 100 |
=100 |
|
(см3) или 0.1 дм3 |
|
|||||||||||||
|
|
|
|
ρ |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
Молярная концентрация раствора HF равна c = |
n |
|
= |
0.01 |
= 0.1(моль/дм3) |
||||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
HF |
V |
0.1 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Концентрация ионов водорода при степени диссоциации кислоты 2% (0.02) равна |
|||||||||||||||||
CH + |
= 0.1×0.02×1 = 0.002 (моль/л). |
|
|
|
|
|
|
|
|
|
|
||||||
www.studhelp.info
mail to denny@studhelp.info
3
Тогда рН = –lg[Н+] = –lg 0.002 = 2.7
Ответ: 2.7
248. В молекулярной и краткой ионной формах запишите уравнения реакций получения и гидролиза соли HCOONa и рассчитайте рН раствора, в 1 л которого содержится 0,68 г этой соли.
Реакция получения соли: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
fo |
|
|||||
HCOOН + NaОН = HCOONa + Н2О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
HCOOН + ОН– = HCOO– + Н2О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Гидролиз соли: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HCOONa + Н2О ↔ HCOOН + NaОН |
|
|
|
|
|
|
|
|
|
|
|
|
i |
|
|
|||||||||||||||
HCOO– + Н2О ↔ HCOOН + ОН– |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
0.68 |
|
|
|
|
|
|
|
|
|
||||
Концентрация HCOONa равна C = |
|
|
= |
= 0.01(моль/л) |
|
|
n |
|
||||||||||||||||||||||
|
|
|
|
68 |
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
M ×V |
|
|
|
|
L |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Концентрация ионов водорода при гидролизе определяется по формуле CH + = C ×h , где h |
– |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
E |
P |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
степень гидролиза, h = |
KГ |
. Константа гидролиза K |
Г = |
Kw |
|
|
|
|
||||||||||||||||||||||
Kдисс |
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Таким образом, C |
|
= C × |
|
KГ |
= |
|
|
|
|
= |
|
Kw |
×С |
|
|
|
|
|
|
|
|
|
||||||||
H + |
|
|
K |
Г |
×С |
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
Kдисс |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Константа диссоциации муравьиной кислоты Kдисс =1.8×10−4 . |
|
|
|
|
|
|||||||||||||||||||||||||
Тогда CH + = |
10−14 ×0.01 |
|
|
|
10−12 |
U |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
1.8×10−4 = |
|
|
1.8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
= 0.75×10−6 , рН = = –lg [Н+] = –lg 0.75×10−6 = 6.12 |
|
|
||||||||||||||||||||||||||
Ответ: 6.12 |
|
|
|
|
|
|
T |
|
|
|
DH |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
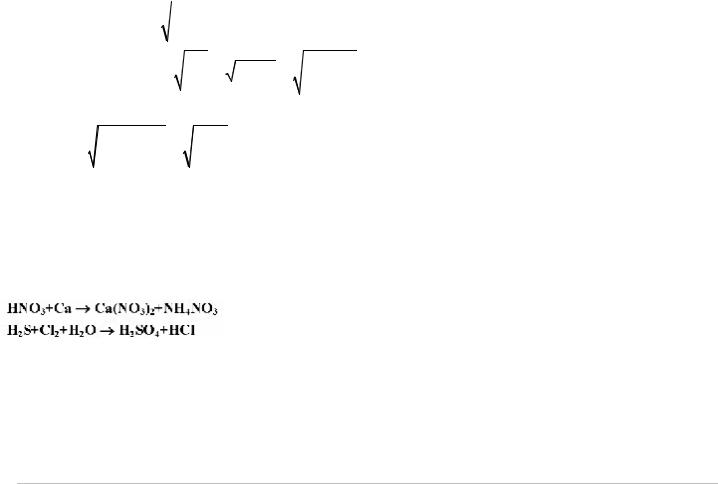
263. На основании электронно–ионных схем составьте полные молекулярные уравнения |
||||||||
|
|
S |
|
|
|
|
|
|
окислительно–восстановительных реакций, установив восстановитель, окислитель и |
||||||||
|
. |
|
|
|
|
|
|
|
процессы окисления и восстановления. |
|
|
|
|
|
|||
|
w |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
w |
|
|
10Н+ + NО3– + 8 е → NН4+ + 3Н2О |
|
|
1 |
||
1) окислитель (восстановление) |
|
|
||||||
w |
восстановитель (окисление) |
Ca – 2 e → Ca2+ |
|
|
4 |
|||
|
|
|
4 Ca + 10Н+ + NО3– → 4 Ca+2 + NН4+ + 3Н2О |
|
|
|
||
|
|
10 HNO3 + 4 Ca → 4 Ca(NO3)2 + NH4NO3 + 3Н2О |
|
|||||
2) окислитель (восстановление) |
Сl2 + 2 е → 2 Cl– |
|
|
4 |
||||
|
восстановитель (окисление) |
4 H2O + H2S – 8 e → 10 H+ + SO42– |
|
|
1 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
4 H2O + H2S +4 Сl2 → 8 Cl– + 10 H+ + |
SO42– |
|
|
|
|
|
|
|
|
|
||||
|
|
|
4 H2O + H2S +4 Сl2 → 8 HCl + H2SO4 |
|
||||
www.studhelp.info
