
ОПРЕДЕЛЕНИЕ ЖЕСТКОСТИ ВОДЫ В ПРИРОДНО-ПОВЕРХНОСТНЫХ КОМПЛЕКСАХ КОМПЛЕКСОНОМЕТРИЧЕСКИМ МЕТОДОМ
.pdf
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное автономное образовательное учреждение высшего образования
«САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ АЭРОКОСМИЧЕСКОГО ПРИБОРОСТРОЕНИЯ»
КАФЕДРА 31
КУРСОВАЯ РАБОТА (ПРОЕКТ) ЗАЩИЩЕНА С ОЦЕНКОЙ
РУКОВОДИТЕЛЬ
доц., канд. хим. наук. доц. |
подпись, дата |
инициалы, фамилия |
должность, уч. степень, звание |
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА К КУРСОВОЙ РАБОТЕ
ОПРЕДЕЛЕНИЕ ЖЕСТКОСТИ ВОДЫ В ПРИРОДНО-ПОВЕРХНОСТНЫХ КОМПЛЕКСАХ КОМПЛЕКСОНОМЕТРИЧЕСКИМ МЕТОДОМ
по дисциплине: ХИМИЯ
vk.com/id446425943
РАБОТУ ВЫПОЛНИЛ |
|
vk.com/club152685050 |
|||
СТУДЕНТ ГР. № |
|
||||
|
|
|
|
||
|
|
|
подпись, дата |
|
инициалы, фамилия |
Санкт-Петербург 2018
СОДЕРЖАНИЕ:
ВВЕДЕНИЕ 1. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
1.1Теоретические основы комплексонометрического метода
1.2Методика определения жесткости воды
1.3Отбор проб
1.4Реактивы и оборудование
1.5Выполнение определения 2. ЭКСПЕРЕМЕНТАЛЬНАЯ ЧАСТЬ 2.1 Обработка результатов
vk.com/club152685050
vk.com/id446425943
ВВЕДЕНИЕ
Вода́(оксид водорода) — химическое вещество в виде прозрачной жидкости, не имеющей цвета (в малом объёме), запаха и вкуса (при нормальных условиях). Химическая формула: Н2O. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, лёд на полюсах).
Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы).
Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды.
Вода на Земле может существовать в трёх основных состояниях — жидком, газообразном и твёрдом и приобретать различные формы, которые могут одновременно соседствовать друг с другом. Водяной пар и облака в небе, морская вода и айсберги, горные ледники и горные реки, водоносные слои в земле. Вода способна растворять в себе много веществ, приобретая тот или иной вкус. Из-за важности воды, «как источника жизни», её нередко
подразделяют на типы по различным принципам. vk.com/club152685050 vk.com/id446425943
В последние несколько десятилетий крупномасштабный характер приняло загрязнение атмосферы. Загрязнение постоянно наносит ущерб водохранилищам, рекам, озерам, морям. Рано или поздно различными путями загрязнение из атмосферы проникает в почву. Из атмосферы загрязнения (тепловые, физические, химические, биологические) проникают в почву, и ведет к ухудшению качества и изменению состава подземных вод.
К подземным водам также относятся артезианские и ключевые воды. Артезианская вода, как правило, находится в глубоких слоях, залегающими
между двумя не подверженными проникновению воды грунтами. Такие воды также называют напорными, так как при наличии большого давления вода из таких скважин бьет фонтаном.
Некоторые виды грунтовых вод находят выход на поверхность. Их называют ключевыми. Ключи могут появляться из нижних слоев и в
результате обнажения пластов.
vk.com/club152685050
vk.com/id446425943
1. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
1.1Теоретические основы комплексонометрического метода
Воснове метода комплексонометрии лежит образование комплексных соединений анализируемых катионов с органическими реагентами - комплексонами.
Вкомплексонометрическом анализе в качестве рабочего вещества чаще всего используют трилон Б.
Трилон Б |
vk.com/club152685050 |
|
NaООССНООССН2 СН2СООН |
||
vk.com/id446425943 |
||
N-СН2-СН2-N |
|
|
НООССН2 СН2СООNaООССН |
|
С6Н12N2(СООН)2(СООNа)2 ·2Н2О
Трилоном Б называется двузамещенная натриевая соль органической этилендиаминотетрауксусной кислоты.
Трилон Б - это фирменное название вещества; его называют также хелатон, версен, комплексон III.
Сокращенное обозначение молекулы трилона Б: NaООССН2Н2Тр.
Это соединение легко образует прочные внутрикомплексные соли со многими катионами. Соли образуются, с одной стороны, за счет замещения металлом водорода карбоксильных групп, с другой - за счет образования координационных связей между ионами металла и атомами азота.
При комплексонометрическом титровании к раствору, содержащему определяемые ионы, добавляют постепенно титрованный раствор комплексона. По мере титрования определяемые ионы связываются в комплекс, и в точке эквивалентности они практически отсутствуют в растворе. Реакцию в общем виде можно записать так:
Mg2+ + NaООССН2H2Tp = NaООССН2MgTp + 2H+
vk.com/club152685050
vk.com/id446425943
Чтобы реакция комплексообразования шла до конца, нужно связать выделяющиеся ионы водорода. Поэтому при титровании к анализируемому раствору добавляют смесь хлорида и гидроксида аммония - аммиачнобуферный раствор.
Для определения момента окончания титрования служат индикаторы - вещества, образующие окрашенные соединения с ионами кальция и магния или с одним из этих катионов. Такими индикаторами являются кислотный хром синий К, дающий переход от розовой к серо-голубой окраске при рН=10-11; магнезон и эриохром черный Т, называемый также хромом черным специальным ЕТ00, изменяющие окраску от вино-красной к синей; мурексид и др.
Индикаторы обладают различной чувствительностью, т.е. их окрашенные соединения с ионами кальция и магния возникают при различных, но определенных для данного индикатора и для выбранных условий концентрациях этих ионов
Устойчивость комплекса существенно зависит от рН раствора. Поэтому комплексонометрическое титрование ведут в заданном интервале рН, используя различные буферные растворы.
Методом комплексонометрии можно определить катионы магния, кальция, цинка, алюминия, бария, свинца и многие другие - более 40 различных катионов. Этот метод широко применяется для определения жесткости воды.
vk.com/club152685050
vk.com/id446425943
1.2 Методика определения жесткости воды
При определении жесткости по методу А подкисление проводят соляной кислотой, по методу Б — соляной или азотной кислотой, при использовании метода В — азотной кислотой. Контроль pH проводят по универсальной индикаторной бумаге или с использованием pH-метра. Срок хранения подкисленной пробы воды — не более 1 мес. Для воды, расфасованной в емкости, сроки и температурные условия хранения должны соответствовать требованиям, указанным в нормативной документации* на готовую продукцию.
1. Установление коэффициента поправки к концентрации раствора трилона Б
В коническую колбу вместимостью 250 см3 вносят 10,0 см3 раствора ионов магния, добавляют 90 см3 бидистиллированной воды, 5 см3 буферного раствора, от 5 до 7 капель раствора индикатора или от 0,05 до 0,1 г сухой смеси индикатора и сразу титруют раствором трилона Б до изменения окраски в эквивалентной точке от винно-красной (красно-фиолетовой) до синей (с зеленоватым оттенком) при использовании индикатора эриохром черный Т, а при использовании индикатора хромовый темно-синий кислотный до синей (сине-фиолетовой).
Раствор трилона Б в начале титрования добавляют довольно быстро при постоянном перемешивании. Затем, когда цвет раствора начинает меняться, раствор трилона Б добавляют медленно. Эквивалентной точки достигают при изменении окрашивания, когда цвет раствора перестает меняться при добавлении капель раствора трилона Б.
Титрование проводят на фоне титрованной контрольной пробы. В качестве контрольной пробы можно использовать немного перетитрованную анализируемую пробу. За результат принимают среднеарифметическое
vk.com/club152685050
vk.com/id446425943
значение результатов не менее двухопределений. Значение коэффициента поправки должно быть равным 1,00 + 0,03.
Коэффициент поправки К к концентрации раствора трилона Б рассчитывают по формуле
 ,
,
где V — объем раствора трилона Б, израсходованный на титрование, см3, 10 — объем раствора ионов магния, см3.
Жесткость воды Ж, °Ж, рассчитывают по формуле:
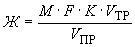 , где М — коэффициент пересчета, равный 2Стр,
, где М — коэффициент пересчета, равный 2Стр,
где Стр — концентрация раствора трилона Б, моль/м3 (ммоль/дм3), (как правило М = 50);
F — множитель разбавления исходной пробы воды при консервировании (как правило F = 1);
К — коэффициент поправки к концентрации раствора трилона Б; Утр — объем раствора трилона Б, израсходованный на титрование, см3; Vпр — объем пробы воды, взятой для анализа, см3.
За результат измерения принимают среднеарифметическое значение результатов двух определений. Приемлемость результатов определений оценивают исходя из условия:
|
│Ж1-Ж2│≤ r |
где г— предел повторяемости; |
vk.com/club152685050 |
Ж1 и Ж2 — результаты определений, °Ж. |
vk.com/id446425943 |
|
Если расхождение между двумя результатами превышает установленное значение, то определение жесткости воды повторяют
2. Контроль показателей качества результатов измерений
Контроль показателей качества результатов измерений в лаборатории предусматривает проведение контроля стабильности результатов измерений с учетом требований с применением ГСО или раствора ГСО состава жесткости воды, в наибольшей степени отражающего значение жесткости анализируемых в лаборатории вод.
Оформление результатов Результаты измерений регистрируют в протоколе (отчете) по ГОСТ
ИСО/МЭК 17025. В протоколе указывают применяемый в лаборатории метод по настоящему стандарту. Результат измерений может быть представлен в виде:
(Ж ± ), где Ж — значение жесткости воды, °Ж;
— границы интервала, в котором погрешность определения жесткости воды находится с доверительной вероятностью Р= 0,95
vk.com/club152685050
vk.com/id446425943
1.3Отбор проб
1.Общие требования к отбору проб — по ГОСТ 31861, ГОСТ 31862 и ГОСТ 17.1.5.05.
Пробу отбирают объемом не менее 400 см3 для анализа по методу А и не менее 200 см3 для анализа по методам Б и В в емкость, изготовленную из полимерных материалов или стекла. Срок хранения пробы воды — не более 24 ч. Для увеличения срока хранения пробы и для предотвращения осаждения из воды карбонатов кальция (что характерно для подземных или бутилированных вод) пробу подкисляют кислотой до pH < 2.
2.1. Программа отбора проб должна быть составлена в соответствии с целью последующего определения химического состава и физических
свойств воды и предусматривать: |
vk.com/club152685050 |
|
перечень определяемых компонентов; |
||
vk.com/id446425943 |
требования к месту отбора проб; периодичность и частоту отбора проб, а также, при необходимости,
статистическую обработку данных по отбору проб с целью выявления оптимальных величин периодичности и частоты отбора проб.
Место, периодичность и частоту отбора проб устанавливают в соответствии с требованиями ГОСТ 2761-84, ГОСТ 17.1.3.07-82*, ГОСТ 17.1.3.08-82 и ГОСТ 17.1.5.02-80.
Статистическую обработку данных по отбору проб выполняют при необходимости.
2.2. Требования к приборам и устройствам для отбора, первичной обработки и хранения проб - по ГОСТ 17.1.5.04-81.
