
- •Министерство образования рф
- •Строение атомов
- •Периодическая система элементов д. И. Менделеева
- •Химическая связь и строение молекул. Конденсированное состояние вещества
- •Стандартные теплоты (энтальпии) образования некоторых веществ
- •Химическое сродство4
- •Стандартные изобарные потенциалы образования некоторых веществ
- •Стандартные абсолютные энтропии некоторых веществ
- •Химическая кинетика и равновесие
- •Способы выражения концентрации раствора
- •Свойства растворов
- •Ионные реакции обмена5
- •Гидролиз солей
- •Контрольное задание 2 Окислительно-восстановительные реакции
- •Электродные потенциалы и электродвижущие силы*6
- •Стандартные электродные потенциалы е° некоторых металлов (ряд напряжений)
- •Электролиз
- •Коррозия металлов7
- •Комплексные соединения
- •Жесткость воды и методы ее устранения
- •Органические соединения. Полимеры
- •Приложение
- •Наименование наиболее важных кислот и их солей
- •Константы диссоциации и степени диссоциации некоторых слабых электролитов
Приложение
Таблица 5
Наименование наиболее важных кислот и их солей
|
|
Название кислоты |
Формула |
Общее название солей |
Примеры названий отдельных солей |
|---|---|---|---|---|
|
|
Азотистая |
HNO2 |
Нитриты |
Нитрит калия |
|
|
Азотная Бромоводородная |
НNO3 НВг |
Нитраты Бромиды |
Нитрат калия Бромид калия |
|
|
Двухромовая |
Н2Сг2О7 |
Дихроматы |
Дихромат калия |
|
|
Иодоводородная |
HI |
Иодиды |
Иодид калия |
|
|
Кремниевая метакислота |
H2SiO3 |
Метасиликаты |
Метасиликат калия |
|
|
Марганцовая |
HMnO4 |
Перманганаты |
Перманганат калия |
|
|
Сернистая Сероводородная |
H2SO3 H2S |
Сульфиты Сульфиды |
Сульфит натрия Сульфид аммония |
|
|
Серная |
H2SO4 |
Сульфаты |
Сульфат меди |
|
|
Соляная |
HCl |
Хлориды |
Хлорид натрия |
|
|
Угольная Уксусная |
H2CO3 CH3COOH |
Карбонаты Ацетаты |
Карбонат натрия Ацетат натрия |
|
Фосфорная ортокислота Фтороводородная Хлорноватистая Хлорноватая Хлорная Хромовая Синильная или циано-водородная |
Н3РO4
НF
HClO
HClO3 HClO4 H2CrO4 HCN |
Ортофосфаты
Фториды
Гипохлориты
Хлораты Перхлораты Хроматы Цианиды |
Ортофосфат калия
Фторид кальция
Гипохлорит натрия
Хлорат калия Перхлорат калия Хромат калия Цианид калия | |
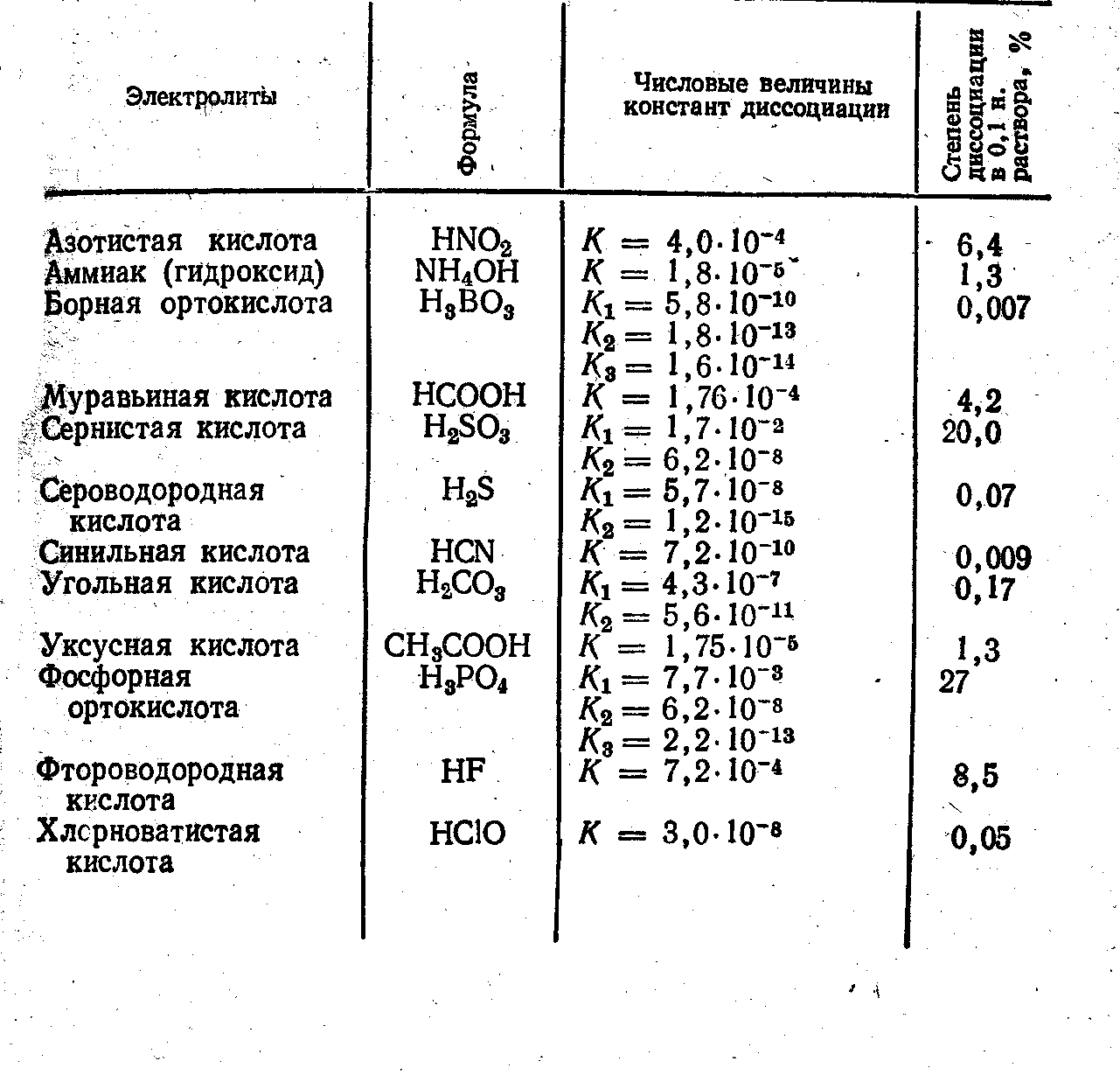
Таблица 6
Константы диссоциации и степени диссоциации некоторых слабых электролитов

1Нормальные условия: 760 мм рт. ст.= 1 атм, или по системе СИ 1,013105Па, 273 К. или 00С.
2В химической литературе понятия атомный вес и молекулярный вес выражают и аналогичными терминами; относительная атомная масса и относительная молекулярная масса.
3При решении задач этого раздела см. табл. 1.
4При решении задач этого раздела см. табл. 1–3.
5При решении задач этого раздела см. табл. 6 и 7.
6При решении задач этого раздела см. табл. 4.
7При решении задач этого раздела см. табл. 4.
8Общая электронная формула, гдеп - главное квантовоечисло.
9Общая электронная формула, гдеп – главное квантовоечисло.
10Общая электронная формула, где n – главное квантовое число.
