
книги / Химия. Классы неорганических соединений
.pdfМинистерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования
«Пермский национальный исследовательский политехнический университет»
Кафедра химии и биотехнологии
Х И М И Я
КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Методические указания
Издательство Пермского национального исследовательского
политехнического университета
2018
Составители: Т.С. Соколова, Г.А. Старкова
УДК 541.1 Х46
Рецензент
канд. хим. наук, доцент Л.С. Пан (Пермский национальный исследовательский политехнический университет)
Химия. Классы неорганических соединений : метод. укаХ46 зания / сост. Т.С. Соколова, Г.А. Старкова. – Пермь : Изд-во
Перм. нац. исслед. политехн. ун-та, 2018. – 31 с.
Рассмотрены важнейшие классы неорганических соединений: их состав, номенклатура, химические свойства. Приведены типовые задания для самостоятельной работы и примеры их решений.
Предназначено для самостоятельной работы студентов нехимических направлений, изучающих дисциплину «Химия».
УДК 541.1
© ПНИПУ, 2018
2
|
ОГЛАВЛЕНИЕ |
|
1. |
СТЕПЕНЬ ОКИСЛЕНИЯ ЭЛЕМЕНТОВ.......................................... |
4 |
2. |
КЛАССИФИКАЦИЯ И СВОЙСТВА НЕОРГАНИЧЕСКИХ |
|
СОЕДИНЕНИЙ........................................................................................ |
6 |
|
|
2.1. Оксиды .......................................................................................... |
7 |
|
2.2. Основания..................................................................................... |
9 |
|
2.3. Кислоты....................................................................................... |
11 |
|
2.4. Соли............................................................................................. |
15 |
3. |
РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ....................................................... |
19 |
4. |
ЗАДАНИЯ ДЛЯ САМОКОНТРОЛЯ............................................... |
23 |
5. |
ТЕСТОВОЕ ЗАДАНИЕ..................................................................... |
25 |
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ................................ |
27 |
|
ПРИЛОЖЕНИЕ 1 .................................................................................. |
28 |
|
ПРИЛОЖЕНИЕ 2 .................................................................................. |
30 |
|
3
1. СТЕПЕНЬ ОКИСЛЕНИЯ ЭЛЕМЕНТОВ
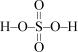
Неорганические соединения являются сложными веществами и состоят из атомов различных элементов. Для каждого соединения существует своя химическая формула, представляющая набор символов элементов с численными индексами. Различают химические (молекулярные) и графические формулы. Химическая формула отражает качественный и количественный состав соединения, а в графической формуле с помощью валентных штрихов указывается последовательность соединения атомов и число химических связей между атомами. На рис. 1 приведены примеры формул оксида углерода (IV) и серной кислоты.
СО2 О=С=О
Н2SО4
аб
Рис. 1. Формулы: а – химическая; б – графическая
Составление химических формул соединений основано на использовании понятия степени окисления элемента.
При образовании химических связей между атомами, как правило, происходит смещение общей пары электронов к одному из атомов. Поскольку электрон является заряженной частицей, то смещение электронов приводит к появлению зарядов на атомах. Атом, к которому смещена общая электронная пара, приобретает отрицательный заряд; другой атом, от которого оттянута общая электронная пара, приобретает положительный заряд. При значительном смещении общей пары электронов к одному из атомов происходит практически полная передача электронов и образование ионов.
Реальные заряды ионов могут иметь дробные значения. Однако в большинстве случаев для удобства расчетов принято приписывать
4
атомам условный целочисленный заряд, который называют степенью окисления. Степень окисления записывают над элементом, обозначают арабской цифрой и перед ней указывают знак заряда. Так, в молекуле аммиака NH3 степени окисления водорода +1 и азота –3 записываются в следующем виде:
–3 +1
NH3.
Большинство элементов периодической системы проявляют в соединениях переменные степени окисления, которые можно определить по следующим правилам:
1. Степень окисления элементов в простом веществе равна нулю:
00
Cl2, Zn.
2. В соединениях степень окисления фтора равна –1, кислорода –2 (кроме –1Fe+22O), водорода +1 (кроме гидридов металлов,
+1 –1
например NaH).
3.Степени окисления щелочных (Li, Na, K, Rb, Cs, Fr) и щелоч- но-земельных (Ca, Sr, Ba, Ra) элементов в соединениях равны +1
и+2 соответственно.
4.В бинарных ионных соединениях степень окисления элементов совпадает с зарядом ионов:
+1 –1 +4 –1
NaBr, TiCl4.
5. В ковалентных соединениях степень окисления определяется числом общих электронных пар, которые атом элемента образует с атомами других элементов. Отрицательный заряд приписывают атому, к которому смещена общая электронная пара, а положительный заряд – атому, от которого оттянута общая электронная пара, например:
+1 –2 +3 –1
H2S, BF3.
6. В химическом соединении выполняется условие электронейтральности молекулы: алгебраическая сумма степеней окисления
5
всех атомов с учетом их количества равна нулю. Это правило дает возможность определять степень окисления элементов в сложных химических соединениях.
Определим, например, степень окисления фосфора в фосфате кальция Ca3(PO4)2. Учитывая степени окисления кальция +2 и кислорода –2, можно записать условие электронейтральности молекулы:
(+2) 3 + x 2 + (–2) 4 2 = 0,
где x – степень окисления фосфора. Из уравнения получим: х = 5. Тогда степень окисления всех элементов в соединении можно записать так:
+2 +5 –2
Ca3(PO4)2.
Необходимо помнить, что степень окисления является формальной величиной и реальные эффективные заряды на атомах не всегда соответствуют степени окисления.
В отличие от степени окисления заряды ионов принято обозначать арабской цифрой с указанием знака заряда после цифры, например Fe3+, Fe(OH)2+, HCO3–, SO42–, PO43–. С участием ионов составляются ионные уравнения реакций.
2. КЛАССИФИКАЦИЯ И СВОЙСТВА НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
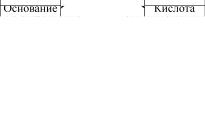
Рис. 2. Схема генетической связи между классами неорганических соединений
По составу все неорганические соединения делят на четыре класса: оксиды, основания, кислоты и соли.
Между классами неорганических соединений существует генетическая связь (рис. 2), которая основана на получении веществ одного класса из веществ другого класса.
6
2.1. Оксиды
Оксиды – химические соединения, образованные из атомов двух элементов, одним из которых является кислород.
По химическим свойствам оксиды могут быть солеобразующие
инесолеобразующие. Несолеобразующие оксиды в химических ре-
акциях солей не образуют, например NO, N2O, CO. Солеобразующие оксиды, в свою очередь, делят на три группы: кислотные, основные
иамфотерные.
Кислотным оксидам соответствуют кислоты. Кислотные оксиды образуют неметаллы, а также некоторые металлы в высшей степени окисления. Кислотными оксидами являются B2O3, CO2, SiO2,
N2O3, N2O5, P2O3, P2O5, As2O5, SO2, SO3, SeO3, CrO3, Cl2O7, I2O7, Mn2O7 и другие.
Большинство кислотных оксидов взаимодействуют с водой с образованием кислот, например:
P2O5 + 3H2O = 2H3PO4.
При взаимодействии кислотных оксидов с основными гидроксидами образуются соль и вода:
SO2 + 2NaOH = Na2SO3 + H2O.
Основным оксидам соответствуют основания. Основные оксиды образуют щелочные и щелочно-земельные металлы, а также некоторые другие металлы, как правило, с низшими степенями окисления. Основными оксидами являются Li2O, Cs2O, CaO, BaO, Cu2O, MgO, FeO, CoO, NiO, MnO, VO, V2O3, Bi2O3.
Оксиды щелочных и щелочно-земельных металлов взаимодействуют с водой с образованием растворимых в воде гидроксидов, то есть щелочей, например:
Na2O + H2O = 2NaOH.
Оксиды других металлов в воде не растворяются.
Основные оксиды взаимодействуют с кислотами, образуя соль и воду:
7
MgO + H2SO4 = MgSO4 + H2O.
Кислотные и основные оксиды взаимодействуют между собой с образованием солей:
MgO + SO2 = MgSO3.
Амфотерным оксидам соответствуют амфотерные гидроксиды. Амфотерные оксиды, как правило, образуют металлы с промежуточными степенями окисления. Амфотерными оксидами являются
BeO, ZnO, SnO, PbO, Al2O3, Ga2O3, In2O3, Sb2O3, Cr2O3, GeO2, SnO2, PbO2, TiO2, ZrO2, MnO2.
В химических реакциях амфотерные оксиды проявляют свойства и кислотных, и основных оксидов. Амфотерные оксиды взаимодействуют с кислотой и щелочью, образуя соль и воду. Так, в расплаве щелочи оксид цинка образует цинкат натрия:
ZnO + 2NaOH = Na2ZnO2 + H2O,
а в растворе серной кислоты образуется сульфат цинка: ZnO + H2SO4 = ZnSO4 + H2O.
Получение оксидов
Оксиды получают непосредственным окислением простых веществ:
4Na+ O2 = 2Na2O,
или разложением солей, гидроксидов, иногда кислот при их нагревании:
CaCO3 = CaO + CO2,
2Fe(OH)3 = Fe2O3 + 3H2O,
H2SiO3 = SiO2 + H2O.
Номенклатура оксидов
При составлении названия оксидов к слову «оксид» добавляют название элемента в родительном падеже. Если элемент имеет не-
8
сколько степеней окисления, то в скобках римской цифрой указывают степень окисления элемента, например: ZnO – оксид цинка, SO3 – оксид серы (VI), Mn2O7 – оксид марганца (VII).
Составление формул оксидов
Формулы оксидов составляют по их названию из условия электронейтральности молекулы: алгебраическая сумма степеней окисления атомов в молекуле (с учетом количества атомов) равна нулю.
В качестве примера составим формулу оксида алюминия. Алюминий находится в IIIА группе периодической системы и имеет постоянную степень окисления +3. Степень окисления кислорода равна –2. Положительный заряд двух атомов алюминия ((+3) 2 = +6) можно компенсировать отрицательным зарядом трех атомов кислорода ((–2) 3 = –6). Таким образом, формула оксида алюминия будет
Al2O3.
2.2. Основания
Основания – химические соединения, молекулы которых состоят из ионов металла и гидроксид-ионов. Количество гидроксидионов в основании обычно не превышает четырех, например, в гидроксиде титана (IV) Ti(OH)4 их четыре. Основания также называют гидроксидами.
Гидроксиды, растворимые в воде, называют щелочами. Щелочи образуют щелочные и щелочно-земельные металлы.
Щелочи взаимодействуют с солями с образованием малорастворимых соединений, например:
Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH,
6NaOH + Fe2(SO4)3 = 2Fe(OH)3↓ + 3Na2SO4.
По химическим свойствам гидроксиды бывают основные и амфотерные. Основные гидроксиды взаимодействуют с кислотными оксидами:
9
Ca(OH)2 + CO2 = CaCO3↓ + H2O,
и с кислотами:
Ca(OH)2 + 2HCl = CaCl2 + 2H2O.
Амфотерные гидроксиды аналогично основным взаимодействуют с кислотными оксидами и с кислотами. Кроме того, они растворяются в избытке щелочей с образованием солей. Так, в расплаве амфотерный гидроксид цинка образует цинкат натрия:
Zn(OH)2 + 2NaOH = Na2ZnO2 + 2H2O,
а в растворе – комплексное соединение тетрагидроксоцинкат натрия: Zn(OH)2 + 2NaOH = Na2Zn(OH)4.
Получение оснований
Щелочи получают растворением в воде металлов и их оксидов: Ca + 2H2O = Ca(OH)2 + H2,
CaO + H2O = Ca(OH)2.
Малорастворимые в воде гидроксиды получают по реакциям обмена, например:
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4.
Здесь образование гидроксида происходит в результате обмена ионами в растворе, как это показывают ионные уравнения (полное и сокращенное):
Cu2+ + SO42– + 2Na+ + 2OH– = Cu(OH)2↓ + 2Na+ + SO42– Cu2+ +2OH– = Cu(OH)2↓.
При этом гидроксиды выпадают в осадок.
Номенклатура оснований
При составлении названия к слову «гидроксид» добавляют название элемента в родительном падеже. Если элемент имеет не-
10
