Уравнение изотермы адсорбции Ленгмюра
Степень
заполнения поверхности зависит от
сорбции и десорбции, когда скорость
адсорбции = скорости десорбции
Kap(1-Ѳ)=kdѲ;
где Ѳ-доля занятой активной поверхности
Kадс=b=ka/kd
тогда,

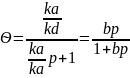 – уравнение
изотермы адсорбции Ленгмюра
– уравнение
изотермы адсорбции Ленгмюра
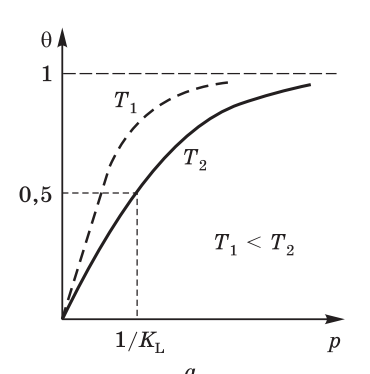 1)bp<<1
Ѳ=bp
1)bp<<1
Ѳ=bp
2)bp>>
Ѳ=1
Адсорбция
процесс самопроизвольный и эндотермический.

Если
температура повышается, процесс адсорбции
будет сдвигаться в сторону исходных
веществ.
Механизмы процесса адсорбции
1.
Механизм ленгмюра-хиншельвуду
2.
Механизм Или-Рудига
1)Мономолекулярная
реакция
реагент
А → продукт В
а)
Если продукт не адсорбируется
r=
kѲA=k*BAPA/1+BAPA
б)
Продукт адсорбируется и скорость реакции
меньше чем, в случае когда не адсорбируется
r=k*BAPA/1
+ BAPA+
BBPB
2)
Бимолекулярные реакции
А
+ В = С
а)
Если продукт не адсорбируется
r=(k*BAPA/1+BAPA
+ BBPB)*
BBPB/1+BAPA
+ BBPB)*
б)
Продукт адсорбируется – скорость будет
уменьшаться, те будет влиять BC,
PC.



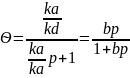 – уравнение
изотермы адсорбции Ленгмюра
– уравнение
изотермы адсорбции Ленгмюра 1)bp<<1
Ѳ=bp
1)bp<<1
Ѳ=bp