
- •АЛЬДЕГИДЫ И КЕТОНЫ
- •-Альдегиды и кетоны – это
- ••Если оксогруппа связана с одним углеводородным радикалом, то соединения называют альдегидами:
- •Классификация и номенклатура
- •По ИЮПАК карбонильная группа альдегидов
- •Способы получения
- •в) окисление алкенов:
- •г)Окисление алкенов без разрыва С-скелета
- •д) окисление углеводородов – применяют
- •2. Восстановление хлорангидридов карбоновых к-т (по Розенмунду) – получают альдегиды:
- •3. Оксосинтез (гидроформилирование алкенов) – с увеличением числа С- атомов на 1.
- •4. Гидратация алкинов (р-ция Кучерова) –
- •5. Гидролиз гем- дигалогенпроизводных
- •6. Декарбоксилирование карбоновых кислот и их солей:
- •А и К могут быть получены и из карбоновых к-т нагреванием в присутствии
- •Если декарбоксилированию подвергают соли дикарбоновых
- •7. а) Ароматические кетоны получают ацилированием по Фриделю- Крафтсу).
- •б) ароматические альдегиды –
- •Физические свойства
- •ХИМИЧЕСКИЕ СВОЙСТВА
- ••Наиболее типичными реакциями А и К являютя р-ции нуклеофильного присоединения АN
- •Реакции нуклеофильного
- •Механизм АN-реакций
- •2-ая стадия – быстрое присоединение электрофила к аниону с образованием конечного продукта присоединения.
- •Влияние катализаторов.
- •Однако следует выбирать оптимальное значение кислотности среды, т.к. избыток кислоты может привести к
- •Некоторые р-ции нуклеофильного присоединения проводят в условиях
- •• Влияние природы нуклеофила.
- •Влияние строения субстрата. 2 фактора –
- ••альдегиды более реакционноспособны, чем кетоны
- •Карбонильные соединения с учетом электронных эффектов групп, связанных с карбонильным С-атомом, можно расположить
- •б)пространственный фактор – карбонильный С-атом имеет плоскую конфигурацию, min энергии обеспечивается при атаке
- •АN-реакции с О-, S-, C- и Hal – нуклеофилами
- •Н2О – слабый нуклеофил.
- •Карбонильное
- •б) Присоединение спиртов
- ••Ацетали в отличие от простых эфиров легко гидролизуются в кислой среде с образованием
- •Кетоны менее активны, однако с 1,2- диолами образуют циклические кетали.
- •в) Присоединение натрий гидросульфита
- •Механизм реакции
- •Гидросульфитные производные гидролизуются как в кислой, так и в щелочной среде. Поэтому реакция
- •г) Присоединение циановодородной кислоты – образование циангидринов (α-гидроксинитрилов).
- •Механизм реакции
- •Присоединение HCN к карбонильным соединениям является р-цией
- •д) Присоединение магнийорганических соединений.
- •В зависимости от строения исходного карбонильного соединения можно получать различные спирты:
- •е) Взаимодействие с галогеннуклеофилами.
- •Реакции с N-нуклеофилами – реакции присоединения-отщепления.
- •Р-ция протекает в 2 стадии:
- •В этих р-циях как правило используют кислотный катализ для активации субстрата. Кроме того
- •Врезультате этого взаимодействия происходит замещение О-атома карбонильной группы с отщеплением молекулы воды.
- •Альдегиды с аммиаком образуют альдимины, которые легко полимеризуются.
- •Имины, содержащие хотя бы одну арильную группу (основания Шиффа) явл- ся более устойчивыми.
- •Оксимы кетонов под действием сильных кислот претерпевают перегруппировку Бекмана с образованием амидов кислот.
- •Реакции конденсации
- •Образующийся анион является амбидентным и может присоединить протон по двум реакционным центрам -
- ••Процесс превращения оксо-формы в енольную называют енолизацией, а явление существования оксосоединений в двух
- •а) Альдольная и кротоновая конденсация.
- •Кменее активные в р-ции конденсации, чем
- •Механизм альдольной конденсации АN
- •2) нуклеофильное присоединение енолят- иона к карбонильному С-атому с образованием связи С-С:
- •3) протонирование алкоксиданиона с регенерацией гидроксид-иона (kt):
- ••б) Реакция Кляйзена – Шмидта
- •Механизм аналогичен механизму альдольной конденсации.
- ••в) Реакция Перкина
- •Реакции окисления и восстановления
- •Окисление можно проводить не только обычными окислителями (р-рами КМnO4 и СrO3 в H2SO4),
- ••Р-ция серебряного зеркала является
- •Кетоны окисляются значительно
- •Практическое значение имеет
- •• Восстановление
- •Боргидрид натрия является мягким восстановителем, поэтому его используют для избирательного восстановления А и
- •• б) Получение углеводородов.
- ••Восстановление избытком гидразина в присутствии щелочи в среде растворителя диэтиленгликоля (по Кижнеру-Вольфу):
- •Реакции окисления-восстановления (диспропорционирования)
- •С конц. растворами щелочей они вступают в реакцию окисления- восстановления – одна молекула
- •окисление
- •Механизм реакции
- •Затем анион передает гидрид-ион другой молекуле альдегида
- •В перекрестной р-ции Канниццаро окисление-восстановление происходит между различными альдегидами.
- •б) Реакция Меервейна-Понндорфа Взаимодействие кетонов с
- •Реакции по углеводородному радикалу
- ••В щелочной среде происходит исчерпывающее галогенирование.
- •Иодоформная реакция используется также для идентификации метилкетонов – образуется желтый осадок иодоформа, имеющий
- •б) по ароматическому кольцу
- •Общие представления о непредельных альдегидах и кетонах
- •Наиболее общие методы получения:
- •дегидратация глицерина
- •в) специфический способ получения метивинилкетона
- •Химические свойства
- •Реакции электрофильного присоединения несимметричных реагентов протекают против правила Марковникова- через стадию 1,4- присоединения
- ••α,β-ненасыщенные А и К проявляют повышенную склонность к р-циям полимеризации;
- ••Окисление
- ••Сильные окислители окисляют и кратную связь, что приводит к расщеплению молекулы.
- ••Восстановление.
- •• При каталитическом гидрировании Н2 на
- •Отдельные представители
- •ХИНОНЫ
- •В основе этих соединений лежит группировка, которую называют хиноидной
- •Способы получения
- •Строение бензохинона
- •Химические свойства
- •Хиноны являются активными электрофилами и легко вступают в р-ции Дильса-Альдера – получение би-
- •Для хинонов наиболее характерны ОВР
- •Значительный интерес представляют красители, содержащие хиноидные структуры- дифенил-, трифенилметановые красители (малахитовый зеленый, фенолфталеин),
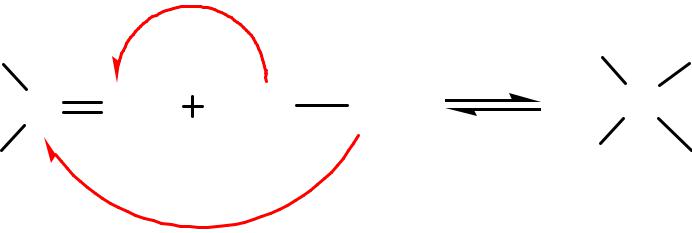
АN-реакции с О-, S-, C- и Hal – нуклеофилами
а) Присоединение воды (гидратация). Продукты прсоединения – гем-диолы.
R |
R |
OH |
C O H OH |
C |
|
R' |
R' |
OH |
гем-диол
Н2О – слабый нуклеофил.
Р-ция обратима. Большинство гем-диолов (гидратной формы карбонильных соединений) неустойчивы. Степень гидратации зависит от строения субстрата.
Уактивных карбонильных соединений, содержащих небольшие по объему и ЭА- заместители, положение равновесия сдвинуто
всторону гидратной формы, причем последняя обладает значительной устойчивостью.
Унеактивных карбонильных соединений гидратная форма неустойчива, положение равновесия сильно сдвинуто влево.

Карбонильное |
Содержание |
Свойства |
||||||||
соединение |
гидратной |
гидратной формы |
||||||||
|
|
|
|
|
|
|
|
|
формы (20оС) |
|
|
|
|
|
Cl |
O |
100% |
Гидрат устойчив, |
|||
|
|
|
|
|
|
|
|
|||
Cl |
|
|
|
|
|
|
|
C |
|
можно выделить |
|
|
|
C |
|
||||||
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
Cl |
|
|
||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
> 99,9% |
Гидрат устойчив |
H |
|
|
C |
|
только в водном |
|||||
|
|
|
|
|||||||
|
|
H O |
|
р-ре |
||||||
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
58% |
Гидрат |
|
H3C |
|
C |
|
неустойчив |
||||||
|
|
|||||||||
H
O 0%
H3C C
 CH3
CH3
б) Присоединение спиртов
Спирты - слабые нуклеофилы, поэтому в реакции с ними вступают только альдегиды. Вначале образуются полуацетали –
неполные простые эфиры гем-диолов.
Последние находятся в равновесии с исходным альдегидом.
Далее с избытком спирта в присутствии кислого катализатора полуацеталь реагирует со спиртом с образованием ацеталя. Ацетали устойчивы и могут быть выделены в свободном виде.
Ацетали – простые эфиры гем-диолов.
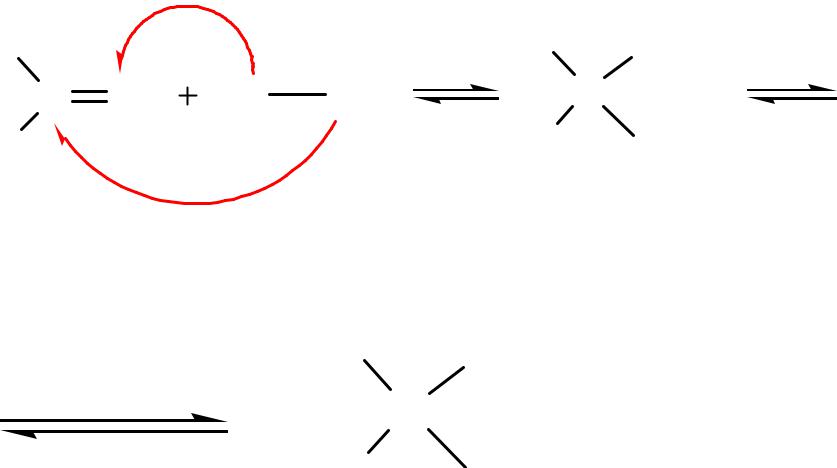
R C O |
R' OH H+ R C OR' |
|
Н |
H |
OH |
|
полуацеталь |
|
R'OH H+ |
R |
OR' |
|||
|
|
|
|
H |
C |
|
|
|
|
||
|
_ H2O |
||||
|
OR' |
||||
ацеталь
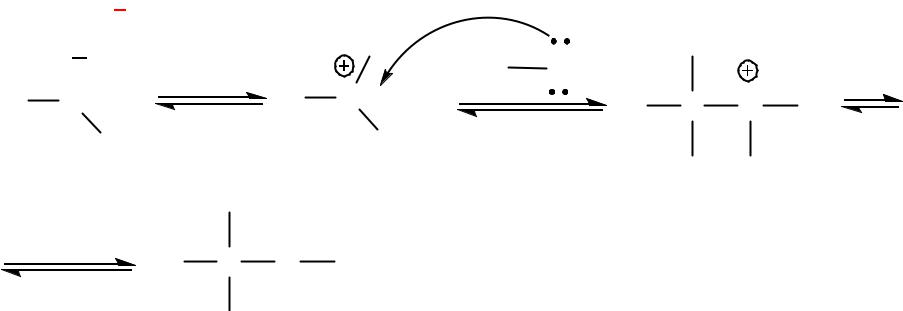
R C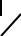
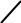 O
O
Н
- H+
быстро
Механизм реакции в условиях кислотного катализа
|
OH |
|
AN |
OH |
|
H+ |
R' |
OH |
|
||
C |
|
|
|||
R |
медленно |
R C |
O R' |
||
быстро |
Н |
Н |
H |
||
OH |
|
|
|
||
|
|
|
|
|
|
R C O R'
Н
•Ацетали в отличие от простых эфиров легко гидролизуются в кислой среде с образованием альдегида и спирта. Однако они устойчивы в щелочной среде.
•Образование ацеталей используют в органическом синтезе для временной защиты альдегидной группы.
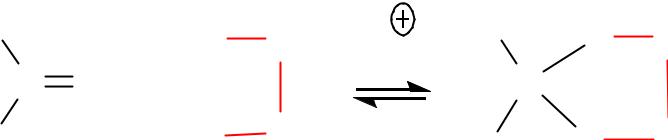
Кетоны менее активны, однако с 1,2- диолами образуют циклические кетали.
R |
|
|
HO |
CH2 |
H |
R |
O |
CH2 |
|
C |
O |
+ |
|
+ HOH |
|||||
|
CH2 |
|
|
C |
|
||||
R' |
|
|
HO |
|
R' |
O |
CH2 |
|
в) Присоединение натрий гидросульфита
– образование гидросульфитных производных.
Сульфит-ион является сильным нуклеофилом, поэтому р-ция у
альдегидов и метилкетонов идет
легко без катализаторов.
Вследствие большого объема нуклеофильного реагента пространственно затрудненные кетоны не вступают в эту р-цию.

R |
OH |
|
R |
OH |
!!! |
C |
O . |
O |
C |
|
|
R' |
S |
H |
SO3Na |
|
|
O |
Na |
|
|||
|
гидросульфитное |
||||
R'=Н, СН3 |
|
||||
|
производное |
|
|||
Качественная р-ция на альдегиды и метилкетоны –
выпадает белый осадок.
