

Состоит из растворимой АТФазы (фактор F1) и мембранных компонентов (комплекс F0). F1 располагается на поверхности внутренней
мембраны со стороны матрикса и обладает каталитической активностью синтеза или гидролиза АТФ. Комплекс F0 состоит из нескольких полипептидных субъединиц, он образует протонный канал в мембране.
а
Схема расположения Н+АТФсинтазных комплексов в мембранах хлоропластов (а) и митохондрий (б)
б
Пространственное строение Н+АТФсинтазного комплекса
|
Н+ |
|
F1 |
|
|
|
|
|
АДФ |
|
АТФ |
|
|
|
Р1 |
|
|
|
Н2О |
|
F0
Н+
Роль АТФазы заключается в следующем:
1.Перенос протонов из ММП в матрикс – осуществляется протонным каналом F0.
2.Гидролиз АТФ – осуществляется фактором F1.
3.Синтез АТФ – осуществляется комплексом F0 – F1.
122
До сих пор не раскрыт механизм превращения энергии тока протонов (или энергии «разрядки» мембраны) в энергию АТФ. Возможно, это происходит следующим образом. Субъединица F1 имеет два центра связывания: первый – с АДФ, другой – с Н3Р04. Причем фосфат присоединяется к F1 вблизи отверстия протонного канала (субъединицы F0).
Протоны, двигаясь через канал из ММП в матрикс, сталкиваются с фосфатом, отрывают от него один атом кислорода. В результате образуется высокореактивный богатый энергией радикал фосфорил. Он самопроизвольно присоединяется к АДФ, образуя АТФ.
5. Дыхательный контроль
Для синтеза АТФ в процессе тканевого дыхания необходимо наличие:
1)Субстратов окисления.
2)О2.
3)Субстратов фосфорилирования, т.е. АДФ и Рн.
В зависимости от соотношения этих компонентов различают 5 состояний дыхательной цепи:
1.Нет субстратов окисления и субстратов фосфорилирования. Скорость дыхания очень низкая.
2.Нет субстратов окисления, а субстратов фосфорилирования достаточно. Дыхание ограничено.
3.Активное дыхание. В избытке субстраты окисления и фосфорилирования. Скорость дыхания высокая. Происходит синтез АТФ. В результате уменьшается содержание АДФ и дыхание переходит в состояние 4.
4.Состояние дыхательного контроля. Когда весь АДФ превратится в АТФ, дыхание затормозится. На сопрягающей мембране накапливается ЭХП, т.к. мембрана не может разрядиться из-за отсутствия АДФ.
Мембранный потенциал препятствует движению электронов по дыхательной цепи, т.е. прекратится и окисление субстратов. Возврат в состояние 3 (активное дыхание) возможен при расходе АТФ и увеличении концентрации АДФ.
5.Нет О2 – дыхание прекращается (анаэробиоз).
Дыхание дает энергию для синтеза АТФ. Много АТФ – не нужно окислять субстраты, т . е . не нужно дыхание. Мало АТФ (много АДФ) – дыхание ускоряется. Следовательно, регуляция цепи переноса электронов или скорости дыхания осуществляется отношением АТФ/АДФ. Чем меньше это отношение (преобладание АДФ), тем интенсивнее идет дыхание, обеспечивая выработку АТФ.
Изменение скорости дыхания с изменением концентрации АДФ носит название дыхательного контроля.
123
Пример. Для состояния покоя в мышцах характерна низкая скорость дыхания, низкая концентрация АДФ и высокая – АТФ. Если вызвать ряд сокращений мышцы, то АТФ→АДФ + Рн, т.е. увеличится концентрация АДФ. Это приводит к повышению скорости дыхания (иногда в 100 раз), что в свою очередь, приведет к превращению АДФ в АТФ. Высокая скорость дыхания будет сохраняться до тех пор, пока АТФ-
зависимая сократительная система будет функционировать и поставлять АДФ.
6. Разобщители тканевого дыхания и окислительного фосфорилирования
Сопряжение между дыханием и синтезом АТФ может быть нару-
шено разобщителями. Разобщители нарушают дыхательный контроль ( т .е . стимулируют дыхание в отсутствие синтеза АТФ) и
стимулируют гидролиз АТФ в митохондриях.
Механизм действия разобщителей стал хорошо понятен после гипотезы Митчелла. Основное ядро этой гипотезы – создание ЭХП за счет избирательной проницаемости внутренней мембраны митохондрий для протонов. Если мембрана потеряет эту избирательность, т.е. протоны смогут проходить через мембрану в любом месте, не будет создаваться ЭХП, а значит, не будет синтезироваться АТФ, т.е. энергия окисления будет рассеиваться в виде тепла. Оказалось, что все разобщители имели общее свойство: они являлись протонофорами – т.е. переносчиками протонов. Они переносят протоны через мембрану в любом месте, а не только в пунктах сопряжения, это приводит к выравниванию градиента рН и мембранного потенциала. Энергия окисления рассеивается в виде тепла. Ученые В.П. Скулачев, Либерман показали, что разобщители резко понижают сопротивление мембран, т.е. экспериментально доказали гипотезу Митчелла.
В норме ~ 60% энергии окисления рассеивается в виде тепла. В этом заключается терморегуляторная функция тканевого дыхания.
Не может ли организм воспользоваться разобщением при неблагоприятных внешних условиях, например при переохлаждении? Здесь весьма кстати старая пословица «Не до жиру, быть бы живу». Лучше уж обойтись без синтеза АТФ, чем окоченеть на морозе. Надежным подтверждением этого послужили остроумные опыты В.П. Скулачева (1958-1960), в то время аспиранта кафедры биохимии животных МГУ.
Предоставим слово самому автору. «Мне не приходилось видеть ничего более жалкого, чем голубь без перьев. Дрожащий, иссиня-красный ко-
мочек стыдливо переминающийся с ноги на ногу и посматривающий с укоризной на своих мучителей. Нет, такой не вынесет двадцатиградусного мороза с ветром. Спустя полчаса после начала охлаждения, мы
124
вынули из холодильника полумертвую птицу с температурой тела около 30 С, вместо нормальной для голубя 41,5 С. Измерили дыхание и синтез АТФ в мышечных митохондриях. Оба показателя были близки к норме. Дыхание по-прежнему сопровождалось синтезом АТФ... Пове-
дение голубя при повторном охлаждении на следующий день разительно отличалось от той трагической картины, что мы видели накануне. Снизив свою температуру на 2-3 С, голубь умудрился каким-то обра-
зом остановить дальнейшее остывание тела. Через 3 часа после начала охлаждения, заглянув в очередной раз в холодильник, мы обнаружили, что голубь ведет себя вполне бодро и как-то даже агрессивно по-
сматривает на нас из своего ледяного плена. Ну, как там его митохондрии? Есть разобщение? Дыхание отключилось от синтеза АТФ. Энергия больше не накапливалась, а тотчас превращалась в тепло.
Потом такой же опыт был проделан на мышах, и вновь при повторном охлаждении наблюдалось разобщение дыхания и фосфорилирования. Охлаждаясь впервые, мыши, как и голуби (в наших суровых условиях опыта), отключить синтез АТФ не умели и гибли, если охлаждение не прекращалось. Им удалось продлить жизнь инъекцией искусственного разобщителя — динитрофенола... Впоследствии оказалось, что в разобщении на холоду замешаны свободные жирные кислоты, которые действительно повышают протонную проводимость мембраны».
Справедливости ради добавим, что подобные опыты, правда в несовершенном виде, проводились в России еще в XVIII столетии, когда
небезызвестная императрица Анна украшала, прибегая к услугам своего фаворита Бирона, ледяные дворцы статуями из прижизненно замороженных крепостных крестьян. В несколько ином ключе, уже в нашем веке, решали вопрос некоторые западные бизнесмены. Они продавали разобщители окислительного фосфорилирования желающим похудеть или улучшить фигуру. К сожалению, во многих случаях пациент, приобретая изящные формы, вскоре становился клиентом похоронного бюро.
Действие разобщителей
При действии разобщителей (лекарственные препараты – аминобарбитал, валиномицин, 2,4-динитрофенол, продукты жизнедеятельно-
сти микробов) более 60% энергии окисления идет на образование тепла → гипертермия.
Существуют эндогенные разобщители – фенолы, ненасыщенные жирные кислоты и их пероксиды.
Разобщение окисления и фосфорилирования наблюдается при действии экстремальных температур, радиации.
125
У новорожденных находится особый бурый жир, богатый митохондриями. Особенность этих митохондрий – на внутренней мембране очень мало пунктов сопряжения, а значит, почти вся энергия окисления рассеивается в виде тепла. Это имеет значение для защиты ЦНС ребенка от возможного переохлаждения, т.к. у них еще плохая терморегуляция.
Известно, что в бурой жировой ткани имеются специфические белки-термогенины, которые могут разобщать дыхание и фосфорилиро-
вание, участвуя в переносе протонов в матрикс митохондрий.
При охлаждении из симпатических нервных окончаний в бурой ткани освобождается норадреналин и выполняет двоякую функцию: во- первых, он активирует термогенины, а во-вторых, в адипоцитах он ак-
тивирует гормоночувствительную триглицеринлипазу и стимулирует высвобождение жирных кислот.
В свою очередь выделение норадреналина стимулируется тироидными гормонами, концентрация которых в крови повышается при охлаждении.
7. Гипоэнергетические состояния
Если на синтез АТФ идет меньше энергии, чем обычно, то наступает гипоэнергетическое состояние.
Причины развития гипоэнергетических состояний:
1)Нарушена доставка субстратов окисления (голод).
2)Нарушено поступление О2 (гипоксия).
–снижение концентрации кислорода в воздухе;
–нарушения работы сердечно-сосудистой и дыхательной сис-
тем, которые обеспечивают доставку кислорода к клеткам;
–анемия различного происхождения.
3)Повреждение внутренней мембраны митохондрий (или действуют разобщители).
4)Различные типы гиповитаминозов – нехватка витаминов РР,
В2, В1 и др., из которых образуются коферменты, участвующие в реак-
циях энергетического обмена.
126
Лекция 9
ОКИСЛИТЕЛЬНЫЕ СИСТЕМЫ, НЕ СВЯЗАННЫЕ С ЗАПАСАНИЕМ ЭНЕРГИИ
1. Свободное окисление. Роль в теплопродукции
Свободное окисление Тканевое дыхание, происходящее без сопряжения с окисли-
тельным фосфорилированием, называется свободным.
Свободное дыхание участвует:
1.В терморегуляторном образовании теплоты.
2.В образовании или разрушении метаболитов.
3.Детоксикации ксенобиотиков.
Выделяющаяся при этом энергия окисления рассеивается в виде тепла. Свободное дыхание (окисление) объединяет как разобщенные, так и первично не сопряженные дыхательные системы.
1.1. Первично не сопряженные дыхательные системы
Пероксидазный путь окисления – это окисление субстрата пу-
тем дегидрирования, водород сразу переносится на кислород с образованием перекиси – Н2О2.
SН2 + О2 → S + Н2О2 + Q
Энергия окисления рассеивается в виде тепла. Это простые окислительные системы. Окисление происходит с участием аэробных дегидрогеназ. Это флавопротеины, содержащие в качестве простетической группы ФАД или ФМН. Часто в их состав входят и металлы, т.е. они являются металлофлавопротеинами. В клетке около 80% этих ферментов сосредоточено в пероксисомах. Кроме того, они встречаются в мембранах, соприкасающихся с цитозолем. Субстратами окисления служат альдегиды, амины, Д и L аминокислоты, пурины. Некоторые из них
токсичны для организма.
Интенсивно проходит пероксидазное окисление в лейкоцитах, макрофагах и др. клетках, способных к фагоцитозу. Это связано с тем, что образующаяся Н2О2 используется для обезвреживания бактерий, распада токсичных продуктов. Однако избыточное накопление Н2О2
токсично, т.к. оно ведет к генерации свободных радикалов, повреждающих мембраны клеток. Поэтому простые окислительные системы требуют дополнительных ферментов для обезвреживания Н2О2. Это
ферменты пероксидаза, каталаза.
127
Оксигеназный путь окисления. Оксигеназы подразделяются на
2подгруппы.
1.Диоксигеназы (кислород-трансферазы, истинные оксигеназы).
Катализируют включение в молекулу субстрата обоих атомов молекулы
О2. Например: гомогентизатоксигеназа катализирует разрыв ароматиче-
ского кольца гомогентизиновой кислоты. При врожденном дефекте данного фермента в моче больного накапливается гомогентизиновая кислота. Она под действием воздуха окисляется в пигмент черного цвета – алкаптон, который выделяется с мочой и развивается алкаптонурия (моча черного цвета).
Оксигеназы участвуют в синтезе и деградации многих типов метаболитов. Включение кислорода происходит в две стадии:
1.О2 связывает с активным центром фермента,
2.Происходит реакция, в результате которой связанный О2 вос-
станавливается или переносится на субстрат.
Эти ферменты могут содержать в качестве активной группы гем или негемовое Fe. Чаще всего они катализируют разрыв двойной связи в ароматическом кольце.
2.Монооксигеназы (оксидазы со смешанной функцией, гидроксилазы). Эти ферменты катализируют включение в субстрат только одного из атомов молекулы кислорода. Другой атом кислорода восстанавливается до воды. Для этой цели необходим дополнительный донор водорода (косубстрат).
S Ã Н + О2 + ZН2 → S Ã ОН + Н2О + Z,
где Z – косубстрат.
Монооксигеназы часто участвуют в метаболизме лекарств. В ходе монооксигеназного окисления повышается растворимость веществ, могут появляться новые фармакологические свойства. Монооксигеназный путь окисления локализован в мембранах эндоплазматического ретикулума. При разрушении клетки мембраны эндоплазматического ретикулума собираются вместе, образуя пузырьки – микросомы. Отсюда часто монооксигеназный путь окисления называют кратко – микросомальное окисление.
Для работы монооксигеназной системы необходимы следующие основные компоненты:
1.Неполярный окисляемый субстрат;
2.Кислород;
3.Дополнительный субстрат (косубстрат) – донор водорода – НАДФН2;
4.Цитохромы Р450.
Цитохромы Р450 получили свое название вследствие способности в
128
виде восстановленного комплекса иметь максимум поглощения при длине волны 450 нм. Цитохром Р450 выполняет двоякую функцию:
1)Связывает субстрат окисления,
2)Проводит активацию молекулярного О2.
Микросомальное окисление представляет собой короткую цепь, состоящую из НАДФН2, ФАД, железосерных белков, цитохромов Р450,
в5, флавопротеинов, содержащих ФАД.
В общем виде микросомольное окисление неполярных ксенобиотиков (лекарств) осуществляется с помощью гидроксилазного цикла. Вначале первый (основной) субстрат окисления R-CН3 в мембране связывается с цитохромом Р450, железо в котором в форме Fe3+. Чтобы к этому комплексу R-CН3 присоединился О2, нужно Fe2+. Поэтому одновременно с этой реакцией НАДФН2 (косубстрат) окисляется флавопро-
теином, протоны и электроны передаются на ФАД и затем с помощью FeS белков происходит разделение потоков протонов и электронов. Первый электрон восстанавливает Fe3+ в Fe2+ в комплексе цитохром Р450-R-CН3. Этот комплекс может уже связать молекулу О2. Второй электрон от FeS активирует молекулу О2 в комплексе и образуется сво-
бодный радикал кислорода, он очень активный и происходит введение одного атома О2 в субстрат с образованием гидроксильной группы, а второй атом О2 – соединяется с двумя протонами, образуя Н2О. В ре-
зультате гидрофобный субстрат приобретает гидрофильные свойства, т.е. возможность выведения из организма с мочой. Так окисляются многие ксенобиотики, лекарства (морфин, фенобарбитал). В настоящее время известно свыше 7000 соединений способных окисляться монооксигеназными системами. Это основной путь обезвреживания и выведения ксенобиотиков. К сожалению, есть и исключения: монооксигеназная цепь, окисляя нетоксичный бензпирен (табачный дым, копчености) приводит к образованию токсичного оксибензпирена – сильного канцерогена. Это летальный синтез.
Монооксигеназная цепь содержится также в митохондриях на внутренней стороне внутренней мембраны. Она выполняет биосинтетическую роль, т.е. введение ОН-группы при синтезе стероидных гормо-
нов из холестерина в коре надпочечников, тестикулах, яичниках, плаценте. Таким путем образуется активная форма витамина Д в печени – 1,25-дигидроксихолекальциферол, желчные кислоты из холестерина в
печени.
2. Свободно-радикальное окисление
Кислород – потенциально токсическое вещество, до сих пор его токсичность связывали с образованием Н2О2. В настоящее время токсичность О2 связывают с его свободнорадикальными формами.
129
Под свободным радикалом понимают молекулу или ее часть, имеющую неспаренный электрон на молекулярной или на внешней (валентной) атомной орбитале.
Молекулярный О2 парамагнитен и обладает двумя не спаренными электронами. Они находятся на разных орбиталях. Восстановление О2
путем прямого введения пары электронов в его частично заполненные орбитали затруднено, т.к. существует «спиновый» запрет. Спиновый запрет Ã на орбитали могут находиться два электрона с разнонаправленными спинами, т.е. присоединение пары электронов должно сопровождаться «обращением» спина одного из электронов.
Спиновый запрет восстановления кислорода может быть преодолен последовательным добавлением одиночных электронов. Поэтому О2 легко
вступает в реакции с веществами, содержащими одиночные неспаренные электроны. В одноэлектронных реакциях восстановления О2 участ-
вуют свободнорадикальные промежуточные продукты. Полное восстановление О2 до Н2О требует четырех электронов.
При одноэлектронном восстановлении в качестве промежуточных продуктов возникают 1) супероксидный анион О2-•, 2) пероксид Н2О2; 3)
гидроксидный радикал ОН . Эти продукты очень реакционоспособны, и их присутствие может представлять угрозу для целостности живых
систем. ОН Ã наиболее мутагенный продукт ионизирующей радиа-
ции, представляет собой чрезвычайно мощный окислитель, который
может атаковать все органические соединения. Одноэлектронное восстановление инициирует цепь реакций, которые ведут к образованию ОН–.
Образование свободных радикалов:
О2 + ē О2- супероксидный
О2- + Н+ НО2 пероксидный
О2- + НО2 + Н+ Н2О2+ О2 О2- + Н2О О2 + ОН- + ОН
e2+
О2- + Fe3+ О2+ Fe2+
Н2О2+ Fe2+ Fe3++ ОН + ОН гидроксидный
В процессе тканевого дыхания происходит одноэлектронный перенос, т.е. всегда имеются возможности для генерации свободных радикалов.
3. Пероксидация жирных кислот
Хорошо известно, что жиры при длительном хранении в условиях доступа кислорода и света подвергаются прогорканию, что связано с ау-
130
тоокислением ненасыщенных жирных кислот. Нечто подобное проис-
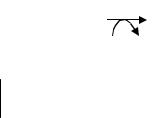
ходит и в животном организме. Аутоокисление жиров, протекающее в органах и тканях, называют липидной пероксидацией, так как этот процесс происходит с образованием перекисей и гидроперекисей ненасыщенных жирных кислот. Пероксидация жирных кислот может быть инициирована любым веществом, способным «атаковать» и захватывать атом водорода метиленовой группы, оставляя, таким образом, неспаренный электрон при углероде. Удаление водорода протекает легче у метиленовой группы, находящейся в непосредственной близости к ненасыщенной связи (углеродные атомы, вовлекаемые в пероксидацию, помечены в приведенной ниже формуле):
O
O CH2OC
COHC
O
CH2OC
Чем больше содержится в жирной кислоте ненасыщенных связей, тем интенсивнее протекает ее пероксидация. Пероксидацию относят к категории свободнорадикального окисления; ее активно инициируют постоянно возникающие в животных тканях первичные кислородные радикалы, такие, как O2-• (супероксид), НО2 (гидроперекисный
радикал), НО (гидроксильный радикал), взаимодействие с которыми приводит к переносу радикального состояния на молекулу жирной кислоты, т. е. к образованию липидных радикалов и перекисей.
Процесс пероксидации жирной кислоты включает следующие 3 стадии:
I стадия – инициация (образование свободного липидного радикала R· из предшественника):
RH+ Х· R·+XH
где RH – ненасыщенная жирная кислота, входящая в состав триа- цил-глицеринов, фосфолипидов, эфиров холестерина;
Х· – первичный свободный радикал.
I стадия пероксидации может быть представлена в следующем ви-
де:
131
