
очень низкой плотности (ЛПОНП) содержат высокий процент триацилглицеринов и небольшой – белка, при электрофорезе ХМ остаются на старте, а ЛПОНП – называют пре- ЛП. Меньшие частицы – липопротеины низкой плотности (β-ЛП) – основные переносчики холестерина. Липопротеины высокой плотности (ЛПВП) (α-ЛП) содержат самое
большое количество белка. И это единственный класс ЛП, которые содержат больше компонентов оболочки, чем сердцевины.
Характеристика основных классов липопротеинов
Название по |
|
Состав |
|
Место |
Функции |
плотности |
ЭФ подвиж- |
Липиды |
Апопротеины |
синтеза |
|
|
ности |
|
|
|
|
ХМ (хиломик- |
ХМ |
ТГ, ХС |
А, В, С, Е |
Кишечник |
Экзогенный |
роны) |
|
|
|
|
транспорт |
ЛПОНП ЛП |
Пре-β-ЛП |
ТГ, ХС |
В, С, Е |
Печень |
Эндогенный |
очень низкой |
|
|
|
|
транспорт |
плотности |
|
|
|
|
|
ЛПНП ЛП |
β-ЛП |
ХС |
В |
Сосуд. рус- |
Прямой |
низкой плот- |
|
|
|
ло, печень |
транспорт |
ности |
|
|
|
|
холестерина |
ЛПВП ЛП вы- |
α-ЛП |
ХС |
А, Е, Д |
Печень, |
Обратный |
сокой плотно- |
|
|
|
кишечник |
транспорт |
сти |
|
|
|
|
холестерина |
Различают экзогенный, т.е. транспорт пищевых липидов и эндо- |
|||||
генный транспорт – т.е. транспорт липидов, синтезированных в орга- |
|||||
низме. |
|
|
|
|
|
|
|
|
жирыпищи |
||
Э |
|
|
жирыпищи |
||
|
|
|
|
||
к |
Жировая |
ХМ |
лимфа |
желчныекислоты |
|
з |
|||||
Т |
|
||||
о |
К |
|
|
|
|
ег |
А ЛПЛ |
|
|
|
|
н |
Н |
|
r - ХМ |
|
|
н |
И |
|
|
|
|
ы |
Мышечная |
|
|
|
|
й |
|
|
|
|
|
э |
Жировая |
|
|
|
|
н |
Т |
|
|
ЛПВП |
|
д |
К |
|
|
|
|
о |
А ЛПЛ |
|
|
ЛХАТ |
|
г |
Н |
|
ЛПНП |
|
|
е |
И |
|
|
|
|
н |
Мышечная |
|
|
непеченочные |
|
н |
|
|
|||
|
|
клетки |
|||
ы |
|
|
|
|
|
й |
|
триацилглицериныглцерды |
холестерин |
||
|
|
|
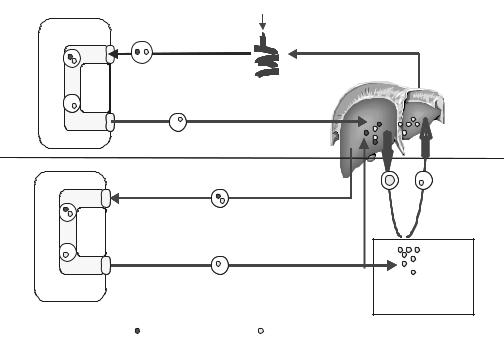
Экзогенный транспорт |
||
182
Ресинтезированные в энтероцитах триацилглицерины вместе с фосфолипидами, холестерином и белками включаются в хиломикроны. Хиломикроны содержат апопротеин В48 и апоА. Хиломикроны из энтероцитов попадают в грудной лимфатический проток и далее – в кровь, здесь они встречаются с частицами ЛПВП, содержащими апоЕ и апоСII. ХМ отдают апоА частицам ЛПВП, а взамен приобретают апоЕ и апоСII. Этот обмен очень важен, т.к. апоСII служит активатором фермента ли-
попротеинлипазы – ЛПЛ. Этот фермент синтезируется и секретируется клетками жировой и мышечной ткани, клетками молочных желез. Секретируемый фермент прикрепляется к плазматической мембране эндотелиальных клеток капилляров тех тканей, где он синтезировался. АпоСII, находящейся на поверхности ХМ, активирует ЛПЛ, она гидро-
лизует триацилглицерины в составе ХМ до глицерина и жирных кислот. Освободившиеся жирные кислоты либо поступают в клетки жировой и мышечной ткани, либо соединяются с альбуминами плазмы и транспортируются в общий кровоток. В результате действия ЛПЛ ХМ резко уменьшаются в размерах и называются уже ремнантами (ремнант-
остаток). Ремнанты ХМ рецепторным путем захватываются печенью и с ними в печень попадают в основном холестерин и небольшое количество триацилглицеринов. Клетки печени включают поступивший холестерин, а также вновь синтезированный, триацилглицерины, фосфолипиды и белки в состав ЛПОНП.
Эндогенный транспорт. Основными белками ЛПОНП являются апоВ и апоС, а липидами – триацилглицерины. Кроме того, в печени синтезируется ещё один класс липопротеинов-ЛПВП, у них основной
белок – апоА, много фосфолипидов и свободного холестерина, а ядро пустое – так называемые насцентные ЛПВП. Они играют большую роль в обратном транспорте холестерина из клеток периферических тканей в печень. Т.к. ЛПОНП содержат апоСII, происходит активация ЛПЛ, ко-
торая гидролизует триацилглицерины ЛПОНП и превращает ЛПОНП в липопротеины промежуточной плотности ЛППП. ЛППП под действием фермента, синтезируемого в печени и секретируемого в кровь, – печеночной триацилглицеринлипазы, превращаются в ЛПНП. Основным липидом в ЛПНП становится холестерин, который в составе ЛПНП переносится к клеткам всех тканей. ЛПНП образуются непосредственно в сосудистом русле и участвуют в прямом транспорте холестерина.
Доказано, что синтез ЛПЛ происходит под влиянием инсулина. При сахарном диабете, когда отмечается дефицит инсулина, уровень ЛПЛ снижается. В результате в крови накапливается большое количество липопротеинов, богатых триацилглицеринами (IV тип ГЛП).
183
Лекция 16
ЭЙКОЗАНОИДЫ - НОВЫЙ ТИП БИОЛОГИЧЕСКИХ РЕГУЛЯТОРОВ
1. Классификация эйкозаноидов, механизм образования
Эйкозаноиды - это производные эйкозаполиеновых жирных кислот, т.е. С:20 жирных кислот. Медицинское значение имеют эйкозатетраеновая жирная кислота ω-6 20:4 (арахидоновая) и эйкозапентаеновая ω-3 20:5 (ЭПК). Арахидоновая кислота может синтезироваться из лино-
левой жирной кислоты (незаменимая жирная кислота), содержится в печени, мясе. ЭПК синтезируется из линоленовой (незаменимая жирная кислота), содержится в морской рыбе.
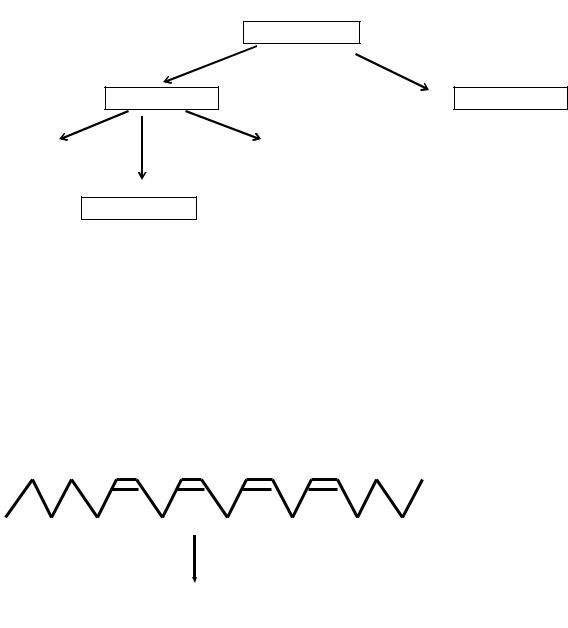
Классификация
козаноид
циклоокс |
сигеназа |
йкотриены
простаг |
|
тациклины |
тромб саны
Термин «простагландины» часто используют для обозначения всех простаноидов.
Простагландины были вначале открыты в семенной жидкости, но сейчас известно, что они содержатся практически во всех тканях и их называют «местные гормоны».
Простагландины образуются из арахидоновой кислоты путем циклизации под действием циклооксигеназы.
|
|
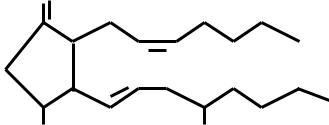
Арахидоновая кислота |
|
|
14 |
11 |
8 |
5 |
СООН |
|
|
|
|
Арахидоновая |
|
|
|
|
кислота 20:4 |
20 |
|
|
|
5,8,11,14 6 |
184
О |
|
5 |
СООÃ |
9 |
|
10 |
Простагландин Е2 PGE2 |
11 |
|
ОН |
ОН |
В зависимости от числа двойных связей все простагландины делят на три группы –1,2,3. Номер группы указывают цифрой справа внизу от названия. Каждая из этих групп, в зависимости от конфигурации пятичленного кольца и характера заместителя в кольце, называется А,В,Е,F и т.д. Например, РGЕ в девятом положении имеет кетогруппу, РGF –
ОН группу.
Механизм образования простагландинов
Источником арахидоновой кислоты служат фосфолипиды мембран. Из фосфолипидов она освобождается под действием фосфолипазы А2. Активация фосфолипазы А2 происходит под действием Са2+, тром-
бина, ангиотензина, брадикинина, липопероксидов.
Арахидоновая кислота подвергается циклизации под действием изоферментов циклооксигеназы 1 и 2 (ЦОГ).
ЦОГ-1 контролирует синтез простагландинов, участников физиологических процессов. Они регулируют:
1) целостность слизистой оболочки желудочно-кишечного тракта; 2) функцию тромбоцитов (тромбоксан А2); 3) функцию эндотелия (простациклины); 4) почечный кровоток.
ЦОГ-2 участвует в синтезе простагландинов в воспаленных тка-
нях.
ЦОГ-1 является конститутивным изоферментом, постоянно при-
сутствует в большинстве тканей организма для обеспечения нормальной функциональной активности клеток.
ЦОГ-2 это индуцируемый изофермент, в нормальных условиях
присутствует в тканях в крайне низких концентрациях, в больших количествах появляется в активированных макрофагах, синовиоцитах. Мощными индукторами ЦОГ-2 являются митогены, эндотоксины, цитокины,
факторы роста.
Кортикостероиды (глюкокортикоидные гормоны) ингибируют фосфалипазу А2, прекращая выработку всех эйкозаноидов, но наиболее значимо ингибируют активность ЦОГ-2, вызывая противовоспалитель-
ный эффект.
185
Нестероидные противовоспалительные препараты (аспирин и др.) подавляют активность ЦОГ-1 и ЦОГ-2. С подавлением активности ЦОГ-2 связано их противовоспалительное действие, с подавлением активности ЦОГ-1 – побочное, например, повреждение слизистой желуд-
ка. В настоящее время ведется поиск противовоспалительных препаратов, селективно ингибирующих ЦОГ-2.
Инактивация простагландинов происходит при участии фермента 15-гидрокси-простагландин-дегидрогеназы. Она активна во всех тканях,
но особенно в легких. Время жизни простагландинов – один оборот крови.
2.Биологические эффекты эйкозаноидов
Вмембранах клеток различных тканей есть рецепторы для простагландинов. После связывания простагландинов Е с рецепторами в клетках увеличивается содержание цАМФ, при связывании РGF –
цГМФ. Поэтому часто эффекты разных простагландинов на одну и ту же клетку могут быть разными.
Примеры эффектов простагландинов
Процесс, ткань |
РGE2 |
РGF |
Гладкая мускулатура матки |
Расслабляет |
Сокращает |
Аллергические реакции |
Индуцирует |
Подавляет |
Тромбоксаны образуются в тромбоцитах, простациклины образуются в сосудистой стенке. Они по-разному влияют на агрегацию
тромбоцитов на поврежденной поверхности эндотелия: тромбоксан ускоряет агрегацию и свертывание крови, простациклин тормозит эти процессы. Поэтому соотношение тромбоксана и простациклина во многом определяет условия тромбообразования на поверхности эндотелия сосудов.
При употреблении жителями Крайнего Севера с пищей эйкозапентаеновой кислоты из нее образуется иная серия простагландинов и тромбоксанов, чем при использовании арахидоновой кислоты; так как такие тромбоксаны обладают слабым агрегационным действием по сравнению с тробоксанами из арахидоновой кислоты, то в целом происходит антиагрегационный сдвиг. Считается, что именно по этой причине у эскимосов Гренландии наблюдается пониженная свертываемость крови и низкая распространенность ИБС. В ряде стран (Норвегия, Япония, Россия и др.) производятся в качестве пищевых добавок препараты, содержащие выделенные из рыбьего жира
186
эйкозапентаеновую и докозагексаеновую кислоты с целью профилактики сердечно-сосудистых заболеваний.
Лейкотриены представляют собой недавно открытое семейство соединений, обладающих исключительно высокой физиологической активностью. Название «лейкотриены» происходит от двух слов: «лейкоциты» (впервые эти соединения были обнаружены в лейкоцитах)
и «триены» (у всех представителей этого класса соединений из четырех ненасыщенных связей три являются конъюгированными).
Различают 6 типов лейкотриенов (А, В, С, D, E, F), причем последние 4 (С-F) содержат остаток трипептида глутатиона или
аминокислоты, составляющие его. Более распространены лейкотриены, не содержащие аминокислот.
Лейкотриены образуются в лейкоцитах, моноцитах и макрофагах в ответ на определенные стимулы, направленные на фосфолипазы мембран этих клеток. Освободившаяся из фосфолипидов при действии фосфолипазы А2 арахидоновая кислота подвергается в указанных
клетках липооксигеназному пути превращений, в ходе которого и образуются лейкотриены. Последние активирую лейкоциты и рассматриваются как медиаторы воспалительных реакций. Они также влияют на проявление анафилаксии и другие реакции иммунного ответа, вызывают сокращение мускулатуры бронхов в концентрациях в 100-1000 раз меньших, чем гистамин, способствуют сокращению
коронарных артерий и, возможно, участвуют в развитии ишемии миокарда.
Лекция 17
ЖИРЫ КАК ИСТОЧНИК ЭНЕРГИИ
1. -окисление жирных кислот
Назначение окисления жирных кислот:
1)с энергетической целью протекает в печени, почках, скелетной
исердечной мышцах; 2) источник эндогенной воды. Окисление жирных кислот происходит в митохондриях. Для удобства процесс окисления можно считать состоящим из 3-х этапов: 1) активация жирных кислот и их транспорт в митохондрии; 2) сам процесс β-окисления; 3) окисления в ЦТК образующегося ацетил-КоА.
β-окисление жирных кислот означает, что атом C, находящейся в β-положении в процессе окисления становится карбоксильным концом
укороченной ацильной цепи.
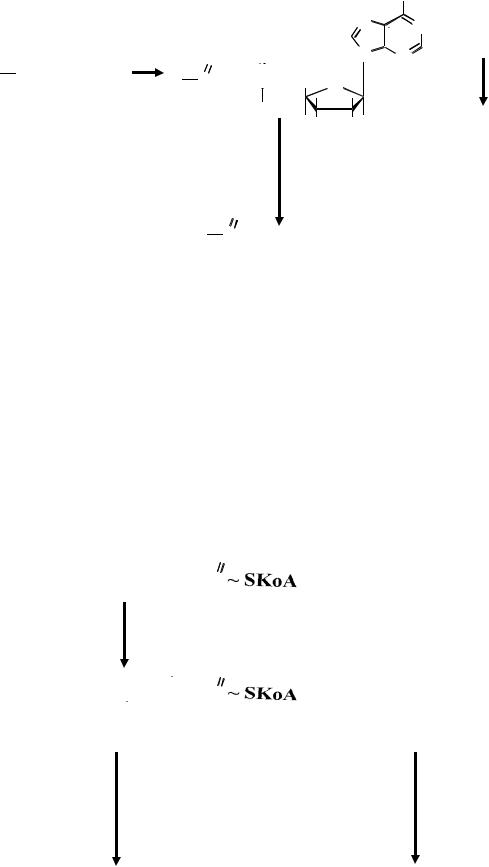
I. Активация и транспорт жирной кислоты.
187
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
NH2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N + Н4Р2О7 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пирофосфат |
R |
COOH+АТФ |
|
O |
O |
|
|
|
|
|
N |
N |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
R |
C ~ O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
P |
|
O |
|
CH |
O |
|
|
|
|
Н2О |
|||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
O- |
|
|
|
|
2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Н3РО4 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|||||
|
|
|
|
|
|
|
|
|
|
ациладенилат |
|
|
||||||||
+НSКоА
O
R C ~ SKoA +АМФ
ацил-КоА
Происходит в цитозоле. Образуется активная форма жирной кислоты – ацил-КоА. Далее ацил-КоА должен попасть в митохондрии, где непосредственно проходит процесс β-окисления. Мембрана митохондрий не проницаема для ацил-КоА, поэтому его перенос происходит с помощью карнитина – ацил-карнитин (транспортная
форма).
II. -окисление
В митохондриях происходит перенос остатка жирной кислоты с карнитина на КоА митохондрий с образованием ацил-КоА. Карнитин
вновь возвращается в цитозоль.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
R |
|
CH 2 |
|
CH 2 |
|
CH 2 |
|
|
C |
ацил-КоА |
|||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
ФАД (ацилКоАдегидрогеназа) |
|||||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
O |
+ФАДН2 |
|
R |
|
CH 2 |
|
C |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
C |
|
|
|
|
C |
||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
H |
|
|
|
|
|
НДЦ |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
транс-изомер |
½ О2 |
||||
|
|
|
|
|
|
|
|
|
|
бета-еноилацил-КоА |
|||||
+2 Н3РО4
еноилгидратаза
+2 АДФ
+ Н2О
ФАД + Н2О + 2 АТФ
188
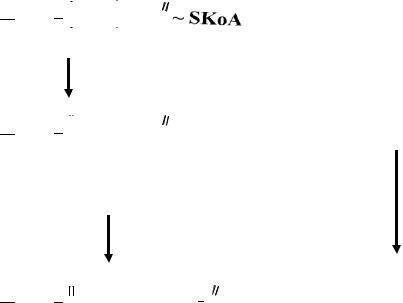
R CH 2
R CH2
R CH 2
ацил-КоА
OH |
|
H |
|
O |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
C |
|
|
|
C |
|
||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||
H |
|
H |
|
|
L-бета-гидроксиацил-КоА |
||||||
|
Бета-гидроксиацил-КоА-дегидрогеназа |
||||||||||
|
+НАД+ |
|
|
|
|||||||
O |
|
|
|
|
|
|
O |
+НАДН+Н+ |
|||
|
|
|
|
|
|
C~SKoA |
|||||
C |
|
CH2 |
|
|
|||||||
|
|
|
|||||||||
|
бета-кетоацил-КоА |
ПДЦ |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
½ О2 |
|
|
|
|
|
|
+НsКоА |
+3 Н3РО4 |
||||
|
|
|
|
|
|
тиолаза |
+3 АДФ |
||||
НАД+ + Н2О + 3АТФ
O O
C~ S K o A + CH 3 C 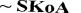
ацетил-КоА
Далее ацил-КоА подвергается вновь процессу β-окисления (т.е. действует ацил-КоАдегидрогеназа), а ацетил-КоА окисляется в ЦТК (общий путь катаболизма). Процесс β-окисления продолжается до образования ацетоацетил-КоА, который распадается до двух молекул аце- тил-КоА.
Катаболизм жирных кислот обеспечивает продукцию энергии. Расчет ведут по формуле:
[5 (n/2-1) + n /2х12] Ã 1
5 – число молекул АТФ, образуемое при одном акте β-окисления; n – число атомов C в жирной кислоте; n/2-1 число актов β-окисления; n/2 число молекул ацетил-КоА; 12 – число молекул АТФ при полном окислении одной молекулы ацетил-КоА в ЦТК; 1 Ã молекула АТФ, за-
траченная на активацию жирной кислоты.
Представление об окислении ненасыщенных жирных кислот и жирных кислот с нечетным числом углеродных атомов
Ненасыщенные жирные кислоты до места двойной связи окисляются также, как насыщенные. Если двойная связь не имеет трансконфигурации, то действуют специальные ферменты, обеспечивающие перемещение двойной связи и изменение конфигурации из цис в трансформу. Далее процесс идет обычным путем.
При окислении жирных кислот с нечетным числом углеродных атомов образуется не ацетил-КоА, а пропионил-КоА, он превращается в
189
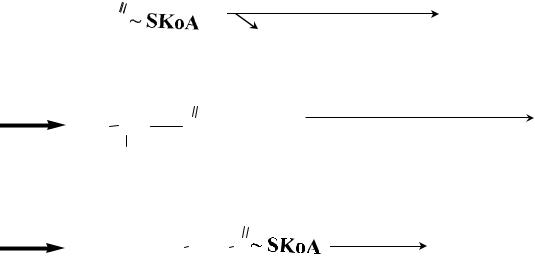
сукцинил-КоА.
|
|
|
|
O |
+ СО + АТФ, биотин |
CH3 |
|
CH2 |
|
C |
|
|
|
АДФ + Рн |
|||
|
|
||||
пропионил-КоАкарбоксилаза |
|
||||
O
CH3 CH C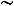
 COOH
COOH
метилмалонил-KoA
VitВ12
мутаза
O
HOOC |
|
CH2 CH2 C |
ЦТК |
|
сукцинил-КоА
Регуляция окисления жирных кислот
Скорость β-окисления определяется количеством жирных кислот
и запасом энергии в клетке. Количество жирных кислот зависит от содержания жиров в пище и от скорости липолиза эндогенных липидов. β-
окисление активируется при накоплении в клетке АДФ и ингибируется накоплением АТФ.
2. Окисление глицерина
Источники глицерина:
1.Гидролиз триацилглицеринов (ТГ) пищи в кишечнике под действием поджелудочной липазы;
2.Гидролиз триацилглицеринов, входящих в состав ядра хиломикронов, ЛПОНП под действием липопротеинлипазы в капиллярах жировой, мышечной ткани;
3.Гидролиз триацилглицеринов ядра ЛППП под действием печеночной триацилглицерин липазы в общем кровотоке;
4.Гидролиз триацилглицеринов жировой ткани под действием внутриклеточных липаз.
Освободившийся глицерин с током крови разносится ко всем органам и тканям. В печени, почках, кишечнике, где есть активная глицеролкиназа, происходит окисление глицерина с образованием 21 АТФ.
190
Цитозоль
Происходит активация глицерина с образованием - глицерофосфата, который поступает в митохондрии с участием α- глицерофосфатного челночного механизма:
CH2OH |
+ АТФ |
|
|
CH2OH |
|
|
|||||
|
CHOH |
|
|
|
|
CHOH |
|
+ АДФ |
|||
|
глицеролкиназа |
|
|
||||||||
|
CH2OH |
|
CH2OPO3H2 |
|
|||||||
|
|
|
|
|
|
|
|||||
глицерин |
|
|
|
|
|
|
-глицерофосфат |
||||
Митохондрии |
|
|
|
|
|
|
|
|
|
||
CH2OH |
+ ФАД |
|
CH2OH |
+ ФАДН2 |
|||||||
CHOH |
|
C |
|
O |
|
+1/2 О2 |
|||||
|
|
|
|||||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||
|
-глицерофосфат- |
|
|
|
|
|
|
|
+ 2АДФ |
||
|
CH2OPO 3H2 |
||||||||||
CH2OPO3H2 |
дегидрогеназа |
+ 2Н3РО4 |
|||||||||
-глицерофосфат |
диоксиацетонфосфат |
||||||||||
|
|||||||||||
|
|
|
Цитозоль |
ФАД + Н2О + 2АТФ |
|||||||
Образующийся в митохондриях диоксиацетонфосфат возвращается в цитозоль, где вступает в реакции специфического пути катаболизма глюкозы.
|
|
CH2OH |
|
H |
|
C |
|
O |
||||
|
|
|
|
|||||||||
|
|
|
|
|
||||||||
|
|
|
|
|||||||||
|
|
|
|
|
триозофосфатизомераза H |
|
|
|
|
|
|
|
C |
|
O |
C |
|
OH |
|||||||
|
||||||||||||
|
|
|
||||||||||
|
||||||||||||
|
|
CH2OPO3H2 |
|
|
|
|
CH2OPO3H2 |
|||||
|
|
|
|
|||||||||
диоксиацетонфосфат |
3-фосфоглицериновый альдегид (3-ФГА) |
|||||||||||
Дальнейшие превращения 3фосфоглицеринового альдегида могут быть двоякими:
1)по реакциям глюконеогенеза до глюкозо-6-фосфата и далее с
образованием свободной глюкозы;
2)по реакциям гликолиза до пирувата, который затем окисляется
вобщей стадии катаболизма до СО2 и Н2О.
Энергетический эффект окисления глицерина до СО2 и Н2О
- На стадии глицеролкиназы затрачена на образование |
-1 АТФ |
-глицерофосфата |
191
