
2 курс / Микробиология 1 кафедра / Доп. материалы / Микробиология от Насти
.pdf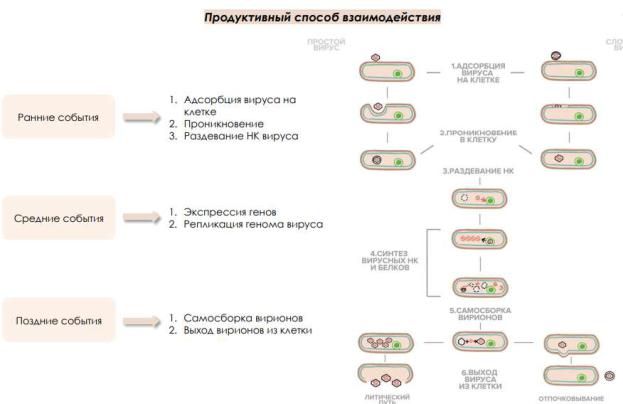
Если необходимо определить возбудитель, выделенный от больного, ставят ориентировочную реакцию агглютинации, применяя диагностические антитела (агглютинирующую сыворотку), т. е. проводят серотипирование возбудителя.
Ориентировочную реакцию проводят на предметном стекле. К капле диагностической агглютинирующей сыворотки в разведении 1:10 или 1:20 добавляют чистую культуру возбудителя, выделенного от больного.
Рядом ставят контроль: вместо сыворотки наносят каплю раствора натрия хлорида. При появлении в капле с сывороткой и микробами хлопьевидного осадка ставят развернутую реакцию агглютинации в пробирках с увеличивающимися разведениями агглютинирующей сыворотки, к которым добавляют по 2—3 капли взвеси возбудителя.
Агглютинацию учитывают по количеству осадка и степени просветления жидкости. Реакцию считают положительной, если агглютинация отмечается в разведении, близком к титру диагностической сыворотки.
Одновременно учитывают контроли: сыворотка, разведенная изотоническим раствором натрия хлорида, должна быть прозрачной, взвесь микробов в том же растворе — равномерно мутной, без осадка. Разные родственные бактерии могут агглютинироваться одной и той же диагностической агглютинирующей сывороткой, что затрудняет их идентификацию. Поэтому пользуются адсорбированными агглютинирующими сыворотками, из которых удалены перекрестно реагирующие антитела путем адсорбции их родственными бактериями. В таких сыворотках сохраняются антитела, специфичные только к данной бактерии.
Билет 27 1. Типы взаимодействия вируса с эукариотической клеткой. Этапы репродукции вируса. Понятие об интерференции. (28)
Различают 3 типа взаимодействия:
продуктивный тип – репродукция завершается образованием вирусного потомства;
абортивный тип – не образуются новые вирусные частицы, т.к. инфекционный процесс прерывается на одном из этапов;
интегрированный тип – вирогения – характеризуется встраиванием вирусной ДНК в хромосому клетки хозяина.
101
1.Адсорбция вируса на клетке. Белки на поверхности вириона притягиваются к специфическим рецепторам на поверхности клеток. Притяжения специфичны для каждого вируса. Некоторые вирусы имеют узкий профиль действия, в то время как другие – достаточно широкий.
Например, полиовирус может заходить только в клетки приматов, в то время как вирус бешенства может инфицировать клетки всех видов млекопитающих.
Также вирусы обладают тропизмом – избирательным поражением определенных клеток, тканей и органов, основанном на их специфическом взаимодействии с рецепторами клетки. Органная специфичность вирусов управляется рецепторами притяжения – клеточные рецепторы, которые могут идентифицировать поверхностные протеины вируса.
Например, ВПГ 1 типа притягивается к рецепторам фактора роста фибробластов, вирус бешенства – к рецепторам ацетилхолина, ВИЧ – к CD-4 рецепторам Т-лимфоцитов, ВЭБ – к рецепторам комплемента.
2.Проникновение вируса в клетку. Простые вирусы проникают в клетку чаще всего с помощью рецепторзависимого эндоцитоза, а сложные – в результате слияния оболочки вируса (суперкапсида) с клеточной мембраной.
Некоторые вирусы могут поддерживать свой репродуктивный цикл, не проникая в клетку, а просто запуская туда свою нуклеиновую кислоты. Такая нуклеиновая кислота, которая поддерживает репродуктивный цикл вируса в клетке без участия самого вируса называется инфекционной. Она способна пройти весь цикл развития вируса и дать начало новым вирусным частицам.
3.Раздевание НК вируса. После того, как вирусы оказались внутри клетки, они подвергаются депротеинизации. В результате в цитоплазме клетки оказывается НК, нуклеокапсид или сердцевина вируса.
4.Экспрессия генов и репликация генома. Начинается с синтеза мРНК, необходимая для синтеза вирусных белков, может синтезироваться поразному. Это зависит от того, какая нуклеиновая кислота представлена у вируса.
5.Самосборка вирионов. Когда вирусная мРНК синтезировалась, она направляется к рибосомам клетки хозяина для синтеза вирусных белков.
Сначала, до репликации генома, образуются ранние протеины – ферменты, необходимые для репликации вируса. Затем образуются поздние протеины – структурные белки. Далее вирусное потомство собирается благодаря упаковке вирусного генома в капсидные белки.
6.Выход вирусов из клетки. Вирусные частички выходят из клетки двумя путями:
Первый – это разрыв клеточной мембраны и выход зрелых частиц. Это случается обычно у простых, безоболочечных вирусов
второй – отпочковывание от клеточной мембраны клетки хозяина. Характерен для сложных, оболочечных вирусов.
Исключение: семейство герпесвирусов: они получают свою липопротеиновую оболочку от ядерной мембраны клетки хозяина, а не от цитоплазматической. Отпочковывание начинается, когда сепцифические вирусные белки входят в клеточную мембрану в специфических участках. Вирусный нуклеокапсид затем взаимодействует со специфическим участком ЦПМ с помощью матриксного протеина. ЦПМ инвагинирует в этом участке и покрывает вирусную частицу собой.
Отпочковывание вирусов обычно не разрушает клетку и в определенных случаях клетка выживает после отпочковывания от нее большого количества вирусов.
ДНК-содержащие вирусы. Все ДНК-вирусы, за исключением поксвирусов, реплицируются в ядре и используют хозяйскую ДНКзависимую РНК-полимеразу, чтобы синтезировать мРНК.
В репликации вирусных геномов у ДНК-содержащих вирусов участвуют клеточные ДНКполимеразы. ДНК-содержащие вирусы (за исключением аденовирусов, герпесвирусов и поксивирусов) могут создавать инфекционные нуклеиновые кислоты, потому что для продолжения репродуктивного цикла им не нужны вирусные ферменты: они могут использовать ферменты клетки хозяина.
ПЛЮС-нить РНК-вирусы (полиовирус). Сама по себе +нить РНК является мРНК. Данный тип вирусов может образовывать инфекционные нуклеиновые кислоты: кроме самой +нити РНК для продолжения репродуктивного цикла вируса ничего не нужно.
МИНУС-нить РНК-вирусы. мРНК у таких вирусов синтезируется из негативной нити, которая является матрицей. Вирус несет свою вирусную РНК-зависимую-РНК-полимеразу. Следовательно, данный тип вирусов не может образовывать инфекционные нуклеиновые кислоты: для продолжения репродуктивного цикла вируса, помимо НК, необходимы вирусные ферменты.
102
Двунитевые РНК-вирусы. В данном случае +нить в двойной цепи РНК не может использоваться в качестве мРНК, потому что она связана водородными связями с негативной нитью. Соответственно таким вирусам для продолжения репродуктивного цикла также необходимы свои ферменты (РНК- зависимая-РНК-полимераза), в эукариотических клетках таких ферментов нет. Данный тип вирусов тоже не может образовывать инфекционные нуклеиновые кислоты.
Ретровирусы. Ретровирусы образуют мРНК в два этапа. Сначала +нить РНК (которая у них есть изначально) транскрибируется в двойную нить ДНК с помощью фермента обратной транскриптазы (РНК-зависимой-ДНК-полимеразы), которую несет в клетку хозяина сам вирус.
Затем эта копия ДНК транскрибируется в двойную нить мРНК, с помощью обычной РНК-полимеразы хозяина. данное семейство также не способно к образованию инфекционной нуклеиновой кислоты. Для продолжения репродуктивного цикла им необходима обратная транскриптаза, которая отсутствует в клетках хозяина.
Интегративный способ взаимодействия (вирогения)
Иногда вирусы идут по альтернативному пути, который называется интегративным. При таком взаимодействии вируса с клеткой ДНК вируса интегрируется в хромосому клетки хозяина и нового вирусного потомства при этом не образуется. Вирусная НК продолжает функционировать в интегрированном сайте.
Интерференция вирусов - ингибиторное, действие одного вируса или его компонентов на репродукцию другого вируса и течение инфекционного процесса, вызываемого последним. Первый вирус, называют интерферирующим, а второй — претендующим или интерферируемым. При одновременном введении вирусов возможна двусторонняя интерференция. Используется при лабораторной диагностике и вакцинной профилактике некоторых вирусных инфекций. Интерференция может влиять на течение заболевания, способствуя выздоровлению или, наоборот,
возникновению хрон, патол, состояний (в случае неполной интерференции), а также изменять сроки появления и распространения эпидемий.
2. Диагностикумы, диагностические сыворотки. Классификации, способы получения и область применения. (68)
При обнаружении антител в сыворотке крови больных, реконвалесцентов и бактерионосителей используются серологические реакции.
Для постановки реакций применяются диагностикумы - препараты, содержащие взвесь обезвреженных микроорганизмов или определенные антигены. Для инактивации микроорганизмов при приготовлении диагностикумов чаще всего используются химические вещества, особенно формалин, являющийся лучшим консервантом.
Убитые нагреванием микробы хуже сохраняют антигенные свойства и применяются редко.
Всерологических реакциях (реакции агглютинации, реакции пассивной гемагглютинации, реакции связывания комплемента, реакции торможения гемагглютинации) для выявления специфических антител применяются: бактериальные, эритроцитарные и вирусные диагностикумы. Бактериальные диагностикумы могут содержать инактивированную микробную взвесь или отдельные антигенные компоненты бактерий: О, Н или Vi-антигены и используются в реакциях агглютинации.
Эритроцитарные диагностикумы представляют собой эритроциты (обработанные танином или формалином) с адсорбированными на них антигенами, извлеченными из бактерий, и применяются в РПГА (реакции пассивной гемагглютинации).
Вирусные диагностикумы — препараты, содержащие инактированные вируссодержащие жидкости (культуральные, из куриных эмбрионов или организма животных, зараженных соответствующим вирусом), применяются в РСК (реакции связывания комплемента), реакции торможения гемагглютинации (РТГА) и реакции нейтрализации.
Внастоящее время в лабораториях используются следующие диагностикумы.
1. Бактериальный диагностикум сальмонелл тифа. Применяется в реакции агглютинации для обнаружения антител в сыворотке больных.
2. Сальмонеллезные О-диагностикумы содержат О-антигены различных групп сальмонелл (инактивированных 15%-ным раствором глицерина).
3. Сальмонеллезные Н-монодиагностикумы. Используются в реакции агглютинации для определения заболевания в прошлом (анамнестическая реакция агглютинации) и реже с диагностической целью.
103
4.Vi — брюшнотифозный диагностикум. Применяется в реакции агглютинации при выявлении брюшнотифозного бактерионосительства.
5.Единый бруцеллезный диагностикум — взвесь бруцелл (инактивированных фенолом), подкрашенная метиленовым синим. Применяется для определения антител в сыворотках крови больных бруцеллезом людей и животных в реакциях агглютинации Райта и Хеддльсона.
6.Эритроцитарный сальмонеллезный О-диагностикум — взвесь эритроцитов с адсорбированными на них О-антигенами различных групп сальмонелл.
7.Эритроцитарный Vi-диагностикум — эритроциты, сенсибилизированные очищенным Viантигеном S. typhi, применяется в РПГА при выявлении брюшнотифозного бактерионосительства.
8.Гриппозный диагностикум представляет собой аллантоисную жидкость инфицированных вирусом гриппа (типов А, В) куриных эмбрионов и инактивированную мертиолатом или формалином.
9.Диагностикум вируса клещевого энцефалита получают из суспензии мозга белых мышей, зараженных вирусом клещевого энцефалита.
3. Микоплазмы. Таксономия и биологическая характеристика. Эпидемиология и патогенез заболеваний. Роль в патологии человека. Микробиологическая диагностика. Лечение. (129)
Антропонозные бактериальные инфекции человека, поражающие органы дыхания или мочеполовой тракт. Микоплазмы относятся к классу Mollicutes.
Морфология: Отсутствие ригидной клеточной стенки, полиморфизм клеток, пластичность, осмотическую чувствительность, резистентность к различным агентам, подавляющим синтез клеточной стенки, в том числе к пенициллину и его производным. Грам «-», лучше окрашиваются по Романовскому—Гимзе; различают подвижные и неподвижные виды.
Клеточная мембрана находится в жидкокристаллическом состоянии; включает белки, погруженные в два липидных слоя, основной компонент которых — холестерин.
Культуральные свойства. Хемоорганотрофы, основной источник энергии — глюкоза или аргинин. Растут при температуре 30С. Большинство видов — факультативные анаэробы; чрезвычайно требовательны к питательным средам и условиям культивирования. Питательные среды (экстракт говяжьего сердца, дрожжевой экстракт, пептон, ДНК, глюкоза, аргинин). Культивируют на жидких, полужидких и плотных питательных средах.
Биохимическая активность: Выделяют 2 группы микоплазм:
1. разлагающие с образованием кислоты глюкозу, мальтозу, маннозу, фруктозу, крахмал и гликоген; 2.окисляющие глутамат и лактат, но не ферментирующие углеводы.
Все виды не гидролизуют мочевину.
Антигенная структура: основные АГ представлены фосфо- и гликолипидами, полисахаридами и белками; наиболее иммунногенны поверхностные АГ, включающие углеводы в составе сложных гликолипидных, липогликановых и гликопротеиновых комплексов.
Факторы патогенности: адгезины, токсины, ферменты агрессии и продукты метаболизма. Адгезины входят в состав поверхностных АГ и обуславливают адгезию на клетках хозяина. Предполагают наличие нейротоксина у некоторых штаммов М. pneumoniae, так как часто инфекции дыхательных путей сопровождают поражения нервной системы.
Эндотоксины выделены у многих патогенных микоплазм. У некоторых видов встречаются гемолизины. Среди ферментов агрессии основными факторами патогенности являются фосфолипаза А и аминопептидазы, гидролизующие фосфолипиды мембраны клетки.
Эпидемиология: М. pneumoniae колонизирует слизистую оболочку респираторного тракта; M. hominis, M. genitaliumu U. urealyticum— «урогенитальные микоплазмы» — обитают в урогенитальном тракте. Источник инфекции — больной человек. Механизм передачи — аэрогенный, основной путь передачи
— воздушно-капельный.
Патогенез: Проникают в организм, мигрируют через слизистые оболочки, прикрепляются к эпителию через гликопротеиновые рецепторы. Вызывают нарушения свойств клеток с развитием местных воспалительных реакций.
Клиника: Респираторный микоплазмоз - в форме инфекции верхних дыхательных путей, бронхита, пневмонии.
Внереспираторные проявления: гемолитическая анемия, неврологические расстройства, осложнения со стороны ССС.
Иммунитет: для респираторного и урогенитального микоплазмоза характерны случаи повторного заражения.
104

Микробиологическая диагностика: мазки из носоглотки, мокрота, бронхиальные смывы. При урогенитальных инфекциях исследуют мочу, соскобы с уретры, влагалища.
Используют культуральный, серологический и молекулярно-генетический методы.
При серодиагностике материалом для исследования служат мазки-отпечатки тканей, соскобы из уретры, влагалиша, в которых можно обнаружить АГ микоплазм в прямой и непрямой РИФ.
Микоплазмы и уреаплазмы выявляются в виде зеленых гранул. АГ микоплазм могут быть обнаружены также в сыворотке крови больных. Для этого используют ИФА.
Для серодиагностики респираторного микоплазмоза определяют специфические AT в парных сыворотках больного.
При урогенитальных микоплазмозах в ряде случаев проводят серодиагностику, AT определяют чаше всего в РПГА и ИФА. Лечение. Антибиотики. Этиотропная химиотерапия.
4. Иммуноферментный анализ (ИФА). Механизм, компоненты, применение. (88)
ИФА— иммуноферментный анализ.
Иммуноферментный анализ — выявление антигенов с помощью соответствующих им антител, конъюгированных с ферментом-меткой (пероксидазой хрена, бета-галактозидазой или щелочной фосфатазой).
После соединения антигена с меченной ферментом иммунной сывороткой в смесь добавляют субстрат/хромоген. Субстрат расщепляется ферментом и изменяется цвет продукта реакции — интенсивность окраски прямо пропорциональна количеству связавшихся молекул антигена и антител. ИФА применяют для диагностики вирусных, бактериальных и паразитарных болезней, в частности для диагностики ВИЧ-инфекций, гепатита В и др., а также определения гормонов, ферментов, лекарственных препаратов и других биологически активных веществ, содержащихся в исследуемом материале в минорных концентрациях (1010 -1012 г/л).
Твердофазный ИФА— вариант теста, когда один из компонентов иммунной реакции (антиген или антитело) сорбирован на твердом носителе, напр., в лунках планшеток из полистирола. Компоненты выявляют добавлением меченых антител или антигенов. При положительном результате изменяется цвет хромогена. Каждый раз после добавления очередного компонента из лунок удаляют несвязавшиеся реагенты путем промывания,
I. При определении антител (левый рисунок) в лунки планшеток с сорбированным антигеном последовательно добавляют сыворотку крови больного, антиглобулиновую сыворотку, меченную ферментом, и субстрат/хромоген для фермента.
II. При определении антигена (правый рисунок) в лунки с сорбированными антителами вносят антиген (напр., сыворотку крови с искомым антигеном), добавляют диагностическую сыворотку против него и вторичные антитела (против диагностической сыворотки), меченные ферментом, а затем субстрат/хромоген для фермента.
Конкурентный ИФА для определения антигенов: искомый антиген и меченный ферментом антиген конкурируют друг с другом за связывание ограниченного количества антител иммунной сыворотки. (рис 1)
Другой тест - Конкурентный ИФА для определения антител: искомые антитела и меченные ферментом антитела конкурируют
друг с другом за антигены, сорбированные на Рисунок 2 твердой фазе.
105
Иммуноблоттинг — высокочувствительный метод выявления белков, основанный на сочетании электрофореза и ИФА или РИА. Иммуноблоттинг используют как диагностический метод при ВИЧинфекции и др. Антигены возбудителя разделяют с помощью электрофореза в полиакриламидном геле, затем переносят их из геля на активированную бумагуили нитроцеллюлозную мембрану и проявляют с помощью ИФА. Фирмы выпускают такие полоски с «блотами» антигенов. На эти полоски наносят сыворотку больного. Затем, после инкубации, отмывают от несвязавшихся антител больного и наносят сыворотку против иммуноглобулинов человека, меченную ферментом.
Образовавшийся на полоске комплекс [антиген + антитело больного + антитело против Ig человека] выявляют добавлением хромогенного субстрата, изменяющего окраску под действием фермента.
Билет 28 1. Общая характеристика вирусов. Определение, биологическое значение, отличия от других микроорганизмов. (26)
Вирусы – субмикроскопические неклеточные организмы, способные размножаться только внутри живых клеток (облигатные паразиты). Они относятся к отдельному царству живых организмов – Царство Вирусы.
Значение:
Регуляция численности видов
Трансдукция
Возбудитель заболеваний человека, животных, растений
Бактериофаги
Борьба с вредителями
Перенос генов в генной инженерии
Характеристика: молекулярная (неклеточная) структура;
геном представлен только одним типом нуклеиновой кислоты (ДНК или РНК); количество цепей (1 или 2) и их структура у разных вирусов существенно отличаются;
вирусы обладают наследственностью и выраженной изменчивостью;
размножение вирусов происходит только в зараженных ими клетках;
вирусы не обладают собственными системами синтеза белка и генерации энергии; для репродукции используют белоксинтезирующие и энергетические системы клеток хозяина;
имеют минимальный размер (обычно в пределах от 10-20 до 400 нм);
Отличия:
▪Неклеточное строение
▪размножаются только в клетках других организмов, используя их вещество и энергию
▪вирусы содержат только одну из нуклеиновых кислот — ДНК или РНК
▪у вирусов отсутствует собственная система обмена веществ
▪в жизненном цикле вирусов наблюдаются две стадии — покоя и репликации
▪неинтегральный способ репродукции
▪отсутствие транскрипционно-трансляционного комплекса.
Основные методы культивирования вирусов.
1.В организме лабораторных животных.
2.В куриных эмбрионах.
3.В клеточных культурах - основной метод.
Типы клеточных культур.
1.Первичные (трипсинизированные) культурыфибробласты эмбриона курицы (ФЭК), человека (ФЭЧ), клетки почки различных животных и т.д. Первичные культуры получают из клеток различных тканей чаще путем их размельчения и трипсинизации, используют однократно, т.е. постоянно необходимо иметь соответствующие органы или ткани.
2.Линии диплоидных клеток пригодны к повторному диспергированию и росту, как правило не более 20 пассажей (теряют исходные свойства).
3.Перевиваемые линии (гетероплоидные культуры), способны к многократному диспергированию и перевиванию, т.е. к многократным пассажам, наиболее удобны в вирусологической работенапример, линии опухолевых клеток Hela, Hep и др.
106
В зависимости от функционального использования среды могут быть ростовые (с большим содержанием сыворотки крови) - их используют для выращивания клеточных культур до внесения вирусных проб, и поддерживающие (с меньшим содержанием сыворотки или ее отсутствием)- для содержания инфицированных вирусом клеточных культур.
Выявляемые проявления вирусной инфекции клеточных культур.
1.Цитопатический эффект.
2.Выявление телец включений.
3.Выявление вирусов методом флюоресцирующих антител (МФА), электронной микроскопией, авторадиографией.
4.Цветная проба. Обычный цвет используемых культуральных сред, содержащих в качестве индикатора рН феноловый красный, при оптимальных для клеток условиях культивирования (рН около 7,2)- красный. При размножении в клеточных культурах вирусов происходит лизис клеток, изменения рН и цвета среды не происходит.
5.Выявление гемагглютинина вирусовгемадсорбция, гемагглютинация.
6.Метод бляшек (бляшкообразования). В результате цитолитического действия многих вирусов на клеточные культуры образуются зоны массовой гибели клеток. Выявляют бляшкивирусные “ клеточнонегативные” колонии
2. Клетки иммунной системы. Характеристика иммунокомпетентных и антигенпрезентирующих клеток. (66)
Все клетки, относящиеся к иммунной системе и привлекаемые ею для обеспечения эффекторных реакций, в функциональном отношении условно разделяют на четыре группы.
1.Антигенпрезентирующие клетки: макрофаги, дендритные клетки типов 1 и 2, В-лимфоциты.
2.Регуляторные клетки: T-индукторы, Т-хелперы типов 1, 2 и 3, естественные регуляторные Т-клетки.
3.Эффекторные клетки: плазматические клетки (дифференцирующиеся из В-лимфоцитов), цитотоксические Т-клетки с фенотипом CD8+ (или T-киллеры); эффекторные Т-клетки воспаления с фенотипом CD4+ (или Т-лимфоциты, ответственные за гиперчувствительность замедленного типа); нейтрофилы, эозинофилы, базофилы, тучные клетки, натуральные киллеры (NK-клетки), макрофаги.
4.Клетки памяти: Т-клетки памяти с фенотипом CD8+; Т-клетки памяти с фенотипом CD4+; долгоживующие плазматические клетки; В-клетки памяти.
Лимфоциты как главные клетки иммунной системы имеют отличительные особенности:
1.Постоянная «патрульная» рециркуляция по кровотоку, лимфотоку, межтканевым пространствам и секретам.
2.Способность распознавать, т.е. взаимодействовать со «своим» и «чужим» по принципу «лиганд - рецептор».
3.Клональная (или групповая) организация и способность формировать сетевые элементы.
4.Способность к непрерывным реаранжировкам в своем геноме в любом возрасте в связи с потребностями формирования специфического ответа на патоген.
5.Умение запоминать антигены и обеспечивать в будущем экспрессный высокоэффективный антигенспецифический ответ.
Клон - это группа лимфоцитов, коммитированных к определенному антигену. До встречи с этим антигеном каждый лимфоцит клона называют наивным. По-видимому, в человеческом организме исходно существуют десятки миллионов клонов Т- и В-лимфоцитов. После контакта с соответствующим антигеном и в результате иммунного ответа коммитированный лимфоцит становится праймированным.
3. Возбудитель бореллиозов (возвратный тиф). Таксономия и биологическая характеристика. Эпидемиология и патогенез заболеваний. Микробиологическая диагностика. Особенность циркуляции в Волгоградской области. (128)
Семейство Spirochaetaceae, род Borrelia.
Вызывают эпидемический и эндемический возвратные тифы, болезнь Лайма. Спирохеты рода Borreliaвызывают антропонозные (возвратный тиф), зоонозные (болезни Лайма) инфекционные болезни с трансмиссивным механизмом передачи возбудителей (клещи, вши). Морфологические свойства: тонкие спирохеты с крупными завитками. Двигательный аппарат
представлен фибриллами. Они хорошо воспринимают анилиновые красители, по Романовскому—Гимзе окрашиваются в синефиолетовый цвет.
107
Культуральные свойства: культивируются на сложных питательных средах, содержащих сыворотку, тканевые экстракты, а также в куриных эмбрионах. Чувствительны к высыханию и нагреванию. Устойчивы к низким t-рам.
Возвратные тифы — группа острых инфекционных заболеваний, вызываемых боррелиями, характеризующихся острым началом, приступообразной лихорадкой, общей интоксикацией. Различают эпидемический и эндемический возвратные тифы. Возбудителем эпидемического возвратного тифа является В. recurrentis.
Эпидемический возвратный тиф - антропоноз. Специфические переносчики - платяная, головная вши. Человек заражается возвратным тифом при втирании гемолимфы раздавленных вшей в кожу при расчесывания места укуса.
Эндемический возвратный тиф— зооноз. Возбудители - В. duttoniи В. persica. Резервуар - грызуны, клещи. Человек заражается через укусы клещей.
Патогенез: Попав во внутреннюю среду организма, боррелии внедряются в клетки лимфоидномакрофагальной системы, где размножаются и поступают в кровь, вызывая лихорадку, головную боль, озноб.
Взаимодействуя с АТ, боррелии образуют агрегаты, которые нагружаются тромбоцитами, вызывая закупорку капилляров, следствием чего является нарушение кровообращения в органах. Иммунитет: к эпидемическому возвратному тифу гуморальный, непродолжительный.
Микробиологическая диагностика.
Бактериоскопический метод — обнаружение возбудителя в крови, окрашенной по Романовскому— Гимзе. Биопробу ставят для дифференциации В. recurrentisот возбудителей эндемического возвратного тифа.В качестве вспомогательного используют серологический метод с постановкой РСК.
Лечение: антибиотики тетрациклинового ряда, левомицетин, ампициллин. Профилактика. Неспецифическая.
Болезнь Лайма - возбудитель В. burgdorferi. Хроническая инфекция с поражением кожи, сердечной и нервной систем, суставов.
Морфология и культуральные свойства: типичные боррелии.
Антигенная структура: Сложная. Белковые антигены фибриллярного аппарата и цитоплазматического цилиндра, антитела к которым появляются на ранних этапах инфекции. Протективную активность имеют антигены, представленные липидмодифицированными интегральными белками наружной мембраны А, В, С, D, E, F.
Факторы патогенности. Липидмодифицированные белки наружной мембраны обеспечивают способность боррелий прикрепляться и проникать в клетки хозяина. В результате взаимодействия боррелий с макрофагами происходит выделение ИЛ-1, который индуцирует воспалительный процесс. Патогенез: На месте укуса клеща образуется красная папула.
Возбудитель распространяется из места укуса через окружающую кожу с последующей диссеминацией с током крови к различным органам, особенно сердцу, ЦНС, суставам.
Клиника подразделяется на 3 стадии:
1.Мигрирующая эритема, которая сопровождается развитием гриппоподобного симптомокомплекса. 2.Развитие доброкачественных поражений сердца и ЦНС 3.Развитие артритов крупных суставов
Иммунитет. Гуморальный, видоспецифический к антигенам клеточной стенки. Микробиологическая диагностика. Используются бактериоскопический, серологический методы и ПЦР в зависимости от стадии заболевания.
Материалом для исследования служат биоптаты кожи, синовиальная жидкость суставов, ликвор, сыворотка крови.
На 1-й стадии заболевания проводится бактериологическое исследование биоптатов кожи из эритемы. 2-й стадии заболевания осуществляется серологическое исследование определением IgM или нарастания титра IgG ИФА или РИФ.
ПЦР используется для определения наличия боррелий в ликворе, суставной жидкости. Лечение: антибиотики тетрациклинового ряда. Профилактика. Неспецифическая.
108
4. Реакция преципитации. Механизм, компоненты, способы постановки, области применение. (81)
Реакция преципитации — это формирование и осаждение комплекса растворимого молекулярного антигена c антителами в виде помутнения, называемого преципитатом. Он образуется при смешивании антигенов и антител в эквивалентных количествах; избыток одного из них снижает уровень образования иммунного комплекса.
Реакции преципитации ставят в пробирках (реакция кольцепреципитации), в гелях, питательных средах и др. К вариантам реакции преципитации в полужидком геле агара или агарозы относят двойную иммунодиффузию по Оухтерлони, радиальную иммунодиффузию, иммуноэлектрофорез и др.
Ее используют при диагностике сибирской язвы, чумы, туляремии, менингита. Реакцию кольцепреципитации
Ставят в узких преципитационных пробирках с иммунной сывороткой, на которую наслаивают растворимый антиген. При оптимальном соотношении антигена и антител на границе этих двух растворов образуется непрозрачное кольцо преципитата.
Если в качестве антигенов используют прокипяченные и профильтрованные водные экстракты органов или тканей, то такая реакция называется реакцией термопреципитации (реакция Асколи при сибирской язве).
Реакция двойной иммунодиффузии по Оухтерлони.
Растопленный агаровый гель тонким слоем выливают на стеклянную пластинку и после его затвердевания в нем вырезают лунки размером 2–3 мм.
Вэти лунки раздельно помещают антигены и иммунные сыворотки, которые диффундируют навстречу друг другу.
Вместе встречи в эквивалентных соотношениях они образуют преципитат в виде белой полосы.
Реакция радиальной иммунодиффузии.
Иммунную сыворотку с расплавленным агаровым гелем равномерно наливают на стекло. После застывания в геле делают лунки, в которые помещают антиген в различных разведениях.
Антиген, диффундируя в гель, образует с антителами кольцевые зоны преципитации вокруг лунок. Диаметр кольца преципитации пропорционален концентрации антигена. Составляют калибровочную кривую, по которой определяют концентрацию антигена в исследуемом образце.
Реакцию используют для определения содержания в крови иммуноглобулинов различных классов, компонентов системы комплемента и др.
Иммуноэлектрофорез — сочетание метода электрофореза и иммунопреципитации: смесь антигенов вносится в лунки геля и разделяется в геле с помощью электрофореза.
Затем в канавку параллельно зонам электрофореза вносят иммунную сыворотку, антитела которой, диффундируя в гель, образуют в месте «встречи» с антигеном линии преципитации.
Реакция флоккуляции по Рамону— появление хлопьевидной массы в пробирке при реакции токсин– антитоксин или анатоксин–антитоксин. Ее применяют для определения активности антитоксической сыворотки или анатоксина.
Билет 29 1. Методы культивирования вирусов и их идентификация, и индикация. (29)
Культивирование вирусов проводят для диагностики вирусных инфекций, для изучения вопросов патогенеза и иммунитета, для получения диагностических и вакцинных препаратов.
Для культивирования вирусов используют лабораторных животных, развивающиеся куриные
эмбрионы, культуры клеток.
Лабораторных животных разными способами заражают (учитывают тропизм вирусов:
ортомиксовирусами заражают интраназально, нейровирусами – субдурально).
Куриный эмбрион является удобной моделью для культивирования вирусов, т.к. полости его стерильны, защищены твердой оболочкой.
Индикацию вируса в курином эмбрионе проводят:
по гибели эмбриона;
помутнению хорион-аллантоисной оболочки;
образованию бляшек на оболочке;
в реакции гемагглютинации (происходит склеивание эритроцитов под действием гемагглютинина вирусов, который расположен в шипах суперкапсида).
109
Метод культур клеток. Для приготовления культур клеток используют различные ткани человека и животных.
Чаще применяют культуры клеток из эмбриональных (куриные фибробласты, человеческие
фибробласты) и опухолевых (злокачественно перерожденных) тканей, обладающих активной способностью к росту и размножению.
Различают три типа культур клеток:
однослойные культуры клеток;
Однослойные культуры клеток по числу жизнеспособных генераций разделяют на первичные или первично трипсинизированные (куриные и человеческие фибробласты); перевиваемые (способны размножаться в лабораторных условиях длительное время); полуперевиваемые диплоидные (способны размножаться в течение 40-50 пассажей).
Для культивирования питательные среды, делятся на ростовые и поддерживающие.
Всоставе ростовых питательных сред должно содержаться больше питательных веществ, чтобы обеспечить активное размножение клеток для формирования монослоя. Неотъемлемый компонент большинства ростовых сред – наличие 5-10 % сыворотки крови животных (телячьей, бычей, лошадиной).
Поддерживающие среды должны обеспечивать лишь переживание клеток в уже сформированном монослое при размножении в клетке вирусов.
Для культур клеток используется - раствор Хенкса.
Всостав поддерживающих сред сыворотка не входит.
культуры суспензированных клеток;
Культуры суспензированных клеток растут и размножаются во взвешенном состоянии при постоянном интенсивном перемешивании среды. Они используются для накопления вирусов.
органные культуры.
Некоторые вирусы размножаются в органных культурах – это кусочки органов, выращенные вне организма и сохраняющие структуру данного органа.
Оразмножении вируса в культуре клеток судят по:
цитопатогенному действию (ЦПД);
Цитопатогенное действие может проявляться полной дегенерацией клеток – слущиванием клеток с поверхности стекла после их гибели (энтеровирусы полиомиелита, Коксаки); частичной дегенерацией – округлением клеток, слиянием и образованием симпластов (вирус кори).
При отсутствии ЦПД можно поставить реакцию интерференйии – исследуемая культура повторно заражается вирусом, вызывающим ЦПД.
В положительном случае ЦПД будет отсутствовать (реакция интерференции положительная), если в исследуемом материале вируса не было, наблюдается ЦПД.
образованию в клетках включений;
Образование включений в клетках – это скопление вирионов или отдельных компонентов в цитоплазме или в ядре клеток, выявляемые под микроскопом при специальном окрашивании. Вирус натуральной оспы образует цитоплазматические включения – тельца гварниери, вирусы герпеса, аденовирусы – внутриядерные включения.
появлению бляшек;
Появление бляшек – зоны клеток, разрушенных вирусом (негативные колонии вирусов), обнаруживают в клеточных культурах, растущих на стекле и покрытых тонким слоем агара.
Бляшки различаются по величине, форме, времени появления, поэтому данный тест используют для дифференциации вирусов.
феномену гемадсорбции;
Реакция гемадсорбции заключается в способности клеток, зараженных вирусами, адсорбировать на своей поверхности эритроциты, потому что эти клетки несут на поверхности гемагглютинины вируса.
цветной пробе.
Цветная реакция основана на изменении цвета питательной среды с индикатором, используемой для культур клеток. При росте клеток, не пораженных вирусом, идет накопление продуктов метоболизма, которые изменяют цвет питательной среды. При репродукции вирусов в культуре нарушается метаболизм клеток, и среда сохраняет первоначальный цвет.
110
