Химия курсовая
.docx-
Физико-химические свойства
АЦЕТИЛЕН- углеводород состава С2Н2, содержащий тройную углерод-углеродную связь.
Он легче воздуха, масса 1 м3 ацетилена при температуре 20 °С (273 К) и нормальном атмосферном давлении составляет 1,09 кг. При нормальном давлении и температуре от –82,4 °С (190,6 К) до –84,0 °С (189 К) ацетилен переходит в жидкое состояние, а при температуре –85 °С (188 К) затвердевает, образуя кристаллы.
Он представляет собой бесцветный газ, обладающий в чистом виде слабым эфирным запахом и сладковатым вкусом. Малорастворим в воде, хорошо растворяется в ацетоне.
В промышленности ацетилен получают при разложении жидких горючих, таких как нефть, керосин, воздействием электродугового разряда. Промышленный ацетилен закачивается в баллоны, где находится в порах специальный массы растворенным в ацетоне.
Ацетилен так же используют :
-для сварки и резки металлов
-как источник очень яркого, белого света в автономных светильниках, где он получается реакцией карбида кальция и воды (карбидная лампа)
-в производстве взрывчатых веществ
-для получения уксусной кислоты, этилового спирта, растворителей, пластических масс, каучука, ароматических углеводородов.
-для получения технического углерода
-в атомно-абсорбционной спектрофотометрии при пламенной атомизации
-в ракетных двигателях (вместе с аммиаком)
Синоним: этин.
Формула в виде текста: C2H2
Молекулярная масса (в а.е.м.): 26,038
Температура плавления(затвердевания) (при 760 мм рт. ст.), °С -85
Температура кипения (в ˚С): -81,8
Плотность: 0,001173
Критическая температура, °С 35,9
Критическое давление, кгс Низшая удельная теплота сгорания, кДж/м3 55890
Температура самовоспламенения, °С : 335/см2
Температура при сгорании пламени °C : 3150 °C
Растворимость ацетилена : Газообразный ацетилен может растворяться во многих жидкостях.
Ацетилен с водой, в присутствии солей ртути и других катализаторов, образует уксусный альдегид.
Химические свойства:
Ацетилен может полимеризироваться в бензол и другие органические соединения (полиацетилен, винилацетилен). Для полимеризации в бензол необходим графит и температура в 400 °C.
Кроме того, атомы водорода ацетилена относительно легко отщепляются в виде протонов, то есть он проявляет кислотные свойства. Так ацетилен вытесняет метан из эфирного раствора метилмагнийбромида, образует нерастворимые взрывчатые осадки с солями серебра и одновалентной меди.
При использовании ацетилена необходимо учитывать его взрывоопасные свойства. Это единственный широко применяемый в промышленности газ, горение и взрыв которого возможны даже при отсутствии кислорода или других окислителей.
2. Расчет термодинамических величин
1. Реакция горения в воздухе:
2C2H2 + 5(O2 + 3,75N2) = 4CO2 + 2H2O + 18,75N2
2. Табличное значение стандартной энтальпии сгорания ацетилена:
∆H0298, сгор. = -1299,63 кДж/моль
Следовательно, высшая энтальпия сгорания топлива (∆H0в, кДж/моль топлива) равна:
∆H0в = ∆H0сгор.топлива = -1299,63 кДж/моль
3. Высшая теплота сгорания топлива (МДж/кг топлива):
Qв
=
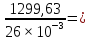 49,99
МДж/кг C2Н2.
49,99
МДж/кг C2Н2.
4. Низшая энтальпия сгорания (∆H0н, кДж/моль топлива) отличается от высшей на величину энтальпии конденсации водяного пара ∆H0конд. H2O(пар) = -44,01 кДж/моль. Поэтому
∆H0н = ∆H0сгор.топлива - ∆H0конд.H2O(пар) = -1299,63 + 2 ⋅ 44,01 = -1211,61.
5. Низшая теплота сгорания топлива (МДж/кг топлива):
Qн
=
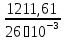 = 46,6.
= 46,6.
6. Теоретически необходимое количество воздуха для полного сгорания 1 кг топлива (кг воздуха / кг топлива):
L0воздуха
=
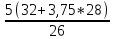 =
10,192.
=
10,192.
7. Количество топливовоздушной смеси (М1, моль):
М1 = 1 мольтоплива + 5(1 + 3,75) = 24,75.
8. Низшая теплота сгорания топливовоздушной смеси (qн, кДж/м3), она же калорийность стехиометрической смеси топлива с воздухом:
qн
=
 = 2185.
= 2185.
Сравнительные характеристики (Qн, L0воздуха, qн) ацетилена и бензина.
|
Характеристики |
Бензин |
Ацетилен |
|
|
Справочные данные |
Расчет |
||
|
Низшая теплотворная способность, Qн (МДж/кг) |
43,3-44,0 |
- |
|
|
Низшая теплота сгорания топливовоздушной смеси, qн (кДж/м3) |
3439-3910 |
3632 |
2185 |
|
Стехиометрическая потребность воздуха в процессе сгорания, Lовоздуха (кг воздуха / кг топлива_ |
14,9 |
- |
10,192 |
-
Характерные химические реакции
Реакции получения и горения ацетилена:
CaC2 + 2H2O → Ca(OH)2 + C2H2 2C2H2 + 5O2 → 4CO2 +2H2O +2600 кДж
Для ацетилена (этина) характерны реакции присоединения:
HC≡CH + Cl2 -> СlСН=СНСl
Гидратация (присоединение воды)
CH≡CH + H2O → CH3 − C═ O │ (H уксусный альдегид)
CH3 − C(O)H→ CH3 – COOH (уксусная кислота)
Реакции гидрогалогенирования и полимеризации
CH≡CH + HCl → CH2 ═ CHCl (винилхлорид)
CH2═ CH + CH2═ CH +…→ (− CH2 − CH−) │ │ │ Cl Cl Cl
4. Выводы
Наилучшими заменителями ацетилена являются сжиженные нефтяные газы - пропан, бутан и их смеси, а также природные газы.
Успешно решена учеными и работниками производства задача по замене ацетилена пропан-бутаном и природным газом при сварке чугуна различной толщины, углеродистой стали толщиной до 5 мм и цветных металлов.
Однако, преимущество ацетилена – в самой высокой температуре горения, которая достигает 3100 ° С. Именно поэтому газопламенная обработка ответственных узлов машиностроительных конструкций производится только с помощью ацетилена, который обеспечивает наивысшую производительность и качество процесса сварки.