
- •Модуль II
- •Химические св-ва
- •Номенклатура солей
- •Фенолокислоты
- •Оксокислоты
- •Номенклатура
- •Вопросы для самоконтроля:
- •Упражнения
- •Лабораторная работа «Свойства оксикислот»
- •Тесты для самостоятельной работы студентов Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Ответы к тестам “ Окси-, оксокислоты ”
Модуль II
Тема занятия №1 “ Биологически активные гидрокси- и оксокислоты ”
Цель занятия: изучение электронного, пространственного строения и химических свойств биологически важных гидрокси- и оксокислот.
Студент должен знать:
- особенности свойств оксо - , гидрокси - и фенолокислот.
Студент должен уметь:
- объяснить химическое поведение гидроксикислот в организме;
- объяснять кето-енольную таутомерию, роль этого фактора в биохимии организма.
Гидрокси-, или оксикислоты
Это соединения, содержащие одну или несколько групп –ОН и –СООН.
В
общем виде их формулу можно представить
 .
В простейшем случаеn
= m
= 1. Количество гр. –СООН определяет
основность, а гр. –ОН – атомность.
.
В простейшем случаеn
= m
= 1. Количество гр. –СООН определяет
основность, а гр. –ОН – атомность.
Номенклатура
гликолевая
к-та, a-оксиуксусная
к-та, 2-гидроксиэтановая
к-та,
С
молочная
к-та, a-оксипропионовая
к-та, 2-оксипропановая
к-та, винная
к-та, a,b-диоксиянтарная
к-та, 2,3-диоксибутандиовая
к-та,
НООС–
Н
лимонная
к-та, 3-гидрокси- 3-карбоксипентандиовая
к-та, ![]() СН2
–СООН
СН2
–СООН
Изомерия
Молекулы с тремя атомами углерода проявляют изомерию положения гр. –ОН, а с четырьмя – изомерию положения и углерод – углеродной цепи. Например,
СН3–СН2– ,
СН3–
,
СН3–![]() –СН2
–СООН,
–СН2
–СООН,
![]() –СН2–СН2–СООН,
–СН2–СН2–СООН,
a-оксимасляная к-та b-оксимасляная к-та g-оксимасляная к-та
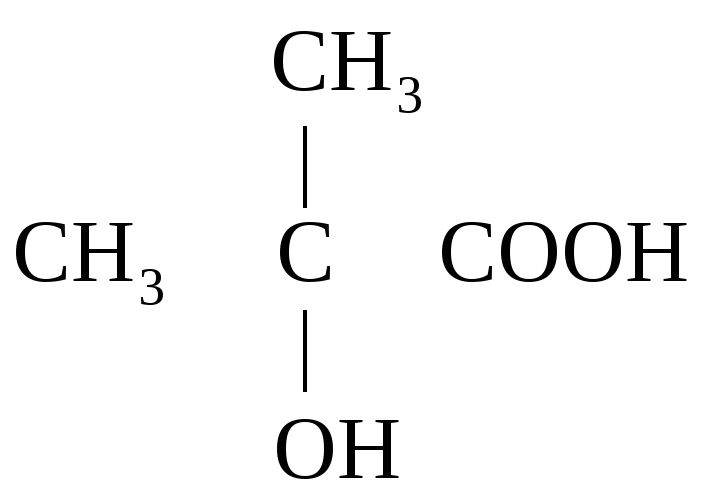 a-оксиизомасляная
к-та
a-оксиизомасляная
к-та
В молочной к-те появляется ассиметрический (хиральный) атом С, а следовательно, имеются оптические изомеры. Оптическая изомерия свойственна для многих оксикислот.
СООН СООН
D-(–) – Молочная к-та L-(+) – Молочная к-та
Винная к-та имеет два ассиметрических атома С. Однако всего изомеров только три, а не четыре (2n), и оптически активных лишь два, т.к. два одинаковых заместителя (гр. –ОН) создают в молекуле плоскость симметрии.
НО Н Н Н НО


Мезовинная к-та D-(+) – Винная к-та L-(–) – Винная к-та
Знак вращения плоскости поляризации света нельзя связывать с отнесением соединений к D – и L – рядам. Знак «+» и «–» определяют прибором - поляриметром. Для соединений с двумя ассиметрическими атомами С определение принадлежности к D – и L – ряду затруднено. По договоренности определяют D – и L – ряды по близлежащему заместителю от старшей функциональной группы, а в углеводах – по положению заместителя у дальнего от старшей функциональной группы атома С.
Химические св-ва
Наличие в молекуле двух функциональных групп приводит к тому, что эти соединения проявляют характерные р-ции как для к-т, так и для спиртов.
За счет взаимного влияния двух групп происходит усиление реакционной способности каждой из них. Кроме того для них возможны специфические р-ции с участием обеих групп.
R
– –I,
– М
–I,
– М
–I –I, +М
I. Р-ции по гр. –СООН
Оксик-ты диссоциируют, образуют соли, сложные эфиры, амиды, ангидриды, галогенангидриды.
СН3–
 Û
СН3–
Û
СН3– + Н+.
+ Н+.
Молочная к-та Лактат-анион
Окси-ты являются более сильными к-тами, чем соответствующие им карбоновые к-ты, что находит объяснение в ЭА характере групп – ОН и – СООН. Например, a-оксиуксусная к-та в 5 раз сильнее уксусной к-ты.
Соли образуются легко с различными веществами Ме, МеО, МеОН, МеСО3, где Ме – активный металл.
СН3–
 +NaOH
®
СН3–
+NaOH
®
СН3– +Н2О.
+Н2О.
Молочная к-та Лактат натрия
Двухосновные к-ты образуют средние и кислые соли. Кислые соли, как правило, мало растворимы в воде, средние – хорошо растворимы. Это используют для обнаружения ионов К+ в фармации и в аналитической химии:
НООС
-
![]() -
-![]() + КОН
+ КОН![]() КООС
-
КООС
-![]() -
-![]() ¯
¯
Винная к-та Гидротартрат калия
Смешанная К–Na соль винной к-ты наз-ся сегнетовой солью.
