
- •РАЗДЕЛ 3
- •Вид используемого электромагнитного излучения
- •20.3.3. Практическое применение
- •Фотометрические реакции
- •Дифференциальная (разностная) фотометрия
- •Производная спектрофотометрия
- •20.5.1. Процессы, приводящие к появлению аналитического сигнала
- •20.5.2. Общая характеристика ИК-спектров
- •20.5.3. Измерение аналитического сигнала
- •20.5.4. Практическое применение
- •21.1.1. Процессы, приводящие к появлению аналитического сигнала
- •21.1.2. Измерение аналитического сигнала
- •21.1.3. Практическое применение
- •Природа вещества
- •Способы получения хроматограммы
- •Хроматографические характеристики, используемые для идентификации веществ (характеристики удерживания)
- •Хроматографические характеристики, используемые для количественного определения веществ
- •Хроматографическая колонка
- •Детекторы
- •Табл. 23.1
- •Характеристика некоторых газохроматографических детекторов
- •ГЛАВА 24
- •24.2.1. Методика получения плоскостной хроматограммы
- •Способы получения плоскостных хроматограмм
- •Некоторые реагенты-проявители, используемые в
- •плоскостной хроматографии
- •Неподвижные и подвижные фазы
- •Ионообменное равновесие
- •ГЛАВА 25
- •Табл. 25.1.
- •Табл. 25.2
- •ГЛАВА 26
- •26.1.5. Потенциометрическое титрование
- •ГЛАВА 27
- •Некоторые современные разновидности вольтамперометрии
- •Предисловие ...................................................................................
- •9.2. Жидкость-жидкостная экстракция ...........................................................
- •9.2.5. Применение экстракции .........................................................................
- •23.1. Общая характеристика .............................................................................
- •Литература .....................................................................................
Раздел 3
|
Вэн |
Eисп |
|
h испNисп |
|
исп |
Вкв |
|
|
Eпогл |
h поглNпогл |
погл |
|||||
|
|
|
|
|
|
|||
Поскольку обычно исп < погл, то Вэн < Вкв Квантовый выход люминесценции не зависит от возб вплоть до
некоторой , находящейся в области наложения спектров поглощения и испускания, после чего резко уменьшается. Энергетический выход зависит от возб: вначале он увеличивается прямо пропорциональновозб , затем на некотором интервале не изменяет своей величины, после чего резко уменьшается (закон Вавилова).
21.2.4. Влияние различных факторов на интенсивность флуоресценции растворов
Люминесценция и, в частности, флуоресценция в гораздо большей степени подвержена влиянию различных факторов, чем поглощение света. Интенсивность флуоресценции зависит от:
природы вещества;
концентрации вещества в растворе;
условий, в которых находится флуоресцирующее вещество
(температура, растворитель, рН, наличие в растворе других веществ, способных влиять на флуоресценцию).
Природа вещества
Неорганические соединения (за исключением некоторых соединений урана, лантанидов) обычно не способны флуоресцировать в растворе. В то же время среди органических соединений флуоресцирующих веществ достаточно много.
Необходимым (но не достаточным!) условием для фотолюми-
несценции является способность вещества поглощать электромагнитное излучение УФили видимого диапазона. Обычно веще-
ства, обладающие интенсивной флуоресценцией, имеют длинную систему сопряжённых связей. Наиболее часто флуоресцирующие вещества встречаются среди ароматических соединений. Введение в бен-
зольное кольцо электронодонорных заместителей увеличивает способность вещества флуоресцировать. Например, многие фенолы и ароматические амины обладают интенсивной флуоресценцией. Вве-
дение электроноакцепторных заместителей, за некоторым исключением, уменьшает флуоресценцию. Атомы тяжёлых галогенов
(Br, I) увеличивают скорость интеркомбинационной конверсии и, тем самым, уменьшают квантовый выход флуоресценции. Однако вве-
дение тяжёлых галогенов увеличивает способность вещества фосфо-
ресцировать. Способность вещества к флуоресценции в растворе
272

Инструментальные методы анализа
увеличивается при конденсации ароматических колец и увеличении «жёсткости» молекулы. Например
O |
O |
O |
O |
O |
флуоресцирует |
|
|
|
|
флуоресцеин |
COO |
|
|
COO фенолфталеин |
Концентрация вещества
Зависимость между интенсивностью флуоресценции и концентрацией флуоресцирующего вещества в растворе более сложная, чем между поглощением света и концентрацией. Это связано с тем, что процесс излучения является вторичным и зависит от предшествующего ему процесса поглощения света.
Рассмотрим простейший случай, когда в растворе находится только одно флуоресцирующее вещество.
If kNf |
kQNпогл |
|
|
I) |
I I0 10 |
C |
Nпогл k I k (I0 |
|
|||||
Таким образом:
If kk QI0 (1 10 C )
Следовательно, зависимость между интенсивностью флуо-
ресценции и концентрацией флуоресцирующего вещества не является линейной.
Функцию 10 C можно разложить в ряд Маклорена
10 С 1 2,3 C (2,3 C)2 (2,3 C)3 ...
2! 3!
Если произведение С (оптическая плотность раствора) неве-
лико, то 10 С 1 2,3 C и тогда
If 2,3kk QI0 C KC
Таким образом, при малых значениях оптической плотности (при возб) зависимость интенсивности флуоресценции от концентрации можно считать линейной, что и используется в количест-
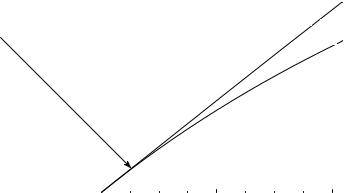
венном анализе. При более высоких значениях A зависимость интенсивности флуоресценции от концентрации становится более сложной и отклоняется от линейной. При A = 0,01 отклонение от линейности составляет 1%, 0,05 - 5%; 0,5 - около 35% (рис. 21.4).
273
|
|
|
Раздел 3 |
|
|
||
|
|
|
|
|
|
|
|
|
область, в которой I I |
I |
|
1 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|||
|
можно считать |
|
|
|
|
|
|
|
прямо пропорциональной А |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,0 0,1 0,2
A
Рис. 21.4. Зависимость между интенсивностью флуоресценции и оптической плотностью раствора
1) рассчитанная по упрощённой формуле I = KC; 2) реальная
Влияние оптической плотности раствора на интенсивность флуоресценции называется «эффектом внутреннего фильтра». Этот эффект обусловлен двумя причинами:
поглощением возбуждающего света, вследствие чего частицы,
находящиеся дальше от источника излучения, будут получать меньше возбуждающего излучения;
поглощением одними частицами вещества излучения, испускаемого другими частицами этого же вещества.
Условия, в которых находится флуоресцирующее вещество
Растворитель может оказывать влияние на величину разности между max спектра поглощения вещества (или спектра возбуждения флуоресценции) и спектра испускания. При увеличении диэлектрической проницаемости растворителя эта разность, называемая Стоксовым сдвигом, увеличивается. Растворитель влияет также и на величину квантового выхода флуоресценции, увеличивая её или уменьшая. Например, квантовый выход флуоресценции эозина в воде равен 0,2, а в ацетоне - близок к 1.
Влияние рН сказывается на флуоресценции тех веществ, в молекулах которых имеются функциональные группы, склонные к ки- слотно-основному взаимодействию. Например, фенол и его производные флуоресцируют в кислой среде, при ионизации фенольного гидроксила флуоресценция исчезает. Органические вещества, цвет и интенсивность флуоресценции которых изменяется при изменении рН, могут быть использованы в качестве кислотно-основных индикаторов (флуоресцеин, хинин и т.п.).
274

Инструментальные методы анализа
При повышении температуры увеличивается вероятность безызлучательных переходов, поэтому интенсивность флуоресценции уменьшается. Однако, у некоторых веществ свечение прекращается уже при -100 С, другие продолжают слабо флуоресцировать даже при >100 С. Если поместить флуоресцирующее вещество в специальную среду и охладить до температуры кипения жидкого азота (или даже жидкого гелия), то можно добиться того, что спектр флуоресценции органического вещества станет линейчатым. Такое явление называется эффектом Шпольского. Использование данного эффекта значительно повышает избирательность анализа и снижает предел обнаружения.
Интенсивность флуоресценции вещества и её квантовый выход могут снижаться в присутствии в растворе других веществ, называемых тушителями. Существуют, так называемые, универсальные тушители (например, O2), которые уменьшают флуоресценцию большинства веществ. Однако, чаще тушитель влияет на флуоресценцию одного вещества и не влияет на флуоресценцию другого (например, хлориды уменьшают интенсивность флуоресценции хинина), поскольку эффект тушения в разных случаях имеет различный механизм. Влияние концентрации тушителя на интенсивность флуоресценции вещества описывается уравнением Штерна-Фольмера
IIq 1 kCq
где Iq - интенсивность флуоресценции в присутствии тушителя, Сq - концентрация тушителя, k - константа тушения.
21.2.5. Измерение аналитического сигнала
Для измерения интенсивности флуоресценции используют спектрофлуориметры и флуориметры (на рис. 21.5).
В качестве источника излучения используют ртутную, ксеноновую и другие лампы. В последнее время для возбуждения флуоресценции применяют лазеры.
Для выделения нужного спектрального интервала в флуориметрах, как и в фотоэлектроколориметрах, используют светофильтры, а в спектрофлуориметрах, также как и в спектрофотометрах - монохроматоры (дифракционные решётки или призмы). Светофильтр (монохроматор), используемый для выделения необходимого возбуждающего излучения, называется первичным, а для выделения наиболее интенсивного излучения из спектра испускания - вторичным.
275

|
|
|
|
|
|
Раздел 3 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
устройство для выделения |
|
|
|
|
|
|
|
|
|
источник |
|
|
|
|
|
|
|
|
|||
|
|
|
|
спектрального интервала |
|
|
|
|
|
|
|
||
|
|
излучения |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
из возбуждающего излучения |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
устройство для выделения спектрального интервала из испускаемого излучения
регистрирующее детектор устройство
Рис. 21.5. Принципиальная схема прибора для измерения интенсивности флуоресценции
Измерение флуоресценции, в отличие от измерения поглощения,
чаще всего проводят под прямым углом к направлению возбуж-
дающего света. Такой приём позволяет избежать наложения возбуждающего света на излучаемый. При измерении интенсивности фосфоресценции, либо при большом Стоксовом сдвиге, можно использовать схему, при которой источник возбуждения, образец и детектор находятся на одной оптической оси. В данном случае возбуждающий свет не мешает определению, так как при измерении интенсивности фосфоресценции измерение проводят после прекращения действия возбуждающего света, а при большом Стоксовом сдвиге возб и исп настолько различаются, что возбуждающий свет задерживается монохроматором и не попадает на детектор. В случае сильно поглощающих растворов, полупрозрачных и твёрдых образцов используют фронтальный способ, при котором измерение флуоресценции проводится под углом 45 относительно возбуждающего излучения.
При измерении флуоресценции имеют дело со слабым излучением, поэтому в качестве детектора используют не фотоэлементы, как
вспектрофотометрии, а фотоумножители.
21.2.6.Практическое применение и основные приёмы люминесцентного анализа
Клюминесцентной спектроскопии относят:
флуоресцентный метод анализа (флуориметрия),
фосфоресцентный метод анализа (фосфориметрия),
хеми- и биолюминесцентный метод анализа (люминометрия) и
др.
276

Инструментальные методы анализа
Наиболее широкое применение среди перечисленных люминесцентных методов анализа имеет флуориметрия. По сравнению со спектрофотометрией флуориметрия обладает:
большей избирательностью (не все вещества, поглощающие УФ- и видимое излучение, способны флуоресцировать);
более низким пределом обнаружения (измерить абсолютную величину малого сигнала всегда легче, чем разность между двумя большими сигналами);
удобным временным диапазоном.
Поглощение света - это практически мгновенный процесс (10-15 - 10-16 с), флуоресценция длится около 10 нс (а фосфоресценция значительно дольше). За это время с молекулой могут произойти различные процессы, которые влияют на характеристики флуоресценции. Данное свойство широко используется в биохимии для изучения строения мембран, диффузии биомолекул, динамики связывания антигенов и антител. Влияние вращения молекул антигенов (лекарств, ядов), меченых флуоресцеином, на поляризацию флуоресценции последнего лежит в основе поляризационного флуороиммуноанализа, одного из современных методов анализа биологических объектов.
Флуоресцентный анализ используют для обнаружения и для количественного определения веществ. В качественном анализе чаще всего используется способность вещества флуоресцировать тем или иным цветом. При этом в качестве источника возбуждения обычно используют УФ-лампу, а наличие или отсутствие флуоресценции определяют визуально. Таким образом, например, обнаруживают флуоресцирующие вещества на плоскостных хроматограммах.
Вколичественном анализе используют зависимость интенсивности флуоресценции от концентрации флуоресцирующего вещества либо, реже, зависимость уменьшения интенсивности флуоресценции от концентрации тушителя, в роли которого выступает вещество, концентрацию которого необходимо определить.
Вфлуоресцентном анализе используется:
измерение собственной флуоресценции вещества;
получение флуоресцирующих продуктов, в том числе и экстракционная флуориметрия;
определения, основанные на тушении флуоресценции;
титрование с флуоресцентными индикаторами и др.
Флуориметрическое определение, основанное на собственной флуоресценции, используется для определения хинина, берберина, рибофлавина, фторхинолонов, флуоресцеина и т.д.
277
|
|
|
Раздел 3 |
|
|
|
|
HO |
|
HO |
|
|
|
|
|
|
N |
|
|
|
|
HO |
|
|
|
|
|
|
OH |
H3CO |
хинин |
|
|
|
|
|
|
|
|||
|
HO |
|
|
|
O |
|
|
|
|
|
|
||
|
|
N |
F |
|
COOH |
|
|
|
|
|
|||
H3C |
N |
N |
O |
|
|
|
|
|
N |
H3C N N |
O |
N |
|
H3C |
N |
H |
|
CH3 |
||
|
рибофлавин O |
|
|
|
||
|
|
офлоксацин |
|
|
||
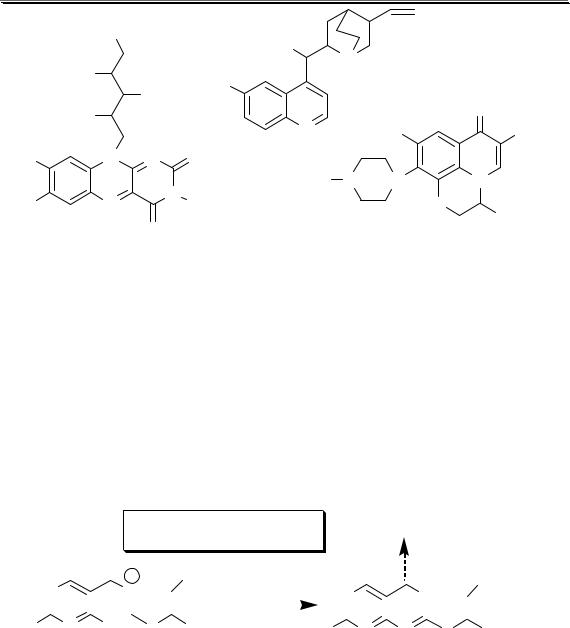
Обратите внимание на особенности структуры флуоресцирующих веществ – наличие в составе их молекул конденсированных ароматических систем.
В основе реакций получения флуоресцирующих продуктов могут лежать различные процессы: окисления, конденсации, образование комплексных соединений, ионных ассоциатов и др. Если образующийся продукт мало растворим в воде, неустойчив в водном растворе, либо избыток реагента мешает определению или влияет на устойчивость продукта, применяют экстракционную флуориметрию. Иногда вещество не флуоресцирует или слабо флуоресцирует в водной среде, но интенсивно флуоресцирует в среде органического растворителя.
экстракт флуоресцирует ярко |
экстракция бутанолом |
голубым светом (430-435 нм) |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
CH3 |
|
N |
N |
|
|
|
|
|
|||||||||||||
|
|
|
K3[Fe(CN)6] |
N |
|
N |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C N NH2 S CH2CH2OH |
H3C N N S CH2CH2OH |
||||||||||||||||||
|
|
|
тиамин |
|
|
|
|
|
|
тиохром |
|||||||||
Флуориметрическое определение, основанное на тушении флуоресценции, применяют для определения сульфаниламидов (тушат флуоресценцию 9-хлоракридина), -лактамных антибиотиков (тушат флуоресценцию меркурохрома) и т.д.
Кновым подходам в люминесцентной спектроскопии относятся:
производная спектрофлуориметрия;
синхронная спектрофлуориметрия;
спектроскопия, основанная на эффекте Шпольского;
флуоресцентная спектроскопия узких линий,
фосфориметрия при комнатной температуре и др.
278

Инструментальные методы анализа
ГЛАВА 22
22.1. Общая характеристика
Хроматография - метод разделения смесей веществ или частиц, основанный на различии в скоростях их перемещения в системе, состоящей из несмешивающихся и движущихся друг относительно друга фаз.
Хроматография - гибридный метод анализа, включающий разделение веществ и их последующее определение при помощи специальных устройств - детекторов.
Вкачестве неподвижной фазы в хроматографическом процессе выступает твёрдое вещество (сорбент) или плёнка жидкости, нанесённая на твёрдый носитель, а в качестве подвижной фазы - жидкость или газ, протекающий через неподвижную фазу.
Вотличие от статических методов разделения - сорбции и экс-
тракции хроматография является динамическим процессом. При перемещении через неподвижную фазу подвижная фаза встречает на своём пути всё новые и новые слои сорбента, что сопровождается многократными повторениями актов сорбции и десорбции разделяемых веществ. Хроматографическое разделение обладает большей эффективностью по сравнению со статическими методами.
"Схвати,  подержи и отпусти"
подержи и отпусти"
22.2. Классификация хроматографических методов
Существует более 50 различных хроматографических методов и вариантов. В основу их классификации могут быть положены:
279

Раздел 3
агрегатное состояние подвижной и неподвижной фазы,
геометрическая форма неподвижной фазы,
преобладающий механизм разделения,
цель проведения,
способ получения хроматограммы и т.д.
АГРЕГАТНОЕ СОСТОЯНИЕ ПОДВИЖНОЙ ФАЗЫ
подвижная |
газовая |
жидкостная подвижная |
||
фаза - газ |
|
|
|
фаза - |
|
|
жидкость |
||
|
|
|
||
газо- |
газо- |
жидкость- |
жидкость- |
жидкость- |
твёрдофазная |
жидкостная |
жидкостная |
твёрдофазная |
гелевая |
ВИД НЕПОДВИЖНОЙ ФАЗЫ
В названии хроматографического метода первым указывается агрегатное состояние подвижной фазы, а вторым - неподвижной
ГЕОМЕТРИЧЕСКАЯ ФОРМА НЕПОДВИЖНОЙ ФАЗЫ
колоночная
 хроматографический
хроматографический 
процесс проходит
в пределах
протяжённого
цилиндрического пространства
капиллярная
диаметр проходного сечения пространства соизмерим с диаметром частиц неподвижной фазы, которая нанесена на стенки капилляра в виде тонкой
плёнки
плоскостная
 хроматографический
хроматографический 
процесс проходит в тонком слое
|
Колоночный вариант используется как в |
жидкостной, так и в газовой хроматографии, а плоскостной - только в жидкостной.
Классификация хроматографических методов в зависимости от преобладающего механизма разделения, приведена в табл. 22.1.
Реальный процесс обычно включает в себя несколько механизмов, обуславливающих разделение веществ, поэтому данная классификация условна.
280
Инструментальные методы анализа
Табл. 22.1.
Классификация хроматографических методов в зависимости от преобладающего процесса, лежащего в основе разделения веществ
Вид хроматографии |
Преобладающий механизм разделения |
|
|
адсорбционная |
различная адсорбируемость разделяемых ве- |
|
ществ неподвижной фазой |
адсорбционно- |
образование (в подвижной фазе или на поверх- |
комплексообразовательная |
ности неподвижной фазы) различных по устой- |
|
чивости комплексных соединений |
аффинная |
различная способность разделяемых веществ к |
|
биоспецифическим взаимодействиям |
ионообменная |
различная способность разделяемых веществ к |
|
ионному обмену |
осадочная |
образование осадков, различающихся по рас- |
|
творимости |
распределительная |
различная растворимость разделяемых веществ |
|
в неподвижной фазе или в подвижной и непод- |
|
вижной фазах |
эксклюзионная |
различия в размерах и форме молекул разделяе- |
|
мых веществ |
ЦЕЛЬ ПРОВЕДЕНИЯ
информационная |
технологическая |
Цель - получение информации о |
Целью является само |
составе объекта (аналитическая |
разделение. Применяется |
хроматография) либо о его |
для выделения целевого |
физико-химических свойствах |
компонента из смеси либо |
(физико-химическая |
для его очистки. |
хроматография) |
|


По способу получения хроматограммы хроматография бывает элюентной, фронтальной и вытеснительной (табл 22.2).
281
