
Ііі Циклічні вуглеводні
Циклічні вуглеводні, молекули яких мають замкнуту структуру, поділяються на три великих групи:
аліциклічні– своєрідні аналоги аліфатичних вуглеводнів із замкнутим вуглецевим ланцюгом; вони можуть бути насиченими (циклоалкани), чи ненасиченими (циклоалкени);
ароматичні, основою структури яких є бензенове кільце;
гетероциклічні, в яких до складу цикла входять гетероатоми (N, P, O, S тощо).
Ііі. І Циклоалкани
Циклоалкани(циклопарафіни) – це насичені вуглеводні із замкнутим вуглецевим ланцюгом, які утворюють гомологічний ряд СnH2n, де n 3.
І.І Класифікація. Номенклатура
Залежно від розміру циклу циклоалкани поділяють на групи:
малі цикли, головний ланцюг яких складається із трьох чи чотирьох атомів Карбону - їх називають відповіднотри- та чотиричленнимициклами;
нафтени, до яких належать пяти- і шестичленні цикли;
великі цикли – замкнуті насичені вуглеводні, цикли яких утворені із 7 та більше атомів Карбону.
Н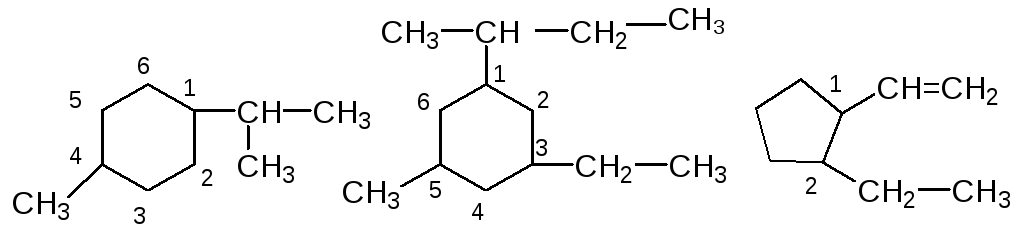 азви
циклоалканів формуються на основі назв
відповідних алканів з додаванням
префіксу цикло-. При наявності замісників
нумерацію починають від радикалу з
більшою кількістю атомів С чи від більш
розгалуженого, наприклад:
азви
циклоалканів формуються на основі назв
відповідних алканів з додаванням
префіксу цикло-. При наявності замісників
нумерацію починають від радикалу з
більшою кількістю атомів С чи від більш
розгалуженого, наприклад:
4-Метилізопропіл- 3-Етил-5-метил- 2-Етилвініл-
циклогексан вторбутилциклогексан циклопентан
Як видно із наведених прикладів, структурні формули циклоалканів записують у скороченій формі, зображуючи геометричні фігури і опускаючи символи С і Н.
2 Ізомерія
Циклоалкани виявляють два види внутрішньокласової ізомерії.
Структурна ізомерія зумовлюється різними розмірами циклу, кількістю, характером і взаємним розташуванням замісників, наприклад, для циклоаканів С5Н10можливі так ізомери:

 CH3
CH3

СН2-СН3
Циклопентан Метилциклобутан Етилциклопропан


СН3СН3- СН3
СН3
1,2-Диметилциклопропан 1.1-Диметилциклопропан
Просторова ізомерія повязана із різним розташуванням замісників відносно площини цикла, наприклад:

 СН3СН3СН3
СН3СН3СН3
СН3
Транс-1,2-диметилциклопропан Цис-1,2-диметилциклопропан
 Крім
того, циклоалкани мають і міжкласові
ізомери –метамери– з алкенами,
наприклад, для складу С3Н6:
Крім
того, циклоалкани мають і міжкласові
ізомери –метамери– з алкенами,
наприклад, для складу С3Н6:
СН2=СН-СН2
Пропен Циклопропан
3 Будова циклоалканів
Всі атоми Карбону в циклоалканах перебувають у стані sp3-гібридизації та утворюють чотири-звязки С-С і С-Н. Кути між вісями гібридизованих орбіталей на відміну від циклоалаків не завжди дорівнюють 109028, а залежать від розмірів цикла. Однак вільне обертання атомних груп навколо звязків С-С, як це спостерігається в алканах, у циклоалканах неможливе.
Розміри циклів визначають особливості їх будови, тому її необхідно розглядати окремо для кожного цикла.
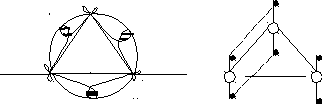
Циклопропан уявляє собою плоский рівносторонній трикутник, тому можна було б очікувати, що валентні кути дорівнюватимуть 600, тобто різко відрізнятимуться від класичного кута 109028приsp3-гібридизації. Однак реально утворення звязків між атомами Карбону відбувається не на вісі зіязку, а зовні від неї (рис.1а). Таке бокове перекривання валентнихsp3-гібридизованих орбіталей дещо нагадує-звязок.
Звязки, утворені sp3-гібридизованими атомами Карбону, при яких максимальна електронна густина зосереджується не на вісі звязку, а збоку від неї, називаються банановими, або -звязками.
а) б)
Вісь звязку
Р исунок
1 – Будова молекули циклопропана: а)
утворення бананових звязків
С-С при боковому перекриванні орбіталей;
б) заслонена конформація циклопропана;
- атоми Карбону;
исунок
1 – Будова молекули циклопропана: а)
утворення бананових звязків
С-С при боковому перекриванні орбіталей;
б) заслонена конформація циклопропана;
- атоми Карбону;
 - атоми Гідрогену
- атоми Гідрогену
Внаслідок відхилення валентного кута від тетраедричного у молекулі циклопропану виникає особливий вид напруження, яке називається кутовим, або байєровським.
Оскільки -скелет молекули циклопропана має плоску будову, атоми Гідрогену можуть розміщуватися тільки над і під його площиною, тобто знаходяться в енергетично невигідному
положенні, утворюючи заслонену конформацію, при якій атоми Н сусідніх карбонових атомів мають найменшу відстань один від одного (на рис. 1б це показано пунктиром). Завдяки невигідній
заслоненій конформації в молекулі циклопропану виникає додаткове напруження, яке називається торсіонним.
Отже, бокове перекривання -звязків, кутове і торсіонне напруження в молекулі циклопропану створюють передумови для того, що він може вступати не тільки у реакції радикального заміщенняSR, як аліфатичний пропан, але і в реакції приєднання на відміну від нього.
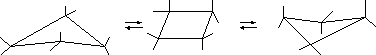
Циклобутанмає валентні кути 900, що викликає досить значне кутове напруження, яке , однак, насправді менше за розраховану величину. Зниження кутового напруження відбувається завдяки можливості виведення метиленових груп (-СН2-) із площини циклу. При цьому циклобутан набуває неплоскої, складеної форми, при якій два атоми С розташовуються нижче або вище площини, де знаходяться інші два атоми Карбону (рис.2). Але енергетичний барєр цих взаємних переходів дуже малий, тому молекулу циклобутану вважають практично плоскою. Наявність кутового напруження зумовлює здатність циклобутану до реакцій приєднання.
 Н
Н Н
Н Н
Н
Н Н
Н Н
Н Н Н
Н
Н Н Н Н Н Н Н Н
Н Н Н Н Н
Н Н
Рисунок 2 – Перехід молекули циклобутану у плоску і складену форми
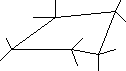
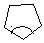
Циклопентан має валентні кути (1080), найбільш близькі до тетраедричного (109228), тому кутове напруження в ньому майже відсутнє. Однак у молекулі циклопентану виявляється торсіонне напруження внаслідок існування заслоненої конформації. Для зменшення терсіонного напруження циклопентан може переходити у неплоску конформацію “конверта”, в якій один атом С виходить із площини цикла, тобто один кут як би загинається (рис. 3). Причому, цим виходячим із площини циклу атомом буває почергово кожний атом Карбону, тому цикл як би перебуває у постійному хвилєподібному русі. Завдяки зменшенню торсіонного напруження пятичленні цикли є стійкими, для них реакції приєднання не характерні.
 Н Н
Н Н
1800Н
 Н
Н
Н Н
Н
Н
Н Н
Рисунок 3 – Взаємний перехід плоскої конформації в конформацію “конверта” для молекули циклопентану
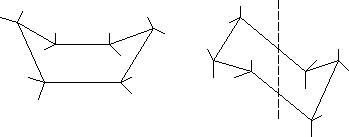
Циклогексанне може мати будову плоского шестикутника, оскільки в такому випадку валентні кути дорівнювали б 1200, а всі атоми Н знаходилися б у заслоненому положенні, тобто великі кутове і торсіонне напруження зруйнували б таку молекулу. Тому в циклогексані реалізуються найменш напружені із можливих конформацій – ванни В (від англ.boat) і крісла С (від англ. сhair). Обидві конформації вільні від кутового напруження, оскільки валентні кути в них дорівнюють 109,50(рис.4).
 а)
б)
а)
б)
Н а Вісь симетрії
Н Н е
4 Н Н
5 6 1 Н
Н Н е а
а е
Н Н е
а е
3 2 Н а
Н
е
а
Рисунок 4 – Будова молекули циклогексану: а) конформація В – ванни;
б) конформація С – крісла; а – оксиальні, е – екваторівльні атоми Гідрогену
Але в конформації Ватоми Гідрогену біля двох пар атомів Карбону (С1і С3, С5і С6) перебувають у заслоненому положенні, що енергетично менш вигідно – порівняно із конформацієюС, потенціальна енергія якої на 35 кДж/моль менша, ніж у конформаціїВ. У конформації кріслаС шість пар атомів Гідрогену, які називаютьсяаксіальними, напрямлені поперемінно вниз і угору від-скелету молекули і паралельні вісі симетрії. Інші шість атомів Гідрогену розташовані відносно вісі симетрії під кутом 109,50і теж напрямлені поперемінно вниз і угору – вони називаються екваторіальними.
Оскільки потенціальна енергія конформації В вища, ніж у конформаціїС, то при кімнатній температурі приблизно 99,9% циклогексану перебуває у конформації крісла.
Завдяки стійкості пяти – і шестичленних циклів вони вступають переважно в реакції заміщення. Реакції приєднання (наприклад, гідрування) проходять рідко, у надзвичайно жорстких умовах і супроводжуються розривом цикла.
