
- •Химическое отделение вятский государственный гуманитарный университет
- •М. А. Зайцев основы биохимии
- •Часть 2
- •6. Нуклеиновые кислоты
- •6.1. Химический состав нуклеиновых кислот
- •6.2. Молекулярная масса нуклеиновых кислот
- •6.3. Локализация в клетке днк и рнк. Виды днк и рнк
- •6.4. Строение структурных элементов нуклеиновых кислот
- •6.5.1. Первичная структура днк
- •Генетический код
- •6.5.2. Вторичная структура днк
- •6.5.3. Третичная структура днк
- •6.5.4. Свойства днк
- •6.5.4.1. Репликация (редупликация, самоудвоение) днк
- •6.5.4.2. Транскрипция (синтез рнк)
- •6.6.1. Первичная структура рнк
- •6.6.2. Вторичная структура рнк
- •6.6.3. Третичная структура рнк
- •6.6.4. Классы рнк
- •6.6.5. Синтез белка (трансляция)
- •7. Общие понятия об обмене веществ и энергии в организме
- •7.1. Основные этапы обмена веществ
- •1 Этап. Подготовительный
- •2 Этап. Превращение строительных блоков (мономеров) в более простые соединения
- •3 Этап. Цикл Кребса (цикл ди- и трикарбоновых кислот, цтк)
- •4 Этап. Окислительная цепь ферментов (дыхательная цепь)
- •7.2. Обмен энергии. Макроэргические соединения
- •8. Биологическое окисление
- •8.1. Функции биологического окисления
- •8.2. Типы биологического окисления
- •II. Окисление, сопряженное с фосфорилированием адф
- •6 Железосерных белков
- •9. Обмен углеводов
- •9.1. Переваривание и всасывание углеводов
- •9.2. Синтез гликогена
- •9.3. Распад гликогена и освобождение глюкозы (глюкогенез)
- •9.4. Превращения моносахаридов
- •9.4.1. Дихотомический путь распада глюкозы. Гликолиз
- •1. Фосфорилирование:
- •9.4.2. Обмен пировиноградной кислоты
- •9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
- •9.4.4. Энергетический эффект гликолитического расщепления 1 молекулы глюкозы и последующего окисления пвк до со2 и н2о
- •9.4.5. Апотомический путь распада глюкозо-6-фосфата (пентозный, или пентозофосфатный цикл окисления углеводов)
- •9.5. Общая схема распада углеводов
- •9.6. Синтез углеводов
- •10. Обмен белков
- •10.1. Переваривание белков
- •10.2. Превращения аминокислот в организме
- •10.2.1. Процессы гниения белков в кишечнике
- •10.2.2. Судьба всосавшихся аминокислот
- •10.2.3. Конечные продукты распада аминокислот
- •10.3. Новообразование аминокислот
- •11. Обмен липидов
- •11.1. Переваривание и всасывание липидов
- •11.2. Окисление жирных кислот
- •11.3. Распад глицерина
- •11.4. Биосинтез липидов
- •11.4.1. Синтез высших жирных кислот
- •11.4.2. Биосинтез триглицеридов
- •12. Взаимосвязь процессов обмена веществ
- •12.1. Взаимосвязь обменов нуклеиновых кислот и белков
- •12.2. Взаимосвязь обменов нуклеиновых кислот и углеводов
- •12.3. Взаимосвязь обмена белков и углеводов
- •12.4. Взаимосвязь обмена белков и липидов
- •12.5. Взаимосвязь обмена углеводов и липидов
- •13. Регуляция обмена веществ
- •I. Метаболитный уровень регуляции
- •II. Оперонный уровень регуляции
- •III. Клеточный уровень регуляции
- •IV. Организменный уровень регуляции
- •V. Уровень регуляции метаболизма в экосистемах (популяционный)
II. Окисление, сопряженное с фосфорилированием адф
Этот тип биологического окисления осуществляется двумя способами.
• Если макроэргическая связь возникает в момент непосредственного окисления субстрата, а затем тем или иным путем передается на фосфатный остаток, который, в свою очередь, используется для фосфорилирования АДФ, т. е. синтеза АТФ, то такой вид биологического окисления называют окислением, сопряженным с фосфорилированием АДФ на уровне субстрата (субстратным фосфорилированием).
Примеры реакций субстратного фосфорилирования:
– при окислении 3-фосфоглицеринового альдегида (3-ФГА) в 2-фосфоглицериновую кислоту (2-ФГК) – см. гликолиз;
– при превращении фосфоенолпировиноградной кислоты (ФЕП) в пировиноградную (пируват, ПВК) – см. там же;
– при превращении -кетоглутаровой кислоты в янтарную (см. реакции цикла Кребса).
• Если атомы водорода с коферментов дегидрогеназ, принимающих участие в окислении субстратов, передаются в оксидоредуктазную цепь, где сопряжено с переносом ионов Н+ и электронов на молекулярный кислород происходит активирование неорганического фосфата и при его посредстве – фосфорилирование АДФ с образованием АТФ, то такое сопряжение окисления с синтезом АТФ называют сопряжением на уровне электронотранспортной (окислительной, оксидоредуктазной, дыхательной) цепи (окислительным фосфорилированием). Понятно, что сам окисляемый субстрат в этом случае непосредственного участия в активировании неорганического фосфата не принимает.
Сопряжение окисления с фосфорилированием идет главным образом на внутренних мембранах митохондрий.
В переносе ионов Н+ и электронов от субстратов к молекулярному кислороду принимают участие следующие окислительно-восстановительные ферменты.
Пиридиновые дегидрогеназы
Коферментами данных ферментов являются НАД и НАДФ. Универсальным донором атомов Н для дыхательной цепи ферментов служит НАДН2. Если при окислении субстрата возникает НАДФН2, то осуществляется реакция:
НАДФН2 + НАД ⇄ НАДФ + НАДН2.
Следовательно, и в этом случае атомы водорода перед поступлением в дыхательную цепь передаются на НАД.
Реакция гидрирования НАД представлена в виде следующего уравнения (полную схему см. выше):

При переносе 2-х атомов водорода от субстрата на НАД+ один из них затем присутствует в восстановленном коферменте в виде атома Н, а другой – в виде электрона. Свободный ион Н+ остается в среде. (Для простоты восстановленные формы НАД и НАДФ изображают: НАДН2 и НАДФН2).
Особенности реакций с участием пиридиновых дегидрогеназ:
Легкая обратимость.
Коферменты легко отделяются от белковой части, обладают высокой подвижностью, что позволяет им переносить атомы Н, ионы Н+ и электроны из одной части клетки в другую.
НАД и НАДФ способны принимать атомы Н от большого числа субстратов, окислительно-восстановительные потенциалы которых ниже (
 ).
).
Флавиновые дегидрогеназы
Коферментами их являются ФМН и ФАД. Флавиновые ферменты являются акцепторами атомов водорода и осуществляют перенос их от НАДН2:
НАДН2 + ФАД ⇄ НАД + ФАДН2.
В некоторых случаях (при окислении янтарной кислоты в цикле Кребса или при окислении жирных кислот) флавиновые ферменты могут играть роль первичных дегидрогеназ, т. е. прямо, без участия НАД, принимать электроны и ионы водорода Н+ от субстратов.
ФМН и ФАД, в отличие от НАД и НАДФ, очень прочно связаны с апоферментом и не отщепляются от него ни на одной стадии каталитического цикла. Активной частью молекул ФАД и ФМН является изоаллоксазиновое кольцо рибофлавина, к атомам азота которого могут присоединяться 2 атома водорода (полную схему см. выше):
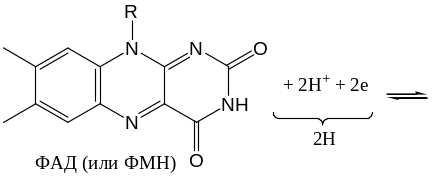
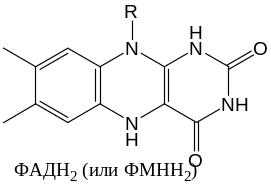
Кофермент Q (убихинон)
КоQ – следующий компонент дыхательной цепи. Убихинон может играть роль промежуточного переносчика атомов водорода. Считают, что восстановленная форма флавиновых ферментов в дыхательной цепи передает атомы водорода коферменту Q (см. выше).
Цитохромы
Дальнейший перенос электронов от КоQ на кислород осуществляет система цитохромов, состоящая из ряда гемопротеидов, расположенных в порядке возрастания окислительно-восстановительных потенциалов, что обеспечивает упорядоченную передачу электронов. Цитохромы а и а3 содержат в своем составе еще и атомы меди. При транспорте электронов в направлении увеличения окислительно-восстановительных потенциалов происходят процессы:
Fe2+
![]() Fe3+
(в цит. b,
c1,
с)
Fe3+
(в цит. b,
c1,
с)
Cu+ Cu2+ (в цит. а, а3).
Схема дыхательной цепи
НАДН + Н+ Е = –0,32 В НАД+
![]()
Флавопротеин
ФМН Е = –0,30 В ФМНН2
![]()
