
- •060101 65 – Лечебное дело, 060103 65 – Педиатрия, 060105 65 – Стоматология, 060104 65 – Медико-профилактическое дело
- •Тема 1. Поверхностные явления 12
- •Предисловие
- •Введение
- •Тема 1. Поверхностные явления
- •1. Свободная поверхностная энергия, поверхностное натяжение
- •2. Смачивание, адгезия, когезия
- •3. Сорбция и ее виды
- •Абсорбция
- •Адсорбция на подвижной поверхности раздела фаз
- •Адсорбция пав в системе воздух-вода
- •Адсорбция на неподвижной поверхности раздела фаз
- •Молекулярная (неэлектролитов) адсорбция из растворов.
- •Адсорбция ионов из растворов
- •Ионообменная адсорбция
- •Основные физико-химические характеристики ионитов
- •4. Хроматография
- •5. Биологические поверхностно-активные вещества
- •6. Медико-биологическое значение адсорбции
- •Типы сорбентов, использующихся для удаления различных веществ
- •Основные области применения энтеросорбентов
- •Тема 2. Дисперсные системы
- •1. Классификация дисперсных систем
- •Свободно- и связнодисперсные системы
- •Лиофобные и лиофильные дисперсные системы
- •Классификация дс по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •2. Методы получения и очистки дисперсных систем
- •Методы очистки дисперсных систем
- •3. Лиофобные коллоидные растворы
- •Строение мицелл в лиофобных коллоидных растворах
- •Устойчивость лиофобных коллоидных растворов
- •Кинетика коагуляции
- •Механизм коагуляции
- •Пептизация или физико-химическое диспергирование
- •Коллоидная защита и флокуляция
- •4. Лиофильные коллоидные растворы
- •Истинный раствор ((;(( коллоидный раствор.
- •Зависимость области применения пав от значения глб
- •Свойства лиофильных коллоидных растворов пав и вмс
- •Ослабление высаливающего действия
- •Солюбилизация
- •5. Микрогетерогенные дисперсные системы
- •Аэрозоли и их свойства
- •Порошки и их свойства
- •Суспензии и их свойства
- •Эмульсии и их свойства
- •Пены и их свойства
- •Тема 3. Свойства вмс и их растворов
- •Классификация вмс
- •Полимерные полиэлектролиты и их свойства
- •Свойства растворов вмс, общие с истинными растворами:
- •Кислотно-основные свойства белков
- •Значения pI белков живого организма
- •Окислительно-восстановительные свойства белков
- •Комплексообразующие свойства белков
- •Поверхностные свойства белков
- •3. Набухание и растворение вмс
- •4. Вязкость растворов вмс
- •5. Осмотические свойства растворов вмс
- •6. Мембранное равновесие Доннана
- •7. Устойчивость и разрушение растворов вмс
- •8. Застудневание (желатинирование). Возникновение связнодисперсных систем и их свойства
- •Обучающие тесты
- •Обучающие задачи
- •Учебно-исследовательские лабораторные работы
- •Тема I. Поверхностные явления
- •Тема: Адсорбция уксусной кислоты на активированном угле. Качественные опыты по адсорбции и хроматографии
- •Тема: Определение обменной емкости ионита
- •Тема: Изотерма поверхностного натяжения и адсорбции изоамилового спирта на твердом адсорбенте
- •Учебно-исследовательская лабораторная работа № 4 Тема: Изучение адсорбции пав на твердом адсорбенте из водных растворов
- •Тема II. Дисперсные системы
- •Тема: Получение и свойства лиофобных коллоидных растворов
- •Конденсационный метод получения золей (химическая конденсация)
- •II. Дисперсионный метод получения золей.
- •Тема: Устойчивость и коагуляция лиофобных коллоидных растворов. Коллоидная защита
- •Тема: Получение и свойства эмульсий
- •Тема III. Растворы вмс
- •Учебно-исследовательская лабораторная работа №8
- •Тема: Вискозиметрическое определение молекулярной
- •Массы полимера
- •Тема: Набухание вмс
- •Тестовые задания, задачи, упражнения для самостоятельного решения
- •Тема 1. Поверхностные явления
- •Тема II. Дисперсные системы
- •Тема III. Растворы вмс
- •Тестовый контроль по теме: «Поверхностные явления».
- •Тестовый контроль по теме: «Лиофобные коллоидные растворы»
- •Тестовый контроль по теме: «Свойства вмс и их растворов».
- •Темы реферативных докладов для студентов лечебного, педиатрического, стоматологического и медико-профилактического факультетов
- •Список использованной литературы
- •Приложение
- •1. Основные единицы измерения физических величин
- •2. Основные физические постоянные
- •3. Метрическая система мер
- •4. Множители и приставки для образования десятичных кратных и дольных единиц и их обозначения
- •5. Плотность пав в жидком состоянии
- •6. Зависимость поверхностного натяжения воды от температуры
- •7. Поверхностное натяжение жидкостей при 293 k
- •Зависимость адсорбции газов на древесном угле от
- •9. Золотые числа
- •10. Критические концентрации мицеллообразования для некоторых мыл
- •11. Значения констант в уравнении Марка-Хаувинка и омм полимеров
2. Методы получения и очистки дисперсных систем
Все методы получениядисперсных систем сводятся либо к объединению молекул или ионов в агрегаты дисперсной фазы, либо к доведению частиц вещества до определенной степени дисперсности.
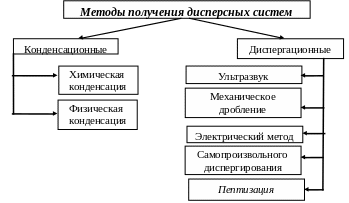
В соответствии с этим получение дисперсных систем осуществляется конденсацией и диспергированием. В основе этих методов лежат два противоположных процесса – агрегация более мелких частиц (конденсация) и дробление более крупных частиц (диспергирование), приводящих к единому результату – образованию дисперсных систем.
Конденсационные методы получения лиофобных коллоидов
Взаимодействие ионов и молекул с образованием частиц коллоидных размеров может быть достигнуто физическими и химическими методами.
Химическая конденсация
Метод окисления. В результате реакции окисления может быть получен коллоидный раствор, например: 2H2S + SO2 3S + 2H2O.
Образующиеся атомы нейтральной серы затем самопроизвольно конденсируются в коллоидные частицы серы:
{[S]m nHS– (n-x) H+}x– xH+.
Реакция восстановления. На реакции восстановления основан один из наиболее распространенных химических методов получения коллоидных растворов металлов. В качестве восстановителей обычно используются вещества, обладающие восстанавливающими свойствами, как, например, газообразный водород, формалин, танин.
Например, реакции получения золя серебра восстановлением разбавленных растворов солей серебра в щелочной среде танином (С76Н52О46):
AgNO3 + K2CO3 Ag2O + 2KNO3 + CO2
3Ag2O + С76Н52О46 6Ag + C76H52O49
Строение мицеллы данного золя можно представить следующей схемой: {[Ag]mmAg2OnAgO–(n-x) K+}x–xK+.
В медицине применяются коллоидные препараты серебра – колларгол, протаргол.
Красный золь золота, применяемый в медицине, получают восстановлением натриевой соли золотой кислоты формальдегидом:
NaAuO2 + HCOH + Na2CO3 Au + HCOONa + H2O.
Строение мицеллы данного золя можно представить следующей схемой: {[Au]m· nAuO2–· (n-x) Na+}x– xNa+.
Реакция обмена. В результате реакции обмена образуется новое малорастворимое вещество, способное сохраняться в высокодисперсном состоянии при наличии ряда соответствующих благоприятных условий (концентрация реагирующих веществ, примеси и др.). Примером может служить получение золя сернистого мышьяка:
2H3AsO3 + 3H2S As2S3 + 6H2O,
{[Аs2S3]m nНS–·(n-x)Н+}x– xН+
Реакция гидролиза. Гидролизом широко пользуются при получении золей из солей, если в результате реакции гидролиза образуются плохо растворимые вещества. Так, например, нерастворимый гидроксид железа(III) получается при гидролизе хлорида железа(III) при температуре 100С по уравнению: FeCl3+ 3H2O ((;t( Fe(OH)3 + 3HCl.
Образующийся на поверхности его частиц оксохлорид железа(III), Fe(OH)3 + HCl FeOCl + 2H2O, диссоциирует на ионы:
FeOCl FeO+ +Cl–, которые образуют двойной электрический слой вокруг частиц Fe(OH)3 и удерживают их во взвешенном состоянии:
{[Fe(OH)3]m nFeO+ (n–x)Cl–}x+ xCl–.
Физическая конденсация
Метод замены растворителя. Метод основан на выделении растворенного вещества из раствора в виде высокодисперсной нерастворимой фазы путем замены растворителя. Молекулы растворенного вещества, находящегося в состоянии молекулярной дисперсности в одном растворителе, попадая в условия малой растворимости при замене растворителя, начинают конденсироваться в более крупные коллоидные частицы. Данным методом можно приготовить золи серы, холестерина, канифоли, мастики при вливании спиртовых растворов этих веществ в воду.
Диспергационные методы получения дисперсных систем
Диспергированием называют тонкое измельчение твердых материалов или жидкостей и распределение их частиц в жидкой или газообразной среде, в результате чего образуются порошки, суспензии, эмульсии, аэрозоли.
Механические методы. Для дробления веществ в лабораториях и на производствах применяются устройства, работающие по принципу ударного размельчения и растирания, диспергируемых материалов; к таким устройствам относятся шаровые и коллоидные мельницы.
Ультразвуковой метод. Диспергирующее действие ультразвука связано с тем, что при прохождении звуковой волны в жидкости происходят локальные быстро сменяющиеся сжатия и растяжения, которые создают разрывающее усилие и приводят к диспергированию взвешенных частиц. Таким путем получают высокодисперсные эмульсии и суспензии, в том числе пригодные для внутривенного введения. Кроме того, при действии ультразвука на коллоидные растворы, эмульсии, суспензии происходит их стерилизация, так как кавитация (образование пузырьков) вызывает разрушение тел микроорганизмов и их спор. Кавитация возникает во время ударной волны при липотрипсии и играет важную роль при разрушении камней в почках.
Электрический метод. Метод получения коллоидных растворов при помощи электричества, который предложен Бредигом (1898), можно использовать главным образом, для приготовления гидрозолей благородных металлов. Этот метод основан на получении электрической дуги между электродами, состоящими из диспергируемого металла (серебра, золота). Под воздействием высокой температуры происходит испарение материала электродов в дисперсионной водной среде. Затем пары металла конденсируются в коллоидные частицы, образуя соответствующий золь. Процесс проводят при охлаждении.
Метод самопроизвольного диспергирования. Этот метод может быть использован для получения растворов высокомолекулярных веществ из твердых полимеров диспергированием их в соответствующих растворителях, как, например, при растворении в воде крахмала, гуммиарабика, желатина, сухого белка, агар-агара.
Метод самопроизвольного диспергирования твердого вещества в жидкой среде приводит к образованию двухфазной устойчивой коллоидной системы. Самодиспергирование совершается без внешних механических воздействий на этот процесс; так, например, некоторые масла могут самопроизвольно эмульгироваться в воде при наличии в среде стабилизатора (15 – 35% натриевого мыла).
