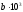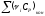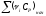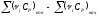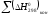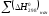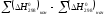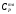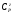курсовая
.docx1. Закон Кирхгофа
Вывести аналитическую зависимость теплового эффекта (Дж/Кмоль) реакции (А) от температуры, если известен тепловой эффект этой реакции при 298 К. (Уравнение зависимости Ср=f(Т) взять из справочника физико-химических величин под редакцией К.П. Мищенко и А.А. Равделя. 1974). Вычислить тепловой эффект реакции при температуре Т.
|
Уравнение реакции (А) |
Т, К |
|
2CO + SO2 = 1/2S2(г) + 2CO2 |
900 |
|
Вещество |
ΔН0, кДж/моль |
Коэффициенты, Дж/моль·К |
Температурный интервал |
|||
|
а |
|
|
||||
|
S2(г) |
129,1 |
36,11 |
1,09 |
-3,52 |
273-2000 |
|
|
CO2 |
-393,51 |
44,14 |
9,04 |
-8,53 |
298-2500 |
|
|
SO2 |
-296,9 |
42,55 |
12,55 |
-5,65 |
298-1800 |
|
|
CO |
-110,5 |
28,44 |
4,10 |
-0,46 |
298-2500 |
|
|
|
— |
106,34 |
18,63 |
-18,82 |
|
|
|
|
— |
99,43 |
20,75 |
-6,57 |
|
|
|
|
— |
6,91 |
-2,12 |
-12,25 |
|
|
|
|
-722,47 |
— |
— |
— |
|
|
|
|
-517,9 |
— |
— |
— |
|
|
|
|
-204,57 |
— |
— |
— |
|
|
Уравнение зависимости:
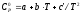
Уравнение Кирхгофа:
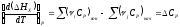
Для
вычисления теплового эффекта процесса
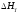 при Т=900
К (P=const),
если известен
тепловой эффект процесса
при Т=900
К (P=const),
если известен
тепловой эффект процесса
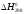 при Т=298
К уравнение Кирхгофа нужно
проинтегрировать:
при Т=298
К уравнение Кирхгофа нужно
проинтегрировать:
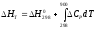
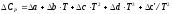 ,
,
где а, b, c, d, c’ – коэффициенты, определяемые эмпирически.
Отсюда получаем:


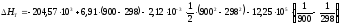
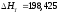 кДж/моль
кДж/моль
-
Расчет энтропии различных процессов.
Исходные данные:
|
№ варианта |
Вещество |
T1, К |
T2, К |
g, кг |
Плавление |
Испарение |
Удельная тепло- емкость, Дж/(кг·К) |
||||
|
Tпл, К |
ΔHпл ∙10-3, Дж/ моль |
Tисп, К |
ΔHисп ∙10-3, Дж/ моль |
∙10-3 |
∙10-3 |
∙10-3 |
|||||
|
10 |
C2H6O |
373 |
143 |
50 |
158,4 |
4,626 |
351,5 |
38,604 |
1,277 |
2,303 |
1,826 |
В процессе охлаждения этанола от T1 до T2 происходят следующие процессы:
-
Охлаждение газообразного этанола от T1 до Tкип.
-
Переход этанола из газообразного в жидкое состояние при Tкип.
-
Охлаждение жидкого этанола от Tкип до Tпл.
-
Переход этанола из жидкого в твердое состояние при Tпл.
-
Охлаждение твердого этанола от Tпл до T2.
Tпл = 158,4 (К); Tкип = 351,5 (К).
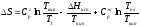 ,
,
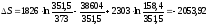 (Дж/(моль∙К));
(Дж/(моль∙К));
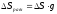 ;
;
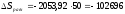 (Дж/(моль∙К));
(Дж/(моль∙К));
 ,
,
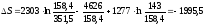 (Дж/(моль·К));
(Дж/(моль·К));
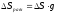 ;
;
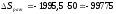 (Дж/(моль∙К));
(Дж/(моль∙К));
Общее изменение энтропии:
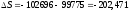 (Дж/(моль∙К)).
(Дж/(моль∙К)).