
|
|
|
Тема 5. Классификация сталей, маркировка 1
5.1. Классификация сталей 1
5.2. Развитие технологических схем производства стали 8
5.3. Маркировка стали и сплавов 9
-
Классификация сталей, маркировка
Сталью называют сплав на основе железа, содержание которого в сплаве выше, чем содержание любого другого металлического (Мn, Сr, Ni, W, V, Мo и др.) или неметаллического (С, Si, S и Р) элемента, а содержание углерода не превышает 2,14 %.
Сталь обладает разнообразными свойствами: способностью к деформации в нагретом и холодном состоянии, хорошей свариваемостью, хорошей обрабатываемостью резанием, высокими твердостью, пластичностью и износостойкостью, высокой коррозионной стойкостью, способностью выдерживать высокие и низкие температуры.
-
Классификация сталей
Единой мировой системы классификации стали нет. В России классификация стали и требования к ее составу и качеству обусловливаются соответствующими государственными стандартами и техническими условиями. Полученные тем или иным способом стали чрезвычайно разнообразны по своим свойствам.
Сталь классифицируется по назначению, химическому составу, характеру затвердевания, качеству и способу производства.
1. По назначению. По этому признаку можно выделить следующие основные группы сталей: конструкционные, инструментальные и специальные.
К конструкционным относятся стали для изготовления деталей механизмов и машин, и элементам конструкций. Им предъявляется определенный уровень механических свойств, определяемых при статических и динамических нагрузках.
К инструментальным относятся стали, отличающиеся высокой твердостью, прочностью, износостойкостью, что позволяет изготавливать из них инструмент для обработки давлением или резаньем.
Специальные стали отличаются особыми химическими и физическими свойствами (нержавеющая, трансформаторная, электротехническая, шарикоподшипниковая и т.д.).
2. По химическому составу. Различают стали углеродистые и легированные.
В сталях большинства марок главной полезной примесью является углерод. Такие стали называются углеродистыми. Углеродистые стали, делятся на три подгруппы:
малоуглеродистые содержание углерода в стали до 0,2%;
среднеуглеродистые от 0,3 до 0,8%;
высокоуглеродистые более 0,8%.
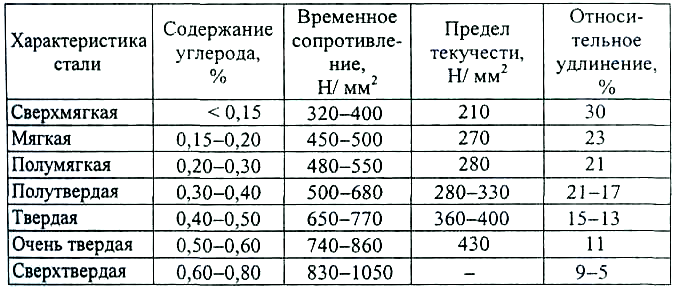
В равновесном состоянии (после медленного охлаждения) твердость и хрупкость углеродистой стали увеличивается с повышением содержания углерода. Стали с низким содержанием углерода называют мягкими, с высоким содержанием углерода - твердыми (табл. 5.1-1).
Таблица 5.1-1
Механические свойства углеродистых сталей в зависимости
от содержания углерода
Углеродистые стали обладают рядом существенных недостатков:
высокой критической скоростью закалки (наименьшей скоростью охлаждения, при которой образуется мартенсит);
плохой прокаливаемостью (глубина проникновения закалки от охлаждаемой поверхности к центру);
низкой антикоррозионной стойкостью и т.д.
Введение в сталь в определенных количествах элементов, называемых легирующими, позволяет устранить указанные недостатки углеродистой стали, а также получить те или иные особые физико-химические и физико-механические свойства, которыми углеродистая сталь не обладает. Такую сталь называют легированной.
Легирующим называют элемент, вводимый в сталь для получения определенных свойств. Элементы, содержание которых в стали связано со способом производства не являются легирующими. Наиболее используются следующие легирующие элементы:
Ni, Mn, Cr – стабилизируют -фазу;
Si – стабилизирует -фазу;
V, Mo – образует дисперсные фазы.
Легированные стали делятся по содержанию легирующего элемента:
на низколегированные – легирующих элементов до 3%;
среднелегированные 3-10%;
высоколегированные более 10%.
Низко- и среднелегированные, как правило, являются конструкционными сталями. Высоколегированные – инструментальные и специальные.
3. По характеру затвердевания сталь подразделяется на кипящую, спокойную и полуспокойную.
Кипящая это сталь, затвердевающая с признаками кипения. Эффект кипения производится образованием газа СО по химической реакции
[C] + [O] = {CO}. (5.1-1)
Реакция возможна при наличии растворенного кислорода в металле. Из-за повышенного содержания кислорода в металле ([О] ≥ 0,025%), такая сталь называется малораскисленной.
Спокойная это сталь, затвердевающая без признаков кипения, т.е. сталь с низким содержанием кислорода в металле ([О] ≤ 0,003%); такая сталь называется глубокораскисленной.
Полуспокойная это сталь, занимающая промежуточное положение по характеру затвердевания и степени раскисленности ([О] ≤ 0,012%) между спокойной и кипящей сталью.
4. По качеству. Стали обычно делят на группы, различия между которыми заключается в допускаемом содержании вредных примесей (фосфора и серы):
стали обычного качества, в них содержание фосфора и серы допускается до 0,045%;
качественные до 0,035%;
высококачественные до 0,025%;
особовысококачественные фосфора до 0,025%, серы до 0,015%.
5. По способу производства. В основу классификации положено физическое состояние получаемого продукта:
производство стали в твердом состоянии;
в размягченном состоянии;
в жидком состоянии (литая сталь).
Способы получения стали в твердом состоянии
Сущность получение железа путем непосредственного восстановления из руд углем или восстановительными газами. Температура процесса 1100оС. Температурный режим исключает расплавление оксидов пустой породы шихтового материала и расплавление металла. Готовый продукт железа получается в виде губки и называется губчатым железом.
Известны две разновидности процессов получения губчатого железа:
1. Восстановление оксидов железа в подвижном фильтрующем слое; агрегатом для этого служит шахтная печь (объем до 40 м3). Восстановитель – подогретые восстановленные газы, получаемые путем углекислотной конверсии природного газа
CH4 + CO2 = 2CO + 2H2 . (5.1-2) Эта же реакция используется в процессе Виберга для регенерации отработанных газов.
Степень металлизации руды 86-96%. Чистота губчатого железа определяется чистотой рудного материала.
2. Восстановление в стационарном фильтрующем слое; агрегатом для этого служат периодически действующие реакторы. Восстановитель тот же. Степень металлизации руды 92-98%.
Это основные способы получения сырья для порошковой металлургии железа. Губка подвергается дроблению и сепарации.
Способы получения стали в размягченном состоянии
Особенность процессов протекание восстановления в интервале температур 1250-1350оС, в котором уже протекает расплавление оксидов пустой породы шихтовых материалов с образованием шлака.
Готовое железо получается в виде размягченных частичек, сваренных между собой.
Готовый продукт этих процессов конгломерат спекшихся частиц металла и шлака, называемый крица. Отделение шлака осуществляется путем нагрева крицы до температур 1100-1200 оС и проковки ее на молотах. В процессе проковки происходит отделение жидкого шлака, а также сваривание частиц железа в единый монолит, т.е. готовым продуктом является сварочное железо, которое отличается высокой коррозионной стойкостью.
По существу процессов различают следующие разновидности:
1. Непосредственное восстановление из руд. Процессы протекают в контакте расплавленных материалов, раскаленный уголь, руда и сырое дутье. Этот процесс называется сыродутным. Современный его аналог руднокричный процесс. Осуществляется во вращающихся печах. Недостатки: низкая производительность, низкая степень восстановления железа.
-
Восстановление из чугуна. Путем окисления его примесей. Осуществляется в кричных горнах в контакте раскаленной руды и чугуна. Примеси окислялись за счет кислорода руды.
-
Пудлинговый процесс. На поду плазменно-отражательной печи. Путем перемешивания в ванне жидкого чугуна и железистого шлака. Современный аналог процесс Астон-Байерс. Предварительно продутый в конвертере жидкий металл сливается в шлаковую чашу, заполненную расплавленной рудой при температуре 1250-1350оС. При контакте капель металла и руды происходит тот же процесс взаимодействия.
Способы получения стали в жидком состоянии (литая сталь)
Характерная особенность температура процесса 1600-1650 оС. Процессы классифицируют по типу агрегата: конвертерные, мартеновские, электропечные. Сталь соответственно называется конвертерная, мартеновская, электропечная. В настоящее время 99% стали получается в жидком состоянии по двухстадийной схеме «чугун-сталь», то есть на первой стадии получают из руды полупродукт – чугун, а на второй литую сталь. Примерный химический состав чугуна и готовой стали, температуры ликвидуса (tликв) и выпуска (tвып) приведены в табл.5.1-2.
Таблица 5.1-2
Характеристика чугуна и сталей
|
Материал |
Химический состав, % |
Температура, оС |
|||||
|
C |
Si |
Mn |
P |
S |
tликв |
tвып |
|
|
Чугун |
3,8- 4,5 |
0,75-1,25 |
0,6-1,75 |
0,2-0,3 |
0,02-0,08 |
1250 |
1400 |
|
Сталь: спокойная
кипящая |
0,2-0,8 0,2 |
0,17-0,37 |
0,5-0,6
0,25 |
0,025 - 0,045 -"- |
0,015 -0,045 -"- |
1480 - 1520 |
1620-1650 |
Сталь выпускается при температуре tликв + t, где t - технологический перегрев металла, необходимый для проведения различных процессов (легирования, внепечной обработки, разливки стали и т.д.), которые связаны с охлаждением стали и t 100-150 о.
Согласно данным табл. 5.1-2 можно отметить две технологических задачи, которые необходимо решать при переработке чугуна в сталь:
-
снижение концентрации примесей путем их окисления кислородом;
-
нагрев металла до температуры выпуска.
Рассмотрим сталеплавильные процессы. Их отличие заключается в способе нагрева металла и способе введения кислорода.
В конвертерных процессах высокие температуры, необходимые для процесса развиваются за счет экзотермических реакций окисления примесей. Кислород необходимый для окисления примесей вводится в виде воздуха или технически чистого кислорода.
Мартеновский процесс. Основной источник тепла для нагрева металла сжигание топлива в рабочем пространстве печи. В факеле горения смешиваются воздух, нагретый до температуры 1100-1200 оС, природный газ и мазут. Нагрев воздуха проводят с использованием регенерации дымовых газов.
Основным источником кислорода для окисления примесей является газовая фаза рабочего пространства печи это продукты горения топлива (СО2, СО, Н2О, О2изб).
Дополнительным источником кислорода в процессе является кислород оксидов железной руды (агломерат или окатыши) и технически чистый кислород.
В электросталеплавильном процессе задача нагрева металла решается за счет преобразования электрической энергии в тепловую. В зависимости от способа преобразования энергии различают печи дуговые, индукционные, сопротивления и электронно-лучевые. Наиболее распространенный агрегат дуговая сталеплавильная печь, где электрическая энергия преобразуется в тепловую в электрической дуге (температура дуги более 3000 оС).
Основной источник кислорода для окисления примесей это кислород оксидов железной руды и технически чистый кислород.
Дополнительный источник – кислород газовой фазы.

