
Итог
.pdfс возрастом, кроме того, появляются возрастные различия между повышением систолического и диастолического давления — среди пожилых людей самой частой формой артериальной гипертензии является изолированная систолическая гипертензия); пол (в возрасте до 40 лет артериальная гипертензия чаще встречается у мужчин, чем у женщин, в более старших возрастных группах это преобладание мужчин не столь значительно выражено); постменопаузальный период..
патогенез
https://studfile.net/preview/3385066/page:3/
3. Вазоренальная артериальная гипертензия: этиология, механизмы развития.
Вазоренальная гипертензия (ВРГ) — одна из форм симптоматической АГ, развивающаяся вследствие нарушения магистрального кровотока в почках без первичного поражения почечной паренхимы и мочевыводящих путей.
ричин развития артериальной гипертензии, которые подразделяют на врожденные и приобретенные. Среди врожденных наиболее часто встречаются: • фиброзно-
мышечная дисплазия почечных артерий; • гипоплазия почечной артерии и почки; • экстравазальная компрессия почечной артерии; • аневризмы почечных артерий; • артерио-венозные свищи. Приобретенные факторы развития : • атеросклероз; • неспецифический аортоартериит; • нефроптоз; • инфаркт почки; • травма; • расслаивающаяся аневризма аорты. Атеросклероз — основная причина вазоренальной гипертензии у лиц старше 40 лет, на его долю приходится 60—85% случаев. Атеросклеротические бляшки локализуются преимущественно в устье или в проксимальной трети почечной артерии. В подавляющем большинстве случаев наблюдается одностороннее поражение, тогда как двустороннее встречается примерно в 1/3 случаев и приводит к более тяжелому течению ВРГ. Правая и левая почечные артерии поражаются одинаково часто. В 10% случаев атеросклероз почечных артерий может осложняться тромбозом. Заболевание чаще (в 2— 3 раза) встречается у мужчин. Фиброзно-мышечная дисплазия (ФМД) как причина вазоренальной гипертензии занимает второе место после атеросклероза. Она встречается преимущественно в молодом и даже детском возрасте (от 12 до 44 лет), средний возраст составляет 28—29 лет. У женщин ФМД обнаруживается в 4—5 раз чаще, чем у мужчин. Морфологически это патологическое состояние проявляется в виде дистрофических и склерозирующих изменений, захватывающих преимущественно внутреннюю и среднюю оболочку почечных артерий и их ветвей. При этом гиперплазия мышечных элементов стенки может сочетаться с образованием микроаневризм. В результате наблюдается чередование участков сужений и расширений (аневризм), что придает артериям своеобразную форму — в виде ниток жемчуга или бус. Патологический процесс хотя и имеет распространенный характер, но в 2/3 случаев бывает односторонним. Неспецифический аортоартериит стоит на третьем месте по частоте среди причин ВРГ (до 10%). Для него характерно первичное поражение средней оболочки сосуда. Воспалительная инфильтрация медии с переходом на адвентицию и интиму завершается склерозированием и разрушением эластического каркаса почечной артерии, что приводит к стенозированию ее просвета. Патологический процесс в основном ограничивается проксимальным сегментом сосуда и практически никогда не распространяется на внутриорганные его ветви. В отличие от фибромускулярной дисплазии при неспецифическом аортоартериите всегда имеется различной степени выраженности поражение аорты. Вазоренальная гипертензия может развиться вследствие экстравазальной

компрессии почечной артерии, в результате тромбоза или эмболии почечной артерии, образования аневризмы, гипоплазии главных почечных артерий, нефроптоза, опухоли, кисты, аномалии развития почек и др.
патогенез https://studfile.net/preview/1857638/page:2/
4. Ренопривная артериальная гипертензия: этиология, механизмы развития.
— симптоматическая (вторичная) артериальная гипертензия, вызванная врожденным или приобретенным заболеванием почек, которое приводит к существенному уменьшению их массы.
Причина ренопривной гипертензии — уменьшение массы паренхимы почек,
вырабатывающей БАБ с гипотензивным действием (ПГ групп Е и I с сосудорасширяющим эффектом, брадикинин и каллидин). Чаще всего это наблюдается при двусторонних (гломерулонефриты, диабетическая нефропатия, тубулоинтерстициальный нефрит, поликистоз) и односторонних поражениях почек (пиелонефрит, опухоль, травма, одиночная киста почки, ее гипоплазия, туберкулез). Наиболее частая причина — диффузный гломерулонефрит.
Патогенез. В патогенезе ренопаренхиматозной артериальной гипертензии ключевое значение имеют: — гиперволемия; — гипернатриемия (из-за уменьшения количества функционирующих нефронов и активации ренин-ангиотензиновой системы); — увеличение ОПСС при нормальном или сниженном сердечном выбросе.
5. Эндокринные артериальные гипертензий: виды, этиология и механизмы развития.
Надпочечники — главный эндокринный орган, обеспечивающий регуляцию системного АД. Все гормоны надпочечников в норме имеют более или менее выраженное отношение к регуляции АД, а в патологии участвуют в формировании и закреплении повышенного АД. Надпочечниковые артериальные гипертензии подразделяются на две группы — «катехоламиновые» и «кортикостероидные».
«Катехоламиновые» гипертензии — катехоламины одновременно увеличивают тонус сосудов и стимулируют работу сердца. Гипертензии развиваются в связи со значительным увеличением в крови уровня катехоламинов — и адреналина, и норадреналина, вырабатываемых хромаффинными клетками.
«Кортикостероидные» артериальные гипертензии. Их разделяют на минералокортикоидные и глюкокортикоидные. Повышенная чувствительность сердца и стенок артерий к гормонам с гипертензивным действием
Минералокортикоидные артериальные гипертензии развиваются в результате избыточного синтеза минералокортикоида альдостерона (при первичном и вторичном гиперальдостеронизме).
глюкокортикоидные артериальные гипертензии являются результатом гиперпродукции глюкокортикоидов с минералокортикоидной активностью (в основном 17гидрокортизона, гидрокортизона — на его долю приходится 80%; остальные 20% — кортизон, кортикостерон, 11-дезоксикортизол и 11-дезоксикортикостерон).
Артериальные гипертензии глюкокортикоидного генеза развиваются при болезни и синдроме Иценко-Кушинга (см. в приложении «Справочник терминов»). Артериальная гипертензия при эндокринопатиях щитовидной железы. Встречается как при гипертиреозе, так и при гипотиреозе.
6. Центральные артериальные гипертензий: этиология и механизмы развития.
Корковые и подкорковые нейроны, участвующие в регуляции АД, представляют собой сложную функциональную систему, состоящую из прессорногипертензивной и депрессорно-гипотензивной подсистем.
В норме доминируют прессорно-гипертензивные механизмы.
Главной структурой, регулирующей системное АД, является кардиовазомоторный
(сосудодвигательный) центр. Его эфферентные влияния изменяют как тонус сосудов, так и функцию сердца.
Наиболее частые причины центрогенных нейрогенных гипертензий:
—расстройства ВНД (невротические состояния);
—органические поражения структур мозга, регулирующих системную гемодинамику.
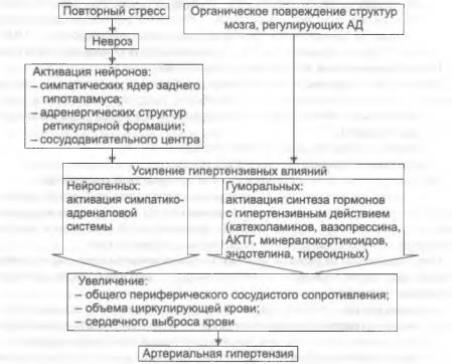
Основные звенья патогенеза центрогенных нейрогенных артериальных гипертензий
Патогенез артериальных гипертензий, вызванных нарушением ВНД (неврозом)
Повторные и затяжные стресс-реакции с негативной эмоциональной окраской вызывают цепь взаимозависимых прогрессирующих изменений. Наиболее важны:
—перенапряжение и срыв основных корковых нервных процессов (возбуждения и активного коркового торможения), нарушение их сбалансированности и подвижности, приводящее к невротическому состоянию;
—развитие невроза (инициального патогенетического звена артериальных
гипертензий центрогенного характера) обусловливает формирование
корково-подкоркового комплекса возбуждения (доминанты возбуждения); этот комплекс включает симпатические ядра заднего гипоталаму-
са, адренергические структуры ретикулярной формации и кардиовазомоторного центра;
—усиление влияний симпатической нервной системы на органы и ткани; характеризуется высвобождением избытка катехоламинов и повышением под их влиянием тонуса стенок артериальных и венозных сосудов, а также
увеличением ударного и минутного выброса крови из сердца, что и приводит к повышению как систолического, так и диастолического АД;
—активация (в связи с возбуждением подкорковых нервных центров) и других
центральных «гипертензивных» систем. Основной среди них является система «гипоталамус — гипофиз — надпочечники»; это сопровождается
увеличением продукции и концентрации в крови гормонов с гипертензивным действием (АДГ, АКТГ и кортикостероидов, включая минералои глюкокортикоиды, а также катехоламинов, тиреоидных гормонов);
— потенцирование степени и длительности сужения артериол и венул, увеличения ОЦК, повышения сердечного выброса.
7. Рефлекторные артериальные гипертензий: этиология и механизмы развития, виды.
Рефлекторные (рефлексогенные) нейрогенные артериальные гипертензии могут развиваться на основе условных и безусловных рефлексов.
Условнорефлекторные артериальные гипертензии
Известны случаи развития рефлекторной гипертензии в форме так называемой артериальной гипертензии «белого халата». Для нее характерно повышение АД в лечебном учреждении, в то время как за его пределами АД
нормальное. При проведении суточного мониторирования АД находят нормальные величины среднесуточного АД: менее 125/80 мм рт.ст.
Причина рефлекторных гипертензий — повторное сочетание индифферентных (условных) сигналов (например, информации о предстоящем публичном
выступлении, важном соревновании или событии) с действием агентов, вызывающих повышение АД (например, кофеина, адреномиметиков, психостимуляторов, алкоголя или наркотиков).
После определенного числа сочетаний увеличение АД регистрируется уже только на индифферентный сигнал. Через некоторое время может развиться стойкое повышение АД.
Так, описан случай артериальной гипертензии у человека, принимавшего перед чтением лекций и докладов кофеин (для психологического допинга). Вскоре у него регистрировалось повышение АД до 180 и 115 мм рт.ст. уже
при одной мысли о предстоящей лекции. Спустя несколько лет у этого человека развилась артериальная гипертензия.
Безусловнорефлекторные артериальные гипертензии
Безусловнорефлекторные артериальные гипертензии развиваются в результате:
—хронического раздражения экстеро- и интерорецепторов, нервных стволов и нервных центров;
—прекращения «депрессорной» афферентной импульсации.
8. Артериальная гипотензия: этиология и механизмы развития. https://studfile.net/preview/2711376/page:10/
Артериальная гипотензия — уменьшение АД ниже нормы: 100/60 мм рт.ст. у мужчин и 95/60 мм рт.ст. у женщин (границы нормн при хорошем самочувствии и полной работоспособности).
По инициальному звену механизма развития выделяют нейрогенные, эндокринные и метаболические артериальные гипотензии
Нейрогенные артериальные гипотензии выделяют гипотензии:
—центрогенные;
—рефлекторные (рефлексогенные).
Рефлекторные (рефлексогенные, проводниковые) центрогенные артериальные гипотензии.
†Причина: нарушение проведения эфферентных гипертензивных импульсов от сосудодвигательного центра продолговатого мозга к стенкам сосудов и сердцу. Наиболее часто это развивается при нейросифилисе, боковом амиотрофическом склерозе, сирингомиелии, периферических невропатиях различного генеза (например, диабетического, инфекционного, нейротоксического).
†Механизм развития. Заключается в значительном уменьшении или прекращении тонических влияний симпатической нервной системы на стенки сосудов и сердца. Это приводит к снижению ОПСС и, соответственно — диастолического АД, а также к уменьшению сократительной функции сердца, величины сердечного выброса и систолического АД. В результате развивается артериальная
гипотензия.
Нейрогенные гипотензии центрогенного генеза являются результатом либо функционального расстройства ВНД, либо органического повреждения мозговых структур, участвующих в регуляции АД.
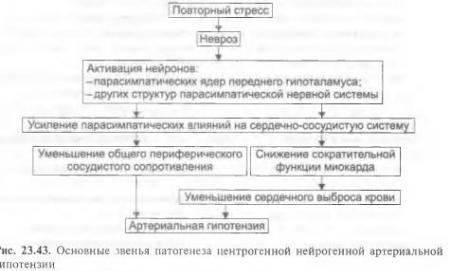
† Артериальные гипотензии вследствие нарушений ВНД.
‡Причина: длительный, повторный стресс, обусловленный необходимостью сдерживания двигательных и эмоциональных проявлений. Это приведёт к развитию невротического состояния.
‡Механизм развития.
§ Перенапряжение (и срыв) ВНД — невроз. Он является инициальным звеном патогенеза гипотензии.
§ Невроз характеризуется формированием корково-подкоркового комплекса возбуждения. Оно распространяется на парасимпатические ядра переднего гипоталамуса и другие структуры парасимпатической нервной системы (например, на дорсальное двигательное ядро блуждающего нерва).
§ Активация парасимпатических влияний на ССС обусловливает снижение сократительной функции миокарда, сердечного выброса крови и тонуса резистивных сосудов. Развивается артериальная гипотензия.
Аргументом приведенным выше представлениям является большой «удельный вес» людей со слабым типом ВНД (с высокой частотой развития у них невротических состояний) среди больных артериальной гипотензией.
Считают, что именно такой механизм лежит в основе развития гипотонической болезни.
9.Метаболические расстройства при экстремальных состояниях.
Можно выделить несколько основных тенденций нарушений метаболизма в критических состояниях. Это прежде всего повышение интенсивности энергетического обмена, лизис протоплазмы и клеточных белков с образованием аминокислот и последующим выходом их во внеклеточное пространство, нарушение электролитного баланса с потерей клеткой К+ и
заменой его Na+ и Н+, задержка Na+, воды, С1— и НСО3—, а также усиленное образование жирных кислот из нейтральных триглицеридов и, наконец, активация практически всех эндокринных функций
10.Нарушение основных физических функций при экстремальных состояниях.
1. Система кровообращения
При всех экстремальных состояниях развиваются сходные расстройства микроциркуляции, нарушение пер фузии микрососудов, расширение капилляров, прекапилярных сфинктеров и венул, снижение их чувствительности к вазопрессорным влияниям, увеличение проницаемости сосудистых стенок и их структурные нарушения. Возникает патологическая агрегация эритроцитов - «сладжсиндром», гиперкоагуляция крови, диссеминированное внутрисосудистое свертывание крови (ДВС), мик ротромбоз сосудов, явления стаза.
Расстройства микроциркуляции проводят к «шоково му легкому» или «шоковой почке» (расстройства газооб мена и почечной недостаточности). То же может происхо дить в печени и мозге. При экстремальном состоянии имеют место рас стройства системной гемодинамики в виде уменьшения объема циркулирующей крови, снижением венозного воз врата крови к сердцу, падением тонуса артериол и вен. Со стороны сердца часто
наблюдается тахикардия, различные формы аритмий, недостаточность коронарного кровотока, уменьшение сердечного выброса и др. признаки сердеч ной недостаточности.
2. Система внешнего дыхания
Расстройства возникают после периода гипервенти ляции. Они характеризуются изменениями глубины и час тоты, соотношения фаз вдоха и выдоха, периодическими феноменами (волнообразное дыхание, дыхание типа Биота и Чейн-Стокса), может наблюдаться дыхание типа Куссмауля и другие патологические формы. При экстренных состояниях могут нарушаться также легочная перфузия и процесс альвеоло-капиллярной диффузии.
3. Нервная система
Страдают все нервные процессы: корковые, вегета тивные, локомоторные, сенсорные. Но эти нарушения ха рактерны для разных видов экстремальных состояний.
4. Нарушение функции почек
Проявляются в преходящей или стойкой олигоили анурии, протеинурии и др. изменений качественного со става мочи, общей недостаточности выделительной функ ции почек вплоть до уремии.
5. Нарушение функции печени
Сопровождается ослаблением процессов детоксикации, синтеза мочевины, белковосинтетических процессов, диспротеинемией, расстройствами углеводного и других видов обмена.
11.Этиология и патогенез коллапса.
Коллапс - вид острой сосудистой недостаточности, характеризующийся резким понижением артериального и венозного давления и снижением массы циркулирующей крови в сосудистой системе.
По этиологии различают следующие виды коллапса: 1. Токсико-инфекционный. Развивается при кишечных инфекциях (дизентерия, сальмонеллез и др.), возбудители которых выделяют эндотоксин, высвобождающийся при гибели микробных тел.
При интенсивной антибактериальной терапии может возникнуть одномоментная гибель огромного количества микробов. Высвобождающиеся при этом большие дозы эндотоксина вызывают поражение нервно-мышечного аппарата стенки сосудов с последующей их атонией, что и приводит в конечном итоге к состоянию коллапса.
2. Постгеморрагический. Возникает при острой массивной кровопотере и связан с быстрым уменьшением объема циркулирующей крови и снижением тонуса сосудов.
3.Панкреатический. Может наступить при тяжелой травме живота, сопровождающейся размозжением ткани поджелудочной железы и поступлением в кровь панкреатического сока. Установлено, что трипсин, действуя на гладкую мускулатуру сосудистой стенки, вызывает резкое снижение ее тонуса, что приводит к развитию коллапса.
4.Аноксический. Возникает при быстром снижении парциального давления кислорода во вдыхаемом воздухе. Развивающаяся в этом случае гипоксия вызывает снижение тонуса гладкой мускулатуры сосудистой стенки, что приводит, в свою очередь, к резкому расширению сосудов.
5. Ортостатический. Возникает у больных после длительного (многодневного) постельного режима при резком переходе из горизонтального положения в вертикальное. Патогенез.В развитии этого вида острой сосудистой недостаточности важную роль играет снижение тонуса емкостных сосудов (преимущественно мелких вен), в которых обычно сосредоточена основная масса (75-80%) крови. Такая ситуация может возникнуть вследствие прямого действия различных токсинов на гладкую мускулатуру сосудов или явиться результатом снижения тонической активности симпатоадреналовой системы в сочетании с ваготонией. Депонированная кровь не участвует в циркуляции, что приводит к снижению объема циркулирующей крови. Итогом этих изменений является уменьшение венозного притока крови к сердцу и вторичное снижение сердечного выброса, в результате чего патологический процесс усугубляется. В дальнейшем при прогрессировании сосудистой недостаточности развивается гипоксия тканей, нарушаются окислительно-восстановительные процессы и возникает ацидоз. Сознание может быть сохранено.
, этиология, патогенез коллапсов
В патогенезе коллапса ведущее значение имеет остро возникающее несоответствие между объемом циркулирующей крови (неизмененном или чаще сниженном) и объемом сосудистого русла (чаще увеличенном или неизмененном). Отмечаемое при коллапсе перераспределение крови в сосудистом русле обычно характеризуется увеличением кровенаполнения органов брюшной полости и уменьшением кровенаполнения других органов (кожи, мышц, головного мозга).
Коллапс возникает в результате несоответствия между возросшими метаболическими потребностями мозга и сниженным поступлением в его структуры (особенно кору больших полушарий) крови. Последнее, главным образом, определяется снижением системного АД, обусловленного уменьшением либо общего периферического сопротивления сосудов, либо объема ОЦК, либо сердечного выброса, либо их сочетания.
Важную роль в механизмах развития этого несоответствия играют:
- возбуждение ПСНС, в том числе М-холинорецепторов органов (сердца, сосудов и др.), ганлиев ПСНС, вазодилататорного отдела сердечно-сосудистого центра
(ССЦ);
- избыточное образование и действие вазодилататорных ФАВ (ацетилхолина, гистамина, кининов, простагландинов E, I, A; оксида азота, аденозина, молочной, пировинаградной и кетоновых кислот и др.);
-угнетение СНС, в том числе -адренорецепторов, ганглиев СНС, вазоконстрикторного отдела ССЦ;
-недостаточное образование и действие вазоконстрикторных ФАВ ( HA, A, PgF2, AT-2 и AT-3, вазопрессина и др.);
-неадекватная компенсаторная реакция симпатоадреналовой гипофизкортикоадреналовой, ренин-ангиотензин-альдостероновой системы (РААС) и гипоталамо-нейрогипофизарной вазопрессиновой системы;
- резкое уменьшение содержание в организме ионов натрия и кальция и увеличение ионов калия;
- повышение проницаемости кровеносных сосудов;
-развитие расстройств микроциркуляции и капиллярно-трофической недостаточности;
-расстройство систем крови и гемостаза;
-развитие печеночной недостаточности;
-парез гладких мышц сосудов и др.
Все это сопровождается снижением венозного возврата крови к сердцу, уменьшением диастолического наполнения последнего, падением уровня как ЦВД, так и АД, приводящими к развитию гипоперфузии, гипоксии, нарушений метаболизма и функций органов, в том числе жизненно важных (мозга, сердца, печени, почек, надпочечников и др.).
12.Проявления и принципы терапии коллапса.
Клинические проявления коллапса. Резко выраженная общая слабость
(в связи с чем вынуждены занять горизонтальное положение тела с низко расположенный головой); головокружение, шум или звон в ушах; ухудшение зрения; жажда; зябкость или озноб; общая заторможенность, помутнение, но чаще сохранение сознания, иногда тошнота и даже рвота.
Объективно выявляются бледные кожа тела и слизистые, холодные конечности (особенно стопы ног и кисти рук). Отмечаются тремор (мелкое дрожание) и иногда судорожное подрагивание пальцев рук.
Зрачки расширены, вяло реагируют на свет. Дыхание частое и поверхностное, не сопровождающееся чувством удушья. Отмечается тахикардия. Пульс слабого наполнения. Среднее АД снижено (обычно до величин ниже 70-60 мм рт.ст.).
Выявляются признаки коронарной недостаточности, генерализованные расстройства микроциркуляции, особенно усиленная адгезия и агрегация эритроцитов и тромбоцитоз, микротромбоз, увеличение гематокритного показателя, замедление кровотока в различных сосудах, развитие циркуляторной гипоксии и метаболического ацидоза. Отмечается олигурия или анурия.
Тяжесть коллапса, как правило, прямо зависит от степени снижения ОЦК, сердечного выброса, АД, ЦВД, ОПС и нарастания циркуляторной гипоксии и метаболического ацидоза.
В течении коллапса, в отличие от шока, фазность не выявляется
Принципы терапии коллапса. Терапия коллапса должна быть эффективной и начата как можно скорей. Особое место должно занимать комплексное этиотропное и патогенетическое лечение.
С целью нормализации несоответствия между сниженным тонусом сосудов (и как следствие увеличенным объемом сосудистого русла) и уменьшенным ОЦК рекомендуется неотложное использование следующих мероприятий и средств.
Прежде всего необходимо быстро и эффективно устранить причину коллапса (например, ликвидировать или уменьшить кровотечение, интоксикацию, микробное обсеменение тканей, использовать необходимые антидоты, детоксиканты, антимикробные средства и др.).
Срочно придать больному (голове и телу) горизонтальное положение, а ноги приподнять.
Нормализовать центральное, органное и микроциркуляторное кровообращение.
Провести трансфузию крови, плазмы или кровозаменителей (реополиглюкина и др.), гемодез, плазмоферез и др. (в целях как восполнения ОЦК, так и нормализации небиологических свойств крови).
Парентерально ввести фармакологические средства для активизации сердечнососудистого центра и сердца (препараты камфоры, кофеина, кардиамина, адреналина и др.).
Назначить сосудосуживающие средства (препараты мезатона, норадреналина, вазопрессина, ангиотензина, эффект которых возрастает при парентеральном введении глюкокортикоидов: дексаметазона, преднизолона, преднизона, кортизола, кортизона и др.)
Нормализовать дыхание (ликвидировать дыхательную недостаточность, подействовать парами аммиака на слизистую носовых ходов, при необходимости назначить искусственную вентиляцию легких или гипербарическую оксигенацию).
Ликвидировать или уменьшить как гемодинамические, так и метаболические (особенно ацидотические) расстройства путем введения растворов глюкозы, бикарбонатов, витаминов, гормонов, ферментных препаратов, гепарина и др.
Назначить антигипоксанты, способные повысить устойчивость тканей организма к недостатку кислорода.
13.Стадии и проявления, основные механизмы развития шока.
Стадии шока. Их краткая характеристика. По предложению крупного советского ученого хирурга Н. Н. Бурденко (1935), в клинике шока выделяют 2 стадии: возбуждения или эректильную (кратковременную) и торможения или тормозную (длительную).
Эректильная стадия характеризуется выраженной активизацией соматической и автономной нервной системы, особенно симпатической и симпато-адреналовой систем, повышением болевой чувствительности, общим двигательным и речевым возбуждением, эйфорией, часто неадекватным поведением, подъемом АД, тахикардией, спазмом периферических сосудов (особенно, кожи) и т.д.
