
Итог
.pdfПовреждение мембранного аппарата, 3 основных механизма:
-внедрение липидов в клетки мембран. Обусловливается высокой способностью проникать и фиксироваться в биомембранах т.н. амфифильных липидов (жирные кислоты, лизофосфатиды, фосфолипиды). Они высвобождаются из липидных компонентов кардиомиоцитов под влиянием причин, вызывающих СН, а также могут захватываться клетками миокарда из плазмы крови, кроме того, внутриклеточное накопление амфифилов т.е. следствием увеличения содержания в них ацил-КоА (в норме окисляется в митохондриях). Накопление в клетках миокарда большого количества амфифилов сопровождается образованием в них мицелл. Включение мицелл в мембраны ведет к разрыву их двойного липидного слоя.
-разрушение гидролазами. Высвобождение и активация гидролаз лизосом, в том числе липаз и протеаз, наблюдается уже в начальном периоде развития СН. Выход ферментов лизосом в саркоплазму кардиомиоцитов является результатом повышения проницаемости их мембран. Попавшие в гиалоплазму энзимы активируются том и гидролизуют белково-липидные комплексы мембран.
-разрушение свободными радикалами и продуктами ПОЛ мембранных липидов, белков. Один из основных механизмов СН. Активация ПОЛ в ткани сердца является следствием: накопления продуктов гидролиза АТФ, увеличением содержания субстратов ПОЛ – жирных кислот, уменьшением содержания и активности антиоксидантов.
Нарушение ионного баланса. Возникает вследствие изменения проницаемости мембран кардиомиоцитов, а также активности ферментов катионного транспорта. В итоге меняется соотношение ионов во внутри- и внеклеточном пространстве. В наибольшей степени это относится к ионам К, Na, Ca, Mg, т.е. к ионам, в основн6ом определяющим реализацию таких процессов как возбуждение, сокращение, расслабление миокарда. СН характеризуется снижением активности К-Na-АТФ-азы и накоплением в кардиомиоцитах ионов Na и потерей К. Увеличение концентрации ионов Na внутри клеток обусловливает задержку в миоплазме ионов Са, что в свою очередь приводит к нарушению расслабления миофибрилл, разобщению свободного и фосфорилирующего окисления→ ↓ содержания АТФ, активации Са-зависимых протеаз и липаз.
Расстройство механизмов нейро-рефлекторной регуляции. В
значительной степени определяет прогрессирующее течение СН. Характеризуется уменьшением концентрации нейромедиатора симпатической нервной системы норадреналина в ткани сердца. Это
17
обусловлено, главным образом, двумя факторами: снижением его синтеза в нейронах СНС (причина - ↓ активности тирозингидроксилазы) и нарушением захвата НА нервными окончаниями из синаптической щели (следствие дефицита АТФ, ацидоза, повреждения мембран нервных окончаний симпатических нейронов).
Аритмии – это нарушения функции сердца, которые проявляются изменениями частоты и регулярности сердечных сокращений, а также сменой водителя ритма и нарушением нормальной последовательности возбуждения и сокращения отделов сердца.
Классификация аритмий.
I.Аритмии вследствие нарушения автоматизма
1.Номотопные:
а) синусовая тахикардия б) синусовая брадикардия в) синусовая аритмия
2.Гетеротопные:
а) предсердный ритм б) атриовентрикулярный ритм
∙с одновременным возбуждением предсердий и желудочков
∙с предшествующим возбуждением предсердий
∙с предшествующим возбуждением желудочков
в) желудочковый ритм г) миграция водителя ритма
II.Аритмии вследствие нарушения функции проводимости
1.по проявлению:
∙замедление и блокада проведения возбуждения
∙ускорение проведения возбуждения
2.по продолжительности:
∙временные
∙постоянные
3.по локализации:
∙синоатриальные
∙межпредсердные
∙атриовентрикулярные
∙внутрижелудочковые
III.Аритмии вследствие нарушения функции возбудимости
1.экстрасистолия
18
∙наджелудочковые (суправентрикулярные) и желудочковые (вентрикулярные)
∙единичные и парные
∙связанные с ритмом (аллоритмии) – экстрасистолы сочетаются
в определенной последовательности с ритмом.
бигемения (экстрасистола после каждого нормального сокращения)
тригемения (после 2х синусовых сокращений)
квадригемения (после3х синусовых сокращений)
∙Редкие (менее 30 в час), частые (> 30 в час.)
∙Мономорфные, полиморфные.
2.пароксизмальные тахикардии
∙наджелудочковые (предсердные, атриовентрикулярные)
∙желудочковые
3.трепетание
∙предсердий
∙желудочков
4.мерцание
∙предсердий
∙желудочков
Как можно понять из приведенной выше классификации, развитие аритмий сердца может быть обусловлено нарушениями 3 основных функций сердца – автоматизма, проводимости и возбудимости.
Автоматизмом у человека обладают атипичные кардиомиоциты, или клетки-пейсмекеры, которые объединяются в проводящую систему сердца (см. рис. 1). Иногда в результате дефектов развития формируются дополнительные проводящие пути, не встречающиеся в норме (пучок Кента, пучок Джеймса на рисунке), которые могут стать причиной нарушений ритма сердца.
Синусовый и атриовентрикулярный узлы имеют обильную вегетативную иннервацию, поэтому изменения их функции (автоматизма и проводимости) зачастую связаны с изменением тонуса симпатической и парасимпатической нервных систем. Нарушения проводимости и возбудимости нижележащих отделов проводящей системы сердца обычно обусловлены гуморальными влияниями либо прямым повреждающим действием на клетки проводящей системы.
19

Рис. 1 Проводящая система сердца
I Аритмии вследствие нарушения функции автоматизма
Номотопные аритмии.
Это нарушения автоматизма, которые характеризуются изменением частоты и регулярности деятельности синусового узла. Локализация водителя ритма при этом не изменяется.
Синусовая тахикардия – увеличение частоты сердечных сокращений выше нормы при генерации импульсов синусовым узлом (нормальная частота сердечных сокращений: в первые 10 лет – 90-100; 10-15 лет – 80-90; до 60 лет- 64-74; старше 60 лет – 50-60 в минуту.
Этиология и патогенез:
∙Эмоциональный стресс, физическая нагрузка, неврозы, страх, эндокринные заболевания (феохромоцитома, тиреотоксикоз, климакс) Механизм: усиление симпатических влияний на сердце.
20
∙Повреждение центральных нервных образований (подкорковых ядер, ретикулярной формации, ядер продолговатого мозга), проводящих путей, парасимпатических ганглиев и нервных стволов, а также снижение холинореактивных свойств миокарда.
Механизм: ослабление парасимпатических влияний на сердце.
∙Прямое действие на клетки синусового узла факторов физической, химической, биологической природы (гипоксемия, ацидоз, повышенная температура, интоксикация, инфекция) при миокардитах, перикардитах, механической травме, кардиосклерозе; никотин, алкоголь, кофеин, наперстянка.
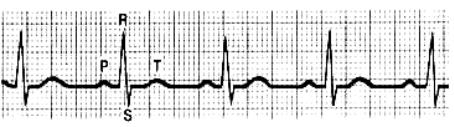
Механизм: прямое воздействие на элементы проводящей системы. Проявления на ЭКГ:
∙Зубец Р синусового происхождения
∙Укорочение интервалов R-R
∙Форма комплексов QRS не изменена
Рис. 2 Синусовая тахикардия. ЧСС 140-150 в секунду.
Синусовая брадикардия – замедление сердечной деятельности ниже 60 ударов в минуту с правильным ритмом (как правило, между 40 и 60 в мин).
Этиология и патогенез
∙Раздражение ядер блуждающего нерва (повышение внутричерепного давления при менингитах, энцефалитах, опухолях, сотрясении головного мозга, мозговых кровоизлияний) или его окончаний; повышение внутрижелудочкового давления и тонуса миокарда – рефлекс Бецольда-Яриша, надавливание на глазные яблоки – рефлекс Ашнера-Даньини, надавливание в зоне проекции бифуркации сонной артерии – рефлекс Геринга; солнечного сплетения; ваго-вагальные рефлексы при почечных, желчных, желудочных и кишечных коликах.
Механизм: активация влияния на сердце парасимпатической нервной системы.
∙Повреждение мозговых структур, например гипоталамуса; проводящих путей, нервных ганглиев и окончаний симпатической нервной
21
системы, снижение адренореактивных свойств миокарда при глубокой гипоксии, ишемии миокарда, особенно с последующей реперфузией. Механизм: снижение симпатоадреналовых воздействий на сердце.
∙Непосредственное воздействие повреждающих факторов физического, химического или биологического генеза на клетки синусового узла (механическая травма, кровоизлияние, инфаркт в зоне синусового узла, токсины, лекарства: хинин, препараты наперстянки, сердечные гликозиды, хинидин, морфий, метаболиты: билирубин, желчные кислоты).
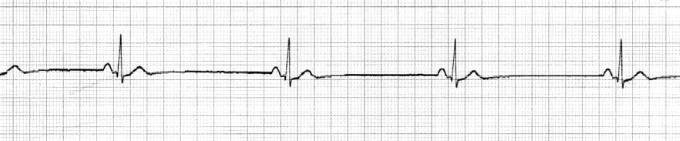
Механизм: прямое воздействие на синусовый узел. Проявления на ЭКГ:
∙Зубец Р синусового происхождения
∙Увеличение продолжительности интервала R-R
∙Форма комплексов QRS не изменена
Рис. 3 Синусовая брадикардия, ЧСС 55 в минуту.
Синусовая аритмия. Характеризуется изменением регулярности генерации импульсов в синусовом узле.
Этиология и патогенез:
∙Нарушение соотношения симпатоадреналовых и парасимпатических воздействий на миокард
∙Колебания содержания в крови газов (СО2, О2), метаболитов (лактата, пирувата, желчных кислот), лекарственных препаратов (наперстянки, опиатов, холинолитиков, симпатолитиков и симпатомиметиков), которые замедляют или учащают сердечную деятельность
∙Действие агентов механического, физического и биологического характера непосредственно на клетки синусового узла (травма, кровоизлияние)
∙Изменение холино- и адренореактивных свойств сердца Проявления на ЭКГ:
∙Зубец Р синусовый, неправильный ритм с разницей между длиной самого большого и самого короткого интервала R-R > 0,16 с и
22
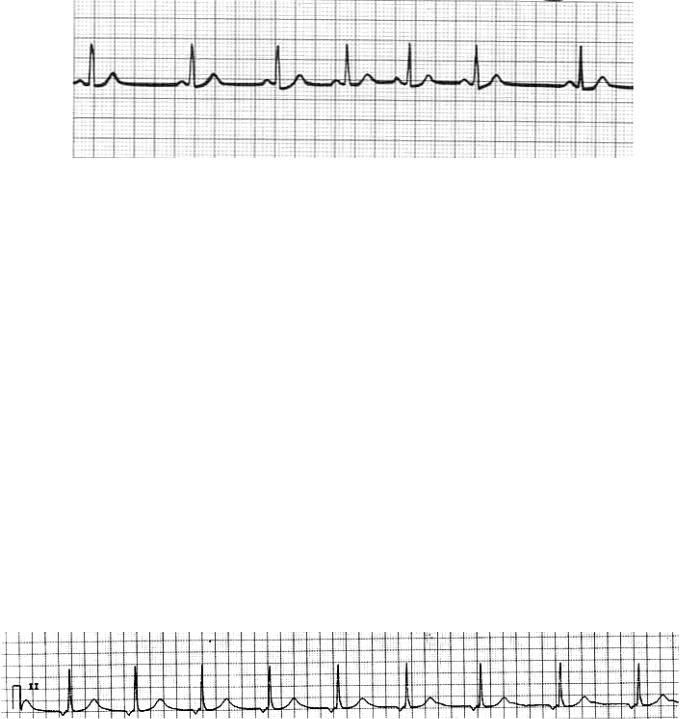
больше (более точный критерий – разница между интервалами R-R более 15%).
Рис. 4 Синусовая аритмия.
Гетеротопные аритмии.
Это нарушения автоматизма, которые характеризуются неспособностью истинного водителя ритма генерировать импульсы либо нарушением проведения их в нижележащие участки проводящей системы.
Этиология и патогенез.
∙Отказ или слабость синусового узла.
∙Полная синоатриальная блокада.
∙АВ-блокада II – III степени
∙Фибрилляция предсердий.
При невозможности поддерживать нормальный синусовый ритм, его функцию на себя берут другие элементы проводящей системы, обладающие меньшей способностью к автоматизму. Эти ритмы еще называют замещающими.
Предсердный медленный ритм. Обычно водитель в левом предсердии.
На ЭКГ:
∙ отрицательный зубец Р во 2,3, АVF, V6 (при нижнепредсердном ритме)
Рис. 5 Предсердный ритм.
Атриовентрикулярный ритм (узловой). Водитель ритма находится в АВ – узле. ЧСС 40-60 в мин. Возможны следующие варианты:
А) с одновременным возбуждением предсердий и желудочков, т.е. импульсы возбуждают предсердия и желудочки одновременно.
На ЭКГ:
23
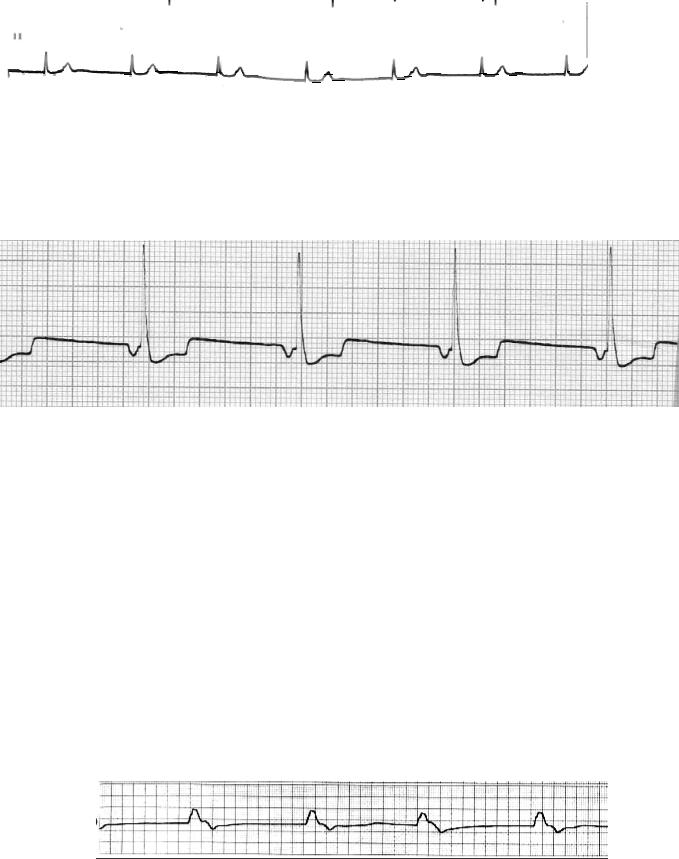
∙Зубец Р отсутствует
∙Комплекс QRS не изменен
Рис. 6 Атриовентрикулярный ритм с одновременным возбуждением предсердий и желудочков
Б) с предшествующим возбуждением предсердий На ЭКГ:
∙ Отрицательный зубец Р перед QRS;
Рис. 7 Атриовентрикулярный ритм с предшествующим возбуждением предсердий
В) с предшествующим возбуждением желудочков На ЭКГ:
∙ Отрицательный зубец Р после QRS
Идиовентрикулярный (желудочковый) ритм носит замещающий характер, при подавлении активности центров первого и второго порядка. Преимущественно импульсы генерируются в пучке Гиса, верхней части межжелудочковой перегородки, в одной из его ножек или их разветвлениях (ритм ножек пучка Гиса) и реже в волокнах сети Пуркинье.
На ЭКГ:
∙Частота ритма 30-40 уд. В минуту
∙Зубец Р отсутствует
∙Комплекс QRS уширен, деформирован, дискордантен с зубцом Т
Рис. 8 Желудочковый ритм
24
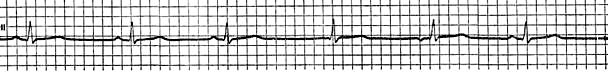
Миграция водителя ритма – перемещение от цикла к циклу пейсмекера из синусового узла в нижележащие отделы сердца (преимущественно в АВ-узел) и обратно. Является результатом периодических изменений интенсивности вагусных влияний на функцию синусного узла. Повышенный тонус вагуса угнетает синусовый узел и центр возбуждения перемещается вниз к атриовентикулярному узлу. При нормальном тонусе блуждающего нерва снова активируется синусовый узел, и центр возбуждения опять возвращается на старое место.
На ЭКГ:
∙ Изменение формы и амплитуды зубца Р: в 1 цикле – нормальный зубец Р, во 2 – амплитуда его меньше, в 3 – зубец Р отсутствует, в 4 – отрицательный зубец Р и далее снова нормальный
Рис. 9 Миграция водителя ритма.
II Аритмии в результате нарушения функции проводимости
Замедление и блокада проведения импульсов
Этиология и патогенез
∙Повышение парасимпатических влияний на сердце и/или его холинореактивных свойств (периферическое или центральное раздражение n. Vagus), в первую очередь влияет на синоатриальную и атриовентрикулярную проводимость.
∙Непосредственное повреждение клеток проводящей системы сердца органическими, химическими и биологическими факторами (травмы, опухоли, соединительнотканные рубцы – у пожилых чаще, перерастяжение сердечной мышцы; интоксикация алкоголем,
никотином, наперстянкой, хинидином, блокаторами β- адренорецепторов; бактериальные яды при дифтерии, скарлатине, брюшном тифе, вирусной инфекции; нарушение трансмембранного распределения ионов (гиперкалиемия)
∙ Болезнь Ленегра |
– склеро-дегенеративное поражение |
обеих |
ножек |
||
пучка |
Гиса без |
поражения миокарда и сосудов. |
Болезнь |
Леви – |
|
склеро-дегенеративное поражение межжелудочковой перегородки. |
|||||
Проведение импульсов нарушается в 2 случаях: либо импульс |
|||||
достигает |
кардиомиоцитов когда они находятся |
в |
состоянии |
||
|
|
25 |
|
|
|
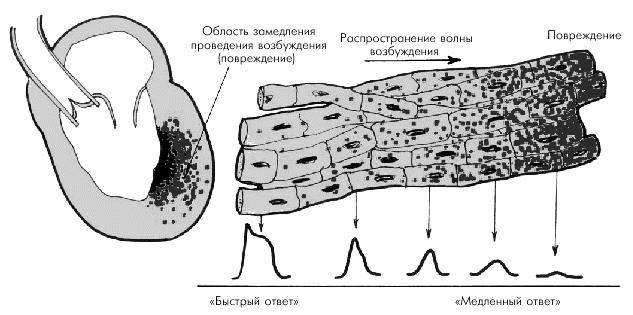
рефрактерности, либо участок ткани теряет способность проводить электрический импульс (при кардиосклерозе). В основе патогенеза блокад лежат следующие механизмы:
∙Удлинение рефрактерного периода
∙Декрементное (затухающее) проведение импульса.
Рис. 10 Схема декрементного проведения импульса по миокарду. Прохождение импульса между двумя возбудимыми участками,
разделенными небольшой зоной высокого сопротивления, сопровождается резким замедлением проводимости в дистальном участке волокна. Такие факторы, как ограниченная ишемия миокарда, местная высокая концентрация ионов К+, локальное сдавление или охлаждение и другие воздействия могут вызвать невозбудимость (т.е. длительный рефрактерный период) в сердечном волокне (волокне Пуркинье) и тем самым способствовать торможению передачи импульса через невозбудимую зону на близлежащие участки.
Синоатриальная блокада – нарушение проведения импульса от синусового узла на предсердия.
На ЭКГ:
∙ Периодическое выпадение комплексов PQRST.
Степень блокады определяется соотношением числа импульсов к числу проведенных импульсов = 4:3, 3:2, 5:4. При полной блокаде или частом выпадении сердечных сокращений происходит смена водителя ритма.
26
