
Таврический национальный университет имени в.И. Вернадского
Факультет биологии и химии
Кафедра органической и биологической химии
ЧЕРКАЕВА ЛЕНАРА НУСРЕТОВНА
Курсовая работа
Специальность 6.040101– химия
Курс 5
Научный руководитель:
доцент кафедры органической и
биологической химии,
кандидат химических наук
С. С. Пертель
Симферополь, 2014
Содержание
ПЕРЕЧЕНЬ УСЛОВНЫХ ОБОЗНАЧЕНИЙ…………………………………
l. Введение …………………………………………………………………….
2. Образование амидной связи: методы и стратегии………………………..
Ацилгалогениды………………………………………………………..
2.1.1. Ацилхлориды…………………………………………………………….
2.1.1.1. Образование ацилхлорида…………………………………………….
2.1.1.2. Реакции конденсации с использованием ацилхлоридов……………
2.1.1.3. Ограничения метода ацилхлоридов………………………………….
2.2. Ацилазиды………………………………………………………………...
2.3. Ацилимидозолы с использованием CDI………………………………...
2.4. Ангидриды………………………………………………………………..
2.4.1. Симметричные ангидриды. ……………………………………………
2.4.2. Смешанные ангидриды…………………………………………………
2.4.2.1. Смешанные карбоксильные ангидриды……………………………..
2.4.2.2. Смешанные карбоновые ангидриды…………………………………
2.4.2.2.1. О-Ацилизомочевина (с использованием карбодиимдов
как конденсирующих реагентов). ……………………………………………
2.5. Эфиры……………………………………………………………………..
2.5.1. Алкильные эфиры…………..………………………………………….
2.5.2. Активированные эфиры..………………………………………………
2.5.2.1. Многостадийные процедуры………………………………………..
2.5.2.1.1. Сукцинимидильные эфиры. ………………………………………
2.5.2.1.2. Использование 1,2,2,2-тетрахлороэтил хлорформната
как интермедната. …………………………………………………………….
3. Заключение…………………………………………………………………
Литература…………………………………………………………………….
Перечень условных обозначений:
DMF - трифенилфосфин
ТРР - диметилформамид
DMAP - N,N-диметиламинопиридин
DPPA – дифенилфосфоний
CDI - карбонил диимидазол
CBMIT - Трифлат N,N`-карбонил-бис(З-метилимдазол
DCC- Дициклогсксилкарбодимид
EDDQ - 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин
DIC - диизопропилкарбодиимид
EDC - 1-этил-3-(3'-диметиламино)карбодиимида
DHU – дициклогексилмочевина
PNP - n-нитрофенол
PFP - пентафторофенол
Bt - бензотриазольные эфиры
DSC - N,N`-дисукцинимидил карбонат
l. Введение
Амидная функция - общий признак маленьких или сложных синтетических или естественных молекул. Например, повсюду в жизни белки играют решающую роль в фактически всех биологических процессах, таких как ферментативный катализ (почти все известные ферменты - белки), транспорт/хранение (гемоглобин), иммунная защита (антитела) и механическая поддержка (коллаген). Амиды также играют ключевую роль для фармацевтов. Глубокий анализ Всеобщей Базы Данных Медицинской Химии показал, что карбоксамидная группа появляется в больше чем 25 % известных лекарств.1 Этого следовало ожидать, так как карбоксамиды нейтральны, устойчивы и имеют свойства как предоставлять водород при образовании водородной связи, так и акцептировать его.
В природе синтез белка, включающий последовательность реакций пептидной конденсации (формирование амидной связи между двумя α-аминокислотами или пептидами), очень сложен, вероятно, чтобы сохранять уникальную и точно определенную последовательность аминокислот каждого белка. Этот барьер преодолен в естественных условиях селективным процессом активации, катализируемым ферментами, где необходимая аминокислота преобразована в промежуточный аминоэфир. Это промежуточное соединение далее вовлечено в процесс, опосредованный скоординированным взаимодействием больше чем ста макромолекул, включая mRNAs, tRNAs, активизирующие ферменты и белковые факторы, в дополнение к рибосомам.2
Формирование амидной или эфирной связи между кислотой и, соответственно, амином или спиртом формально являются конденсациями. Обычные этерификации - равновесные реакции, тогда как при смешивании амина с карбоновой кислотой сначала происходит кислотно-щелочная реакция, в результате которой образуется устойчивая соль. Другими словами, образование амидной связи должно преодолевать неблагоприятное термодинамическое равновесие, показанное на Схеме 1 и протекать в сторону гидролиза, а не синтеза.3
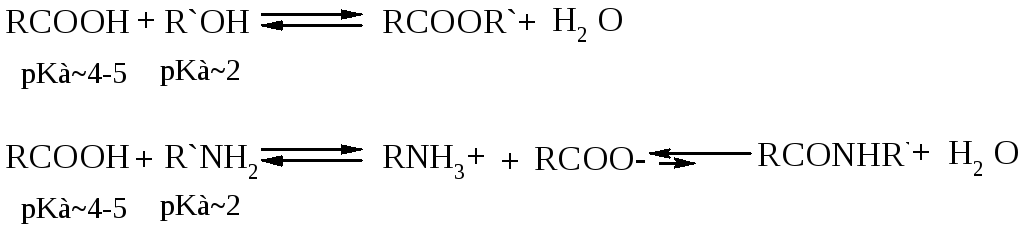
Схема 1. Сравнение образования эфирной и амидной связи.
Прямая конденсация соли может быть достигнута при высокой температуре (160°С),4 что совершенно несовместимо с присутствием других функциональных групп (см. также часть 2.6.3). Поэтому, необходима активация кислоты путем присоединения уходящей группы к ацильному углероду кислоты для того, чтобы стала возможной атака аминогруппой (Схема 2).
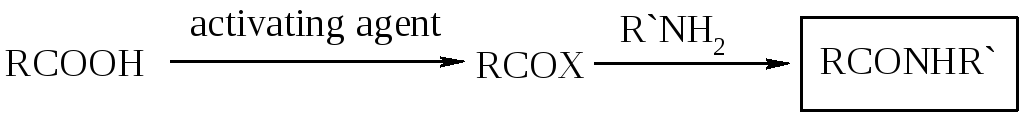
Схема 2. Активация кислоты и этапы аминолиза.
Следовательно, было развито множество методов и стратегий, и они теперь доступны для химика-синтетика. медицинского химика или комбинаторного химика. Соответствующие примеры этих методов приведены и этом обзоре. Химик, возможно, должен просмотреть множество таких условий чтобы найти метод, лучше всего подходящий его ситуации. Например, из-за плохой реакционноспособности или стерических ограничений в некоторых крайних случаев. Задача состоит в том, чтобы сформировать амид вообще. И других ситуациях химик будет требовать такую реакцию, которая позволит избежать рацемизации. В общем, цель состоит также в оптимизации выхода, уменьшении количества побочных продуктов, улучшении селективности, облегчении заключительной очистки, обнаружении масштабируемого процесса или использовании более экономичных реактивов. В прошедшие два десятилетия комбинированное быстрое развитие твердофазных технологии и методов конденсации позволило параллельному синтезу стать наилучшим инструментом для получения больших количеств разнообразных соединений для раннего исследования в фармацевтической промышленности.
