
- •Тема: окислительно-восстановительные реакции (овр)
- •Интегрированные ключевые умения (выносятся на экзамен)
- •Задания для подготовки к занятиям
- •Обучающие задачи
- •1 Определить степень окисления в молекулах и частицах MnO2; k2MnO4; MnO4–; Mn2o3.
- •2. Определить роли в окислительно-восстановительных реакциях веществ: PbO2, h2o2, hno3, h2so3, h2Se.
- •3. Определить эквиваленты веществ в следующих процессах:
- •1 Моль MnO4–присоединяет 3ē
- •2Моль I-освобождает 2 мольē
- •4. Закончить уравнение реакций
- •Задания для самостоятельной домашней работы
- •Проверьте свои знания и умения
Методические указания к занятию
По дисциплине «Неорганическая химия»
для студентов 1 курса, специальность 1-33 01 01-01 Биоэкология. Общая экология
Тема: окислительно-восстановительные реакции (овр)
После изучения темы студент должен знать:
Определение понятия «степень окисления», в чем отличие его от понятий «валентность», «заряд иона», «эффективный заряд»?
Какие процессы называются окислением и восстановлением?
Какие вещества и частицы проявляют свойства окислителей и восстановителей?
Что называется эквивалентом окислителя или восстановителя.
Что называется электродным потенциалом? Какова связь энергии Гиббса и электродного потенциала.
Как электродный потенциал зависит от концентрации, рН, комплексообразования, произведения растворимости? Уравнение Нернста.
В чем сущность электролиза растворов и расплавов солей и щелочей ?
Принцип работы гальванических элементов.
Уметь:
прогнозировать на качественном уровне продукты ОВ реакции (выносится на экзамен);
подбирать коэффициенты ОВР методом электронного баланса и ионно-электронным методом;
вычислять реальные потенциалы, используя таблицу стандартных потенциалов и уравнение Нернста;
определять направление окислительно-восстановительных реакций по электродвижущей силе реакции, пользуясь таблицами электродных потенциалов
Составлять схемы электролиза растворов и расплавов веществ
Составлять схемы работы гальванических элементов.
Интегрированные ключевые умения (выносятся на экзамен)
Прогнозирование на качественном уровне продукты ОВ реакции;
Определение направления окислительно-восстановительных реакций по изменению ЭДС.
Составление уравнений ОВР с подбором коэффициентов ионно-электронным методом
Составление схем электролиза и расчет по ним.
Задания для подготовки к занятиям
Выучить наизусть определение понятий (знания 1-6).
Разобраться и потренироваться в умениях (умения 1-6). Использовать для этого домашнее задание.
Подготовиться к выполнению лабораторного эксперимента, оформить опыты по примеру. Таблица.
Таблица. Пример оформления опытов по изучению химических свойств веществ
-
№ п/п
Название. Ход работы.
Т.Б
Результат
Объяснение. Уравнения реакции. Выводы.
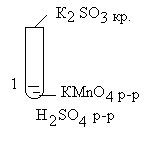
КМnO4
окислитнль-ожоговое действие
Обес
цве
чива
ние
2КМnO4+5К2SO3+3H2SO4=6K2SO4+2МnSO4+ 3H2O
Вывод: Продукты в ОВР зависят от реакции среды
Обучающие задачи
1 Определить степень окисления в молекулах и частицах MnO2; k2MnO4; MnO4–; Mn2o3.
Решение
MnO2: В молекулах суммарный заряд степеней окисления д.б. равен нулю, суммарная степень окисления двух атомов кислорода равна 2•(-2) = -4; поэтому марганец должен иметь степень окисления +4.
K2MnO4: Суммарная степень окисления четырех атомов кислорода 4•(-2) = -8, поэтому вся остаточная часть должна иметь суммарную степень окисления +8, т.к. два атома калия имеют суммарную степень окисления +2, то на марганец остается +8 – 2 = +6, т.е.Mn+6, или алгебраически:
+2 + х + (-8) = 0; х = +6, или:
(-2) • 4 = (8); – 8 => +8; 8 – 2 = 6; 6 1 = (+6)
MnO4–: Суммарная степень окисления иона равна его заряду, поэтому, обозначив степень окисления марганца за «Х», имеем:
–1 = х + (4•(-2); -1 = х – 8; х = +7
Формальная степень окисления марганца здесь +3; однако, такая степень окисления не характерна для него, поэтому следует подумать о том, что это сложный оксид
MnOMnO2где степень окисления соответственно +2 и +4.
Составить окислительно-восстановительный ряд хлора, определить роль хлора с различной степенью окисления в ОВР.
Решение
Электронная конфигурация валентного слоя хлора 3s23p53d0;
т.к. атом может принять один электрон, то минимальная степень окисления Cl–1, при возбуждении получается 1, 3, 5, 7 неспаренных электронов, которые атом может отдать, поэтому степень окисления может бытьCl+1,Cl+3,Cl+5,Cl+7. Окислительно-восстановительный ряд хлора:
Cl-1,Cl20,Cl+1,Cl+3,Cl+5,Cl+7,
т.к. Cl-1может только повышать степень окисления, тоCl-является тольковосстановителем (подчеркнутая буква «в»- мнемоническое правило для запоминания).Cl+7может только уменьшать степень окисления, поэтому он проявляет только окислительные свойства. Остальные атомы хлора проявляют и окислительные и восстановительные свойства.
