
Методичка по общей химии
.pdfФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ
РАЗВИТИЮ
ГОСУДАРСТВЕННОЕ УНИТАРНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«КАЗАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
КАФЕДРА ОБЩЕЙ И ОРГАНИЧЕСКОЙ ХИМИИ
РУКОВОДСТВО
К ЛАБОРАТОРНО-ПРАКТИЧЕСКИМ ЗАНЯТИЯМ
ПО ОБЩЕЙ ХИМИИ
(часть I)
КАЗАНЬ 2005
ББК 24я73
К 24
Печатается по решению Центрального координационно- методичес-кого совета Казанского государственного медицинского университета
Составители:
ст.преподаватель кафедры общей и органической химии
Галеева С.И., доцент кафедры общей и органической химии
Ситдиков И.Б.,
доцент кафедры общей и органической химии Хисамеев Г. Г.,
ст.преподаватель кафедры общей и органической химии
Сагдеев К.А.
Под редакцией д.х.н. Никитиной Л.Е.
Рецензенты:
доцент кафедры Технологии неорганических веществ КГТУ
Порфирьева Р.Т.,
доцент кафедры общей химии КГАСУ Бойчук В.А.
Руководство к лабораторно-практическим занятиям по общей химии (часть I)/ Галеева С.И., Ситдиков И.Б., Хисамеев
Г.Г., Сагдеев К.А. Под ред. Никитиной Л.Е. − Казань: КГМУ, 2005. − 98 с.
Учебное пособие составлено в соответствии с Государственным образовательным стандартом высшего и профессионального обра-зования и программой преподавания общей химии. В пособии при-ведены краткое изложение
теоретического материала, примеры реше-ния задач, вопросы
и |
задачи для самоподготовки, описание |
лабо-раторных работ |
и |
контрольно-измерительные материалы |
в виде тестов по |
различным темам.
Предназначено для студентов I курса лечебного, педиатрического, стоматологического и медикопрофилактического факультетов КГМУ.
© Казанский государственный медицинский университет, 2005
РУКОВОДСТВО
К ЛАБОРАТОРНО-ПРАКТИЧЕСКИМ ЗАНЯТИЯМ ПО ОБЩЕЙ ХИМИИ
(ЧАСТЬ I)
(учебное пособие по общей химии
для студентов I курса медицинских факультетов КГМУ)
Под редакцией Никитиной Л.Е.
Составители: Галеева Сююмбика Исмагиловна Ситдиков Ильдар
Бариевич
Хисамеев Галим
Гильмутдинович
Сагдеев Камиль
Абрарович
Редактор издания: Шакирзянов Р.А.
Компьюторная вёрстка Хисамеева Г.Г.
98
Приложение
Таблица 8
Множители и приставки для образования десятичных кратных и дольных и их наименований
Мно- |
Прис- |
Обозначение |
Мно- |
Прис- |
Обозначение |
||||
жи- |
тавка |
|
|
жи- |
тавка |
|
|
||
Русс- |
Между- |
Русс- |
Между- |
||||||
тель |
|
кое |
народно |
тель |
|
кое |
народно |
||
|
|
|
е |
|
|
|
|
е |
|
|
|
|
|
|
|
|
|
||
1012 |
тера- |
Т |
T |
10−1 |
деци- |
g |
D |
||
|
|
|
|
− |
2 |
|
|
|
|
109 |
гига- |
Г |
G |
10− |
санти |
с |
c |
||
3 |
|||||||||
6 |
мега- |
М |
M |
10 |
- |
м |
m |
||
10 |
10−6 |
||||||||
3 |
кило- |
к |
k |
10−9 |
милли |
мк |
µ |
||
10 |
- |
n |
|||||||
102 |
гекто |
г |
h |
− |
12 |
н |
|||
10 |
- |
да |
da |
10 |
микро |
п |
p |
||
|
дека- |
|
|
|
|
- |
|
|
|
|
|
|
|
|
|
нано- |
|
|
|
|
|
|
|
|
|
пико- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЛИТЕРАТУРА |
1. |
Глинка Н.Л. Общая химия. − Л.: Химия, 1986. − 703 с. |
2. |
Глинка Н.Л. Задачи и упражнения по общей химии. − Л.: |
Химия, 1983. − 264 с.
3.Ленский А.С. Введение в бионеорганическую и биофизическую химию. − М.: Высш.шк., 1989. − 256 с.
4.Пузаков С.А. Химия. − М.: Медицина, 1995. − 624 с.
5.Ахметов Н.С. Общая и неорганическая химия. − М.:
Высш.шк., 1981. − 679 с.
6. Романцева Л.М., Лещинская З.Л., Суханова В.А. Сборник задач и упражнений по общей химии. − М.: Высш.шк., 1991. − 288 с.
ОГЛАВЛЕНИЕ
Занятие 1. Тема: Способы выражения концентрации растворов..….....4
Задачи с решениями……………………………………………………..….…7
Вопросы и задачи для самоподготовки…………………………………...13
Лабораторная работа……………………………...…………………………..15
Занятие 2. Тема: Растворы сильных и слабых
электролитов……....…16
Задачи с решениями…………………………………………………………18
Вопросы и задачи для самоподготовки…………………………………...20
Занятие 3. Тема: Автопротолиз воды. Ионное произведение
воды.
Водородный и гидроксильный показатели. Гидролиз солей………..23
Задачи с решениями………………………………………………………….25
Вопросы и задачи для самоподготовки……………………………….….27
Занятие 4. Тема: Буферные растворы. Гетерогенное
равновесие.……30 Буферные
растворы…………………………………………………………...30
Задачи с решениями………………………………………………………….31
Вопросы и задачи для самоподготовки……………………………….….33
Гетерогенное
равновесие………………………………………………….....34 |
с |
||
Задачи |
|
|
|
решениями………………………………………………………….35 |
для |
||
Вопросы |
и |
задачи |
|
самоподготовки……………………………….….36
Лабораторные работы……………………………..………………………….38
Занятие 5. Тема: Коллигативные свойства растворов
неэлектро-
литов………………………………………………………………………………..40
Задачи с решениями………………………………………………………….42
Вопросы и задачи для самоподготовки……………………………….….46
Занятие 6. Тема: Обобщение знаний по объёмному анализу.
Контрольная работа по разделам «Учение о растворах», «Объёмный анализ». Образец билета контрольной работы……………………………….....52
Занятие 7. Тема: Элементы химической термодинамики и
биоэнергетики.
Термохимия.…………………………………………………52
Задачи с решениями………………………………………………………….55
Вопросы и задачи для самоподготовки……………………………….….57
Занятие 8. Тема: Химическая кинетика и
катализ.…………………….62
Задачи с решениями………………………………………………………….64
Вопросы и задачи для самоподготовки……………………………….….67
Лабораторные |
|
|
|
работы……………..………………………………………….70 |
Химическое |
||
Занятие |
9. |
Тема: |
|
равновесие.………………..……………….73 |
с |
||
Задачи |
|
|
|
решениями………………………………………………………….75 |
для |
||
Вопросы |
и |
задачи |
|
самоподготовки……………………………….….78
Лабораторные работы………………………………………………..……….83
Экзаменационные вопросы…………………………………..………..……….85
Приложение………………………………………………..…………..……….91
Литература……………………………………………………………..……….98
4
ЗАНЯТИЕ 1
Тема: Способы выражения концентрации растворов.
Под концентрацией раствора понимают содержание
растворённо-го вещества (в г или моль) в единице массы
или объёма раствора или растворителя.
Различают приближённые и точные способы. К
приближённым относятся понятия разбавленный,
концентрированный, ненасыщен-ный, насыщенный и
пересыщенный растворы. К точным способам выражения концентрации относятся:
0. Массовая доля растворённого вещества ω(Х)
представляет собой
отношение массы растворённого вещества (m(X)) к массе
раствора |
(m(p-p)); |
это безразмерная величина, выражаемая |
в долях |
единицы, |
в сотых долях или процентах (%), в |

тысячных долях или промилле (%о), в миллионных долях или
вмлн−1. Например, ω(Х) = 0,005 = 0,5% = 5 %о = 5000 млн−1.
Вмедицинской литературе массовую долю принято выражать в грамм-процентах (г%) (равнозначно процентам),
миллиграмм-процен-тах (мг% или 10−3 г%) и в микрограмм-
процентах (мкг%или 10−6 г%). Таким образом, ω(Х) = 0,005 = 0,5% = 0,5 г% = 500 мг% = 500000 мкг%. Например, 5%-ный раствор − это пятипроцентный раствор или раствор с массовой долей растворённого вещества, рав-ной 5% или
0,05.
2. Молярная доля χ(X) представляет собой отношение количества вещества компонента раствора ν(Xi) к общему количеству всех ком-понентов Σν(Xi), составляющих раствор.
Это безразмерная величина, выражаемая в долях единицы или процентах.
3. Объёмная доля ϕ(X) представляет собой отношение объёма компо-
нента раствора (жидкости) V(X) к общему объёму раствора
(смеси жидкостей) V(р-р). И эта безразмерная величина может выражаться как в долях единицы, так и в процентах.
97
Приложение Таблица 7
Таблица логарифмов для вычисления рН
Числа |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
1 |
00 |
04 |
07 |
11 |
146 |
176 |
20 |
230 |
25 |
27 |
|
0 |
1 |
9 |
4 |
|
|
4 |
|
5 |
9 |
|
|
|
|
|
|
|
|
|
|
|
2 |
30 |
32 |
34 |
36 |
380 |
398 |
41 |
431 |
44 |
46 |
|
1 |
2 |
2 |
2 |
|
|
5 |
|
7 |
2 |
|
|
|
|
|
|
|
|
|
|
|
3 |
47 |
49 |
50 |
51 |
532 |
544 |
55 |
568 |
58 |
59 |
|
7 |
1 |
5 |
9 |
|
|
6 |
|
0 |
1 |
4 |
|
|
|
|
|
|
|
|
|
|
60 |
61 |
62 |
63 |
644 |
653 |
66 |
672 |
68 |
69 |
|
|
2 |
3 |
3 |
4 |
|
|
3 |
|
1 |
0 |
5 |
|
|
|
|
|
|
|
|
|
|
69 |
70 |
71 |
72 |
732 |
740 |
74 |
756 |
76 |
77 |
|
|
9 |
8 |
6 |
4 |
|
|
8 |
|
3 |
1 |
6 |
|
|
|
|
|
|
|
|
|
|
77 |
78 |
79 |
79 |
806 |
813 |
82 |
826 |
83 |
83 |
|
|
8 |
5 |
2 |
9 |
|
|
0 |
|
3 |
9 |
7 |
|
|
|
|
|
|
|
|
|
|
84 |
85 |
85 |
86 |
869 |
875 |
88 |
887 |
89 |
89 |
|
|
5 |
1 |
7 |
3 |
|
|
1 |
|
2 |
8 |
8 |
|
|
|
|
|
|
|
|
|
|
90 |
90 |
91 |
91 |
924 |
929 |
93 |
940 |
94 |
94 |
|
|
3 |
9 |
4 |
9 |
|
|
5 |
|
5 |
9 |
9 |
|
|
|
|
|
|
|
|
|
|
95 |
95 |
96 |
96 |
973 |
978 |
98 |
987 |
99 |
99 |
|
|
4 |
9 |
4 |
8 |
|
|
2 |
|
1 |
6 |
|
|
|
|
|
|
|
|
|
|
|
Примеры расчета рН по величинам [H+]:
[H+] = |
5,3.10−1 |
моль/л; рН = −lg[H+] = −lg 5,3.10−1 |
= − |
(0,724 − 1) = −(−0,276) ≈ 0,28; |
|
||
[H+] = |
5,3.10−4 |
моль/л; рН = −lg[H+] = −lg5,3.10−4 = |
−(0,724 − |
4) = −(−3,276) ≈ 3,28; |
|
||
Примеры расчета [H+] по величинам рH:
рН = 0,42; [H+] = antilg(−рН) = antilg (−0,42) = antilg (0,580 − 1) = 3,8.10−1 моль/л;
рН = 3,42; [H+] = antilg(−рН) = antilg (−3,42) = antilg (0,580 − 4) = 3,8.10−4 моль/л.

96
Таблица 6.
Константы нестойкости комплексных ионов в водных
растворах.
Схема диссоциации
Al(OH)3 |
|
|
Al3+ + 6OH- |
|||
[Ag(NH3 )2 ]+ |
|
|
Ag+ + 2NH3 |
|||
|
- |
|
Ag |
+ |
|
- |
[Ag(NO2)2] |
|
|
+ 2NO2 |
|||
|
2− |
|
Ag |
+ |
2- |
|
[Ag(S2O3)] |
|
|
+2S2O3 |
|||
[Ag(CN)2]- |
Ag+ +2CN- |
|||||
[AgCl2]- |
Ag+ +2Cl- |
|
||||
[AgBr2]- |
Ag+ +2Br- |
|||||
[AgEn]+ |
Ag+ +En |
|
|
|||
[AgEDTA]3- |
|
Ag+ +EDTA4- |
||||
[Au(CN)2]- |
Au+ +2CN- |
|||||
[HgCl4 ]2- |
|
Hg2+ + 4Cl- |
||||
[HgBr4]2- |
Hg2+ + 4Br- |
|||||
[HgI4 ]2+ |
|
|
Hg2+ + 4I- |
|||
[Hg(CN)4 |
]2+ |
|
Hg2+ + 4CN- |
|||
[Hg(NH3)4]2+ |
Hg2+ + 4NH3 |
|||||
[CdI4]2- |
Cd2+ + 4I- |
|||||
[CdBr4]2- |
|
Cd2- + 4Br- |
||||
[Cd(OH)4 |
]2- |
|
Cd2+ + 4OH- |
|||
[Cd(NH3)4]2+ |
|
Cd2+ + 4NH3 |
||||
[Cd(CN)4]2- |
|
Cd2+ + 4CN- |
||||
[Cd(En)2]2+ |
|
Cd2+ + 2En |
||||
Кн |
|
|
Схема диссоциации |
|
|
|
Кн |
||||||||||||||||||
1.10 |
− |
33 |
|
[Cu(CN)4 |
]2+ |
Cu2+ + 4CN- |
|
9,6.10− |
|||||||||||||||||
|
|
|
[Cu(OH)4]2- |
Cu2+ + 4OH- |
|
29 |
|||||||||||||||||||
9,3.10 |
− |
|
−19 |
||||||||||||||||||||||
|
[Cu(En)2]2+ |
Cu2+ + 2En |
|
|
|
||||||||||||||||||||
8 |
|
|
|
|
|
|
|
|
|
3,2.10 |
|||||||||||||||
|
. |
10 |
− |
[CuEDTA]2- |
Cu2+ + EDTA4- |
7,4.10−21 |
|||||||||||||||||||
1,8 |
|
|
|
|
|
|
|
|
|
]2- |
Cu2+ + 4SCN- |
|
|||||||||||||
3 |
|
|
|
|
|
|
[Cu(SCN)4 |
1,6.10−19 |
|||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
2,5 |
. |
|
|
|
− |
[CaEDTA]2- |
Ca2+ + EDTA4- |
3.10−7 |
|||||||||||||||||
|
10 |
|
|
|
|
|
|
|
]2+ |
Co2+ + 4NH3 |
2,6.10−11 |
||||||||||||||
14 |
|
|
|
|
|
|
[Co(NH3)4 |
||||||||||||||||||
8.10−22 |
|
[Co(En)2]2+ |
Co2+ + 2En |
|
|
|
−6 |
||||||||||||||||||
|
|
4- |
2,8.10−11 |
||||||||||||||||||||||
1,76 |
. |
10 |
|
|
|
|
2- |
Co |
2+ |
+ EDTA |
2,2.10 |
||||||||||||||
|
|
|
[CoEDTA] |
|
|
|
|
|
|
|
|
7,9.10−14 |
|||||||||||||
−5 |
|
|
|
|
|
|
[Co(CN)4 |
]2+ |
Co2+ + 4CN- |
|
|||||||||||||||
7,8.10− |
[Co(SCN)4]2- |
Co2+ + 4SCN- |
|
8,1.10−20 |
|||||||||||||||||||||
8 |
|
|
|
|
|
|
[Fe(CN)6]4- |
Fe2+ + 6CN- |
|
|
6,3.10−3 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2.10−5 |
|
[Fe(CN)6 |
3- |
Fe |
3+ |
+ 6CN |
- |
1.10−24 |
|||||||||||||||||
4,8.10−8 |
] |
|
|
|
|
|
|
1.10−31 |
|||||||||||||||||
[Fe(OH)6 |
3- |
Fe |
3+ |
|
+ 6OH |
- |
|||||||||||||||||||
5.10−39 |
|
] |
|
|
|
|
|
|
2,8.10−9 |
||||||||||||||||
|
[Fe(SCN) |
|
|
3- |
3+ |
+ 6SCN |
- |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
] |
Fe |
|
|
|
|
|
|
|
|
||||||||
8,5.10−1 |
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
5,9.10−4 |
|||||||
[Ni(NH3)4]2+ |
Ni2+ + 4NH3 |
|
|||||||||||||||||||||||
6 |
|
|
|
|
|
|
[Ni(CN)4]2+ |
Ni2+ + 4CN- |
|
1,1.10−8 |
|||||||||||||||
1.10−21 |
|
|
|||||||||||||||||||||||
|
[PtCl |
4 |
]2- |
|
|
Pt2+ + 4Cl- |
|
|
|
1,8.10−14 |
|||||||||||||||
1,5.10−3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1.10−16 |
|||||||
[PtBr4 ] |
2- |
|
|
Pt |
2+ |
+ 4Br |
- |
|
|
|
|||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3.10−21 |
||||||||||
|
|
|
−42 |
|
[Zn(NH3)4 |
2+ |
Zn |
2+ |
+ 4NH3 |
||||||||||||||||
|
|
|
|
] |
|
|
|
3,5.10−10 |
|||||||||||||||||
4.10 |
|
−2 |
[Zn(CN)4 |
2+ |
Zn |
2+ |
+ 4CN |
- |
|
||||||||||||||||
|
|
|
|
|
] |
|
|
|
|
|
|
|
|
1,3.10−17 |
|||||||||||
5,3.10 |
|
[Zn(OH)4 |
2+ |
Zn |
2+ |
+ 4OH |
- |
|
|||||||||||||||||
|
|
|
|
|
|
|
] |
|
|
|
|
|
|
|
|
|
|||||||||
[CdEDTA]2- |
Cd2+ + EDTA4- |
0 |
[Zn(SCN)4 |
]2- Zn2+ + 4SCN- |
3,6.10−16 |
[Cu(NH3)4]2+ |
Cu2+ + 4NH3 |
8.10−7 |
|
|
2.10−4 |
|
|
2.10−4 |
|
|
|
|
|
2,5.10−9 |
|
|
|
|
|
7,6.10−8 |
|
|
|
|
|
1,4.10−1 |
|
|
|
|
|
9 |
|
|
|
|
|
6.10−11 |
|
|
|
|
|
3,3.10−1 |
|
|
|
|
|
7 |
|
|
|
|
|
2,1.10−1 |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
5
4. Молярная концентрация С(Х) представляет собой отношение коли-чества вещества компонента раствора ν(X) к
объёму раствора V(р-р); размерность − моль/л. Например, 0,1 М раствор означает децимоляр-ный раствор или раствор с молярной концентрацией растворённого вещества, равной
0,1 моль/л.
5. Молярная концентрация эквивалента (или нормальная
концентра-ция) C |
|
1 |
X |
|
представляет собой отношение |
|
|
|
|||||
Z |

количества вещества экви-валента в растворе ν( Z1 X ) к
объёму раствора; размерность − моль/л.
Понятие «эквивалент вещества» связано с конкретной
реакцией, в которой вещество участвует. Эквивалент ( Z1 X )
− это условная или реальная частица вещества Х, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или одному электрону − в данной окислительно-
восстановительной реакции. Эквивалент од-ноосновной кислоты или однокислотного основания − это всегда
реальная частица, молекула Х. В случае многоосновных кислот и многокислотных оснований эквивалентом может быть
реальная молекула Х или её какая-то часть (доля) − Z1 X .
Число, показываю-щее долю реальной частицы, эквивалентной одному иону водорода в реакциях кислотно-основного типа или одному электрону − в окис-лительно-восстановительных реакциях, называется фактором экви-валентности (fэкв.(Х)
или Z1 X ).
Примеры определения эквивалентов различных веществ в различ-ных реакциях приведены в таблицах 1 и 2
Приложения.
Если в химической реакции участвуют два вещества Х1 и Х2, то по закону эквивалентов количество эквивалента одного
вещества ν( Z1 X 1) равно количеству эквивалента второго вещества ν( Z1 X 2), т.е.:
6
ν( Z1 X 1) = ν( Z1 X 2).
Если кислотно-основная реакция протекает до конца,
то при на-хождении фактора эквивалентности кислот,
оснований и солей сле-дует учесть, что Z − это основность кислоты или кислотность основа-ния, а в случае солей − произведение числа атомов металла, обра-зующего соль, на его валентность.
Один моль эквивалентов вещества Х содержит число Авогадро частиц (6,02.1023 эквивалентов Х). Молярная масса
вещества |
|
|
эквива-лента |
1 |
X |
определяется |
произведением |
||||
Z |
|||||||||||
фактора |
|
эквивалентности |
|
на |
молярную массу |
вещества: |
|||||
М( |
1 |
X ) = |
|
1 |
M(X) . |
|
|
|
|
|
|
Z |
Z |
|
иной |
нормальной |
концентрацией |
||||||
|
|
Растворы с той или |
|
||||||||
С( |
1 |
X ) |
рас-творённого вещества |
используются |
для вполне |
||||||
Z |
|||||||||||
конкретных реакций. Например, 0,01 н раствор или
сантинормальный раствор, раствор с нормальной
концентрацией растворённого вещества, равной 0,01 моль/л; 0,001 N раствор или миллинормальный раствор.
6. Моляльность (моляльная концентрация) раствора в(Х)
представ-ляет собой отношение коли-чества растворённого вещества ν(X) к массе растворителя m(р-тель); размерность
− моль/кг.
− допускаются следующие обозначения: нормальной концентрации N(Х) вместо С( Z1 X ), моляльной концентрации
Сm(Х) вместо в(Х).
7. Титр (или массовая концентрация) t(X) представляет собой отно-шение массы растворённого вещества к объёму раствора; размер-ность − г/мл.
Формулы, позволяющие производить расчёт массовых,
объёмных и молярных долей, титра, а также различных видов концентраций раствора приведены в таблице 3 Приложения.
По закону эквивалентов, если взаимодействуют растворы двух веществ V(p-p X1) и V(p-p X2) с нормальной
концентрацией |
|
|
1 |
|
и |
|
C |
|
X1 |
||||
Z |
95
Приложение
Таблица 5.
Произведение растворимости (ПР) некоторых малорастворимых веществ (250С, − 18÷200С)
Вещество |
|
|
ПР |
Вещество |
|
ПР |
|
Вещество |
|
ПР |
|
|||||||||
AgBr |
7,7.10−13 |
Cr(OH)3 |
1.10−30 |
NiS |
|
1,4.10−24 |
||||||||||||||
AgCN |
2,0.10−12 |
CuBr |
|
5,3.10−9 |
|
7,4.10−6 |
||||||||||||||
Ag2CO3 |
6,2.10−12 |
CuCO3 |
|
1,4.10−10 |
PbBr2 |
1,5.10−13 |
||||||||||||||
1,6.10−10 |
|
1,8.10−7 |
PbCO3 |
1,7.10−5 |
||||||||||||||||
AgCl |
1.10−16 |
CuCl |
|
1,1.10−12 |
PbCl2 |
1,8.10−14 |
||||||||||||||
AgI |
1.10−13 |
CuI |
|
|
5,6.10−20 |
PbCrO4 |
3,7.10−8 |
|||||||||||||
AgSCN |
2.10−8 |
Cu(OH)2 |
2,5.10−50 |
PbF2 |
8,7.10−9 |
|||||||||||||||
AgOH |
1,8.10−18 |
Cu2S |
|
4.10−38 |
PbI2 |
2.10−16 |
|
|||||||||||||
Ag3PO4 |
1.10−51 |
CuS |
|
|
1,7.10−34 |
Pb(OH)2 |
1.10−29 |
|
||||||||||||
Ag2S |
7,7.10−5 |
(CuOH)2CO3 |
2,5.10−11 |
PbS |
|
2.10−8 |
|
|
||||||||||||
Ag2SO4 |
4.10−12 |
FeCO3 |
|
4,8.10−16 |
PbSO4 |
1.10−24 |
|
|||||||||||||
Ag2CrO4 |
1,9.10−33 |
Fe(OH)2 |
4.10−38 |
Pd(OH)2 |
3.10−41 |
|
||||||||||||||
Al(OH)3 |
8.10−9 |
Fe(OH)3 |
4.10−19 |
PtBr4 |
8.10−29 |
|
||||||||||||||
BaCO3 |
1,7.10−7 |
FeS |
|
|
3.10−35 |
PtCl4 |
8.10−43 |
|
||||||||||||
BaC2O4 |
2,3.10−10 |
GeS |
|
|
5.10−23 |
PtS |
|
4.10−42 |
|
|||||||||||
BaCrO4 |
1,7.10−6 |
Hg2Br2 |
|
9.10−17 |
Sb(OH)2 |
1,6.10−93 |
||||||||||||||
1,1.10−10 |
Hg2CO3 |
|
2.10−18 |
Sb2S3 |
5.10−26 |
|
||||||||||||||
BaF2 |
6,03.10−39 |
Hg2Cl2 |
|
4.10−29 |
1.10−56 |
|
||||||||||||||
BaSO4 |
. |
|
|
−7 |
Hg2I2 |
|
. |
|
−45 |
Sn(OH)2 |
. |
|
−28 |
|
||||||
Ba3(PO4)2 |
8 10 |
− |
|
1 |
10−58 |
Sn(OH)4 |
1 |
10−9 |
|
|
||||||||||
1,6.10 5 |
Hg2S |
|
4.10−5 |
|
SnS |
|
1.10 |
|
−8 |
|||||||||||
BaSO3 |
6,3.10−22 |
HgS |
|
|
5.10− |
|
|
SrCO3 |
5,6.10− |
|
||||||||||
BaS2O3 |
4,3 |
. |
|
−31 |
|
6 |
1.10 |
|
20 |
3,4.10 |
|
9 |
||||||||
Be(OH)2 |
. |
10 |
2 |
PtCl |
1,7.10 |
−3 |
|
|
2,8.10 |
−7 |
||||||||||
1,6 |
|
−72 |
K |
|
|
SrC2O4 |
|
|
||||||||||||
Bi(OH)3 |
|
10 |
La(OH)3 |
1. |
10 |
−5 |
|
SrF2 |
1. |
10 |
−50 |
|
||||||||
Bi2S3 |
4,8.10−9 |
Li2CO3 |
|
|
|
|
|
SrSO4 |
|
|
|
|
||||||||
CaCO3 |
2,6.10−9 |
MgCO3 |
|
6.10−9 |
Th(OH)4 |
1.10−40 |
|||||||||||
CaC2O4 |
4.10−11 |
MgF2 |
|
8,6.10−5 |
Ti(OH)3 |
4.10−6 |
|
||||||||||
CaF2 |
3,1.10−5 |
|
|
2,5.10−13 |
TlBr |
2.10−4 |
|
||||||||||
6,1.10−5 |
MgC2O4 |
|
1.10−13 |
1.10−44 |
|||||||||||||
Ca(OH)2 |
1.10 |
− |
29 |
MgNH4PO4 |
|
5.10 |
−12 |
TlCl |
4.10 |
−3 |
|
||||||
CaSO4 |
|
Mg3(PO4)2 |
|
Tl(OH)3 |
|
|
|||||||||||
2,5.10−14 |
Mg(OH)2 |
1.10−10 |
5.10−21 |
||||||||||||||
Ca3(PO4)2 |
1,2.10−14 |
4.10−14 |
Tl2SO4 |
6.10−11 |
|||||||||||||
CdCO3 |
1.10−29 |
MnCO3 |
|
1,4. |
|
−15 |
Tl2S |
. |
|
−17 |
|||||||
Cd(OH)2 |
1. −12 |
Mn(OH)2 |
|
. |
10 |
ZnCO3 |
5 |
10 |
|
|
|||||||
|
|
|
−10 |
|
|
|
|||||||||||
CdS |
.10−16 |
MnS |
|
|
4,1 |
|
10 |
Zn(OH)2 |
. |
10 |
−26 |
||||||
CoCO3 |
2 10−27 |
|
|
1,4.10−7 |
ZnS |
|
8 |
|
−13 |
||||||||
2. |
10 |
|
|
Na3AlF6 |
|
|
|
−14 |
|
2,6.10 |
|||||||
Co(OH)2 |
|
|
|
NiCO3 |
|
7.10 |
(сфалерит |
|
|||||||||
CoS |
|
|
|
|
Ni(OH)2 |
|
|
|
|
) |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Zn(CN)2 |
|
|
|
|
|
|
|
|
|
|
|
94 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Приложение |
||||
Таблица 4.
Примеры определения фактора эквивалентности и молярной массы эквивалента в окислительно-восстановительных реакциях
|
Уравнение реакции |
|
Эквивален |
Фактор |
Молярная |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
т |
эквива |
|
масса |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
веществ |
- |
|
|
эквивалента |
|||||||||||||||||
|
|
|
|
|
|
|
а |
1 |
|
лент- |
||||||||||||||||||
|
|
|
|
|
|
|
Х, |
|
X |
ности |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
Z |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
I2 + 5Cl2 + 12KOH= 2KIO3 +10KCl + 6H2O |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
1 |
|
254 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
I2 |
|
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
10 |
|
||||||||
|
|
|
|
|
|
|
|
|
1 |
I2 |
|
|
|
|
|
|
|
|
|
|
|
|||||||
I2 + 5Cl2 + 12OH− = 2IO3− +10Cl−+6H2O |
|
|
|
|
|
|
|
= 25, 4г/моль |
|
|
|
|||||||||||||||||
|
10 |
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
− |
− |
− |
|
|
1 |
|
(одна |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
I2 + 12OH −10e = 2IO3 |
|
+ 6H2O |
|
|
1 |
|
|
M |
|
Cl2 |
= |
|
|
71 |
||||||||||||||
|
|
|
|
|
2 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
десятая |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
||||||
«Х» |
десять эквивалентов |
|
|
|
10 |
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
= 35, 5г/моль |
|
|
|
|||||||||||||||||||||
|
|
|
часть |
1 |
|
|
|
|
|
|||||||||||||||||||
|
− |
− |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Cl2 + 2e |
= 2Cl |
|
|
|
|
молекулы) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
«Х» |
два эквивалента |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Cr2(SO4)3 |
+ 3H2O2 + 10KOH = |
1 Cr (SO |
) |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
||||
3 |
|
|
|
M |
|
Cr (SO |
) |
|
= |
|||||||||||||
|
|
|
6 |
2 4 |
|
|
|
|
6 |
|||||||||||||
2K2CrO4 + K2SO4 + 8H2O |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
4 3 |
|
|
|||||
|
|
(одна |
|
|
|
|
|
|
1 |
392 = 65,33 г/моль |
||||||||||||
2Cr3+ + 3H2O2 +10OH− = 2CrO42- +4H2O |
|
|
|
|
|
|
|
6 |
||||||||||||||
|
шестая |
|
|
|
|
|
1 |
|
|
|
|
|
1 |
34 |
||||||||
|
|
|
|
|
часть |
|
|
|
|
|
M |
|
H |
O |
2 |
|
= |
|
||||
2Cr3+ +8OH−−6e− = 2CrO42- + 4H2O |
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
2 |
|
||||
|
молекулы) |
|
1 |
|
= 17 г/моль |
|
|
|
|
|||||||||||||
1 |
|
|
|
|
1 |
Н2О2 |
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
«Х» шесть эквивалентов |
|
(половина |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
− |
− |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
H2O2 + 2е |
= 2ОH |
|
молекулы) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
«Х» два эквивалента |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7
C Z1 X2 , cоответственно и титром t(X1) и t(X2) , то:
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|||
V(p-pX1) |
C |
|
|
X |
|
|
m(X1) |
V(p-pX1) t(X1) |
|
M( |
X ) |
|
|||||||||||||
|
|
|
|
||||||||||||||||||||||
Z |
1 |
|
; |
|
|
|
Z |
1 |
. |
||||||||||||||||
|
|
|
= |
|
|
|
|
|
|
= |
|
|
|
|
|
= |
|
|
|
|
|||||
V(p-p X |
2 |
) |
1 |
|
|
m(X |
2 |
) |
V(p-p X |
2 |
) t(X |
2 |
) |
M( |
|
1 |
X2 ) |
||||||||
|
|
|
C |
|
|
X2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Z |
|
|||||||||||
|
|
|
|
Z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Задачи с решениями.
Массовая доля компонента.
1. Глауберова соль Na2SO4.10H2O применяется при лечении желудоч-но-кишечных заболеваний как слабительное. Сколько
(г) Na2SO4.10H2O нужно для приготовления 250 г раствора, с
массовой долей Na2SO4, равной 5%.
Дано: Решение: m(p-p) = 250 г.
ω(Na2SO4) = 5% = 0,05 |
1) m(Na2SO4 |
= |
m(p-p)ω%(Na2SO4) |
= |
|||||
m(Na2SO4.10H2O) = ? |
|
|
|
100% |
|
|
|||
|
250.0,05 = 12,5 г; |
|
|||||||
M(Na2SO4) = 142 г/моль |
|
|
|||||||
2) по стехиометрической схеме: |
|||||||||
M(Na2SO4.10H2O)=322 |
|||||||||
г/моль |
|
Na2SO4 → Na2SO4.10H2O |
|
||||||
|
|
ν(Na2SO4) = ν(Na2SO4.10H2O) |
|||||||
|
|
m(Na2SO4) |
|
m(Na2SO4 10H2O) |
|
||||
|
|
|
= |
|
|
|
|
||
|
|
M(Na2SO4) |
|
M(Na2SO4 10H2O) |
|
||||
|
m(Na2SO4.10H2O) = 12,5.322/142 = |
||||||||
|
28,4 г. |
|
|
|
|
|
|||
|
Ответ: 28,4 г. |
|
|||||||
|
|
|
|
|
|
|
|
|
|
1.Сульфат цинка ZnSO4 применяется в виде раствора с массовой до-
лей, равной 0,25%, в качестве глазных капель. Сколько (г)
воды нужно добавить к 25 г раствора с массовой долей
ZnSO4, равной 2%, чтобы приготовить глазные капли?
|
|
|
|
|
|
8 |
|
|
|
|
|
|
Дано: |
|
|
Решение: |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
m(p-p) = 25 г |
|
|
В соответствии |
с |
«правилом |
креста» |
||||||
ω1(ZnSO4) = 2% |
|
|
составим |
схему: |
|
|
|
|
2% |
|||
ω2(ZnSO4) |
= |
0,25 |
|
|
|
|
|
|
|
|||
0,25% |
|
|
|
0,25% |
|
|
|
|
|
|
|
|
m(H2O) = ? |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
0% |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,75 |
|
|
|
|
|
|
|
||
|
|
|
|
|
m(2%p-p) |
= |
0,25 |
= |
1 |
= |
25 |
|
|
|
|
|
|
m(H2O) |
1,75 |
7 |
m(H2O) |
||||
|
|
|
|
|
|
|
|
|
||||
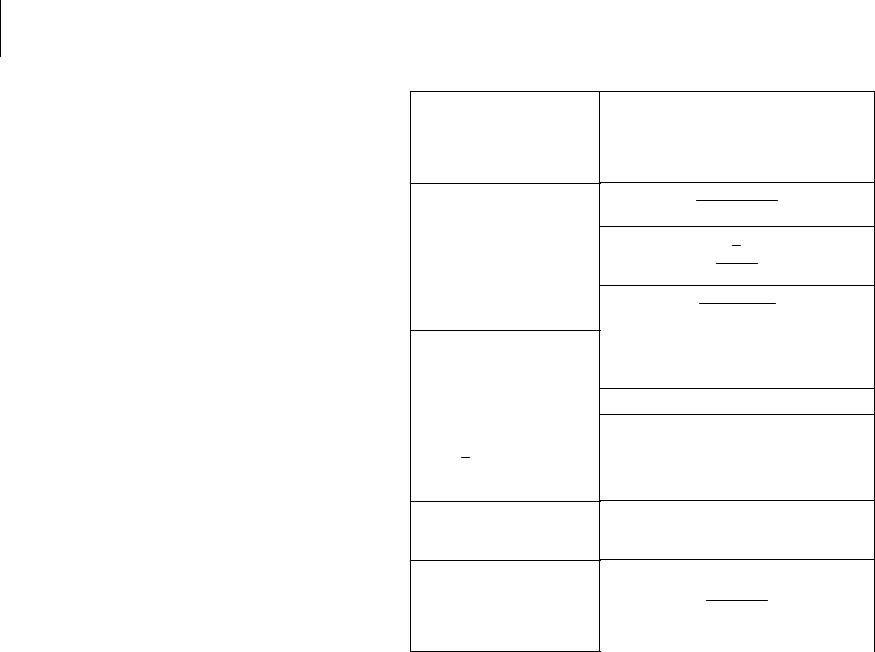
m(H2O) = 7 25 = 175 г.
Ответ: 175 г.
3. Для компенсации недостатка соляной кислоты в желудочном соке применяют её растворы как лекарственные формы. Сколько (мл) 24%-ного раствора HCl с плотностью
1,12 г/мл необходимо для при-готовления 500 г раствора с
массовой долей 5%. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Дано: |
|
|
Решение: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
ρ(p-p1) = 1,12 |
|
|
m(HCl) = |
ω2% m(p-p2) |
|
|
. |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
= 500 0,05 = 25 г. |
|||||||
г/мл |
|
|
|
|
100% |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
m(HCl)100% |
|
|
m(HCl)100% |
|
||||||
ω1%(HCl) = 24% |
|
|
ω1%(HCl) = |
|
= |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
m(p-p 1) |
V(p-p1) ρ(p-p1) |
||||||||||||||
m(p-p 2) = 500 |
|
|
|
|
m(HCl) |
|
|
25 |
|
|
|
|
||||
г |
|
|
V(p-p 1) = |
|
|
|
|
= 93 (мл). |
|
|||||||
|
|
|
|
|
= |
|
|
|
|
|||||||
|
ω |
ρ(p-p1) |
|
0,241,12 |
|
|
||||||||||
ω2%(HCl) = 5% |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
||
|
|
Ответ: 93 мл. |
|
|
|
|
|
|
|
|||||||
V(p-p 1) = ? |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4.Определите массовую долю (в %) HCl в растворе,
полученном при смешивании 50 мл раствора с массовой долей
20% и 20 мл раствора, с массовой долей 10%. |
|
|
||||||
Дано: |
|
Решение: |
|
.ω |
.ρ |
|
||
|
|
|
||||||
V(p-p1) = 50 |
|
1) |
m1(HCl)=m(p-p1) |
(p- |
||||
мл |
|
1(HCl)=V(p-p1) |
|
|||||
|
р |
1) |
.ω |
. . |
|
|
||
ρ(p- |
|
|
1(HCl) = 50 |
1,1 0,2 = 11 (г) |
|
|
||
|
0) |
m2(HCl) = V(p-p 2).ρ(p-p2).ω2(HCl) = |
||||||
p1)=1,1г/мл |
|
|
|
20.1,05.0,1= 2,1 (г) |
|
|
||
ω1%(HCl)= 20% |
|
|
|
|
|
|
|
|
V(p-p 2) = 20 |
|
|
|
|
|
|
|
|
мл |
|
|
|
|
|
|
|
|
|
|
|
|
93 |
|
|
|
|
|
|
|
|
|
|
Приложение |
||
Таблица 3.
Связь между различными способами выражения концентрации растворов.
Способ выражения кон-
центрации,
обозначение,
размерность
Молярная концентрация, С(Х),
моль/л
Молярная концентрация эквивалента
(нормальная концентрация),
С( Z1 X ) или N(X),
моль/л
Титр, t(X), г/мл
Моляльная концентрация,
в(Х) или Сm(X),
моль/кг растворителя
Формула пересчёта
10 ρ(p-p) ω%(X)
M(X)
C 1 XZ
Z
в(Х) m(p-тель)
V(p-p) 10 ρ(p-p) ω%(X)
|
|
|
|
1 |
X |
|
|
||
|
|
M |
|
|
|
||||
|
Z |
|
|||||||
|
|
|
|
|
|
|
|||
|
Z. C(X) |
|
|||||||
|
1000 t(X) |
|
|||||||
|
|
|
|
1 |
X |
|
|
|
|
|
|
M |
|
|
|
||||
|
Z |
|
|||||||
|
|
|
|
|
|
|
|||
|
1 |
|
|
1 |
|
||||
C |
|
|
X M |
|
|
X |
|||
Z |
Z |
||||||||
|
|
|
|
||||||
|
|
|
1000 |
|
|
|
|||
C(X) V(p-p)
m(p-тель)
