
- •Введение
- •История изучения ферментов
- •Классификация
- •Скорость ферментативной реакции. Факторы, влияющие на ферментативную активность
- •Концентрация субстрата
- •Строение ферментов
- •Неорганические ионы (активаторы ферментов)
- •Простетические группы (фад, фмн, биотин, гем)
- •Коферменты (над, надф, кофермент а, атф)
- •Механизм действия ферментов Энергия активации. Принцип действия ферментов
- •Способы увеличения скорости реакции ферментами
- •Активный центр
- •Гипотеза “ключа и замка”. Гипотеза индуцированного соответствия
- •Свойства ферментов
- •Ферментативная кинетика Модель Михаэлиса-Ментен
- •График Лайнуивера-Бэрка в двойных обратных координатах
- •Ингибирование
- •Обратимое ингибирование
- •Конкурентное ингибирование
- •Неконкурентное ингибирование
- •Необратимое ингибирование
- •Аллостерические ферменты
- •Ингибирование конечным продуктом (ингибирование по принципу отрицательной обратной связи — ретроингибирование)
- •Регуляция активности фермента
- •Зимоген
- •Ковалентная модификация
- •Ингибирование по типу отрицательной обратной связи
- •Кооперативные эффекты
- •Симметричная модель
- •Последовательная модель
- •Аллостерическая регуляция
- •Глоссарий
- •Список использованной литературы
Введение
Ферменты — это белковые молекулы, синтезируемые живыми клетками. В каждой клетке имеются сотни различных ферментов. С их помощью осуществляются многочисленные химические реакции, которые могут с большой скоростью идти при температурах, подходящих для данного организма, т. е. в пределах от 5 до 40°С. Чтобы эти реакции с той же скоростью протекали вне организма, потребовались бы высокие температуры и резкие изменения некоторых других условий. Для клетки это бы означало гибель, ибо вся работа клетки строится таким образом, чтобы избежать любых сколько-нибудь заметных изменений в нормальных условиях ее существования. Ферменты, следовательно, можно определить как биологические катализаторы, т. е. как вещества, ускоряющие реакции. Они абсолютно необходимы, потому что без них реакции в клетке протекали бы слишком медленно и не могли поддерживать жизнь.
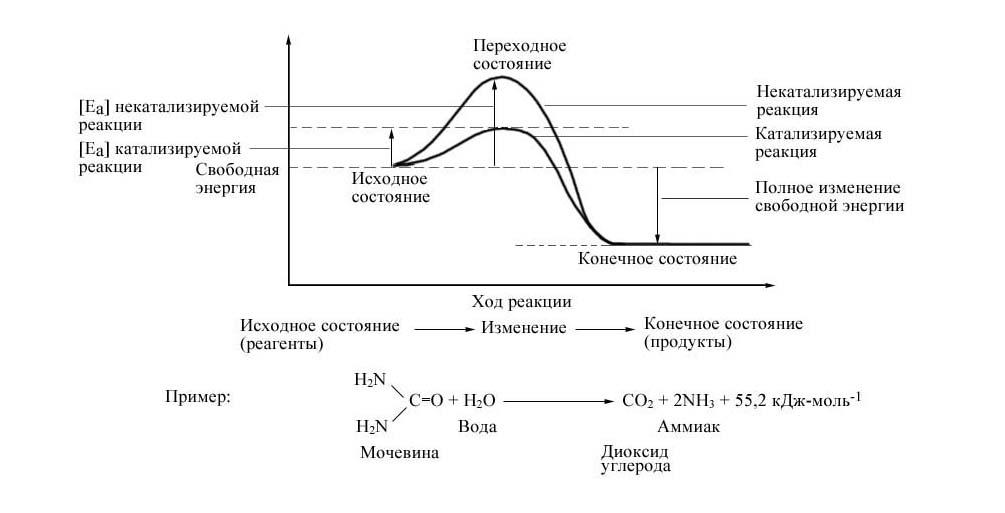
Рис. 1. Энергетические барьеры катализируемой и некатализируемой реакций.
История изучения ферментов
В 1814 году химик К. Г. С. Кирхгоф открыл ферментативное действие водных вытяжек из проросшего ячменя, расщеплявших крахмал до сахара. Можно считать, что эти работы положили начало энзимологии (ферментологии) как самостоятельному разделу биологической химии.
В 1833 году французскими химиками А. Пайеном и Ж. Персо впервые был выделен из солода препарат фермента амилазы, что способствовало развитию препаративной химии Ф.
В середине XIX века разгорелась дискуссия о природе брожения между Л. Пастером, с одной стороны, и Ю. Либихом, П. Э. М. Бертло и К. Бернаром — с другой. Опираясь на свои классические работы, Пастер развивал представление о том, что брожение вызывается лишь живыми микроорганизмами и что процесс брожения неразрывно связан с их жизнедеятельностью. Либих и его сторонники, отстаивая химическую природу брожения, считали, что оно является следствием образования в клетках микроорганизмов растворимых Ф., подобных выделяемой их солода амилазе. Однако все попытки выделить из разрушенных дрожжевых клеток растворимый Ф., способный вызывать брожение, не удавались.
Дискуссия Либиха и Пастера о природе брожения была разрешена в 1897 году Э. Бухнером, который, растирая дрожжи с инфузорной землей, выделил из них бесклеточный растворимый ферментный препарат (названный им амилазой), вызывавший спиртовое брожение. Открытие Бухнера утвердило материалистическое понимание природы брожения и имело большое значение для дальнейшего развития как энзимологии, так и всей биохимии.
В начале XX века Р. Вильштеттер с сотрудниками стал широко применять для выделения и очистки Ф. метод адсорбции. Работы Вильштеттера, имевшие большое значение для характеристики свойств отдельных Ф., привели вместе с тем к принципиально неправильному выводу, что Ф. не принадлежат ни к одному из известных классов органических соединений.
Выдающимся успехом в выяснении химической природы Ф. были исследования американских биохимиков Дж. Самнера, выделившего в 1926 году в кристаллическом виде Ф. уреазу из семян канавалии, и Дж. Нортропа, получившего в 1930 году кристаллы протеолитического Ф. пепсина. Работы Самнера и Нортропа указали путь получения высокоочищенных препаратов Ф. и вместе с тем неопровержимо доказали белковую природу Ф.
В середине XX века благодаря развитию методов физико-химического анализа (главным образом хроматографии) и методов белковой химии расшифрована первичная структура многих Ф. Так, работами американских биохимиков С. Мура, У. Стайна и К. Анфинсена показано, что Ф. рибонуклеаза из поджелудочковой железы быка представляет собой полипептидную цепочку, состоящую из 124 аминокислотных остатков, соединенных в 4-х местах дисульфидными связями.
С помощью рентгеноструктурного анализа расшифрована вторичная и третичная структура ряда Ф. Так, методом рентгеноструктурного анализа английский ученый Д. Филлипс в 1965 году установил трехмерную структуру Ф. лизоцима. Показано, что многие Ф. обладают также четвертичной структурой, т. е. их молекула состоит из нескольких идентичных или различных по составу и структуре белковых субъединиц.
