
- •24). Развитие представлений о природе тепловых явлений. Начала термодинамики. Цикл Карно.
- •25). Проблема необратимости и ее статистическое решение.
- •26).Термодинамический и статистический смысл понятия энтропии.
- •27). Проблема «тепловой смерти» Вселенной: формулировка, развитие и современное решение.
- •28). Динамические и статистические закономерности в естествознании. Особенности описания состояний в динамических и статистических теориях. Проблема детерминизма.
24). Развитие представлений о природе тепловых явлений. Начала термодинамики. Цикл Карно.
Учение о тепловых явлениях стало зарождаться в середине XVII века, когда Галилей изобрел термометр (1600 год). Привычный термометр – 1700 год. 1742 – Цельсий (швед).
Долгое время тепловые явления связывали с перетеканием от одного тела к другому гипотетической субстанции – теплорода. С теорией теплорода конкурировала молекулярно-кинетическая теория, она связывала тепловые движения с движением атомов. Последователи: Бэкон, Декарт, Ломоносов и т.д.
До середины XVIII века господствовала теория теплорода. Позже в опытах было доказано, что тепловой жидкости не существует. Решающий опыт: 1798 – Румфорд.
С 60-ых годов XVIII века началась промышленная революция => поняли, что из теплоты можно получить работу. Необходимо сделать процесс обратимым. Первая машина по превращению теплоты в работу – Уатт. 1807 – первый речной пароход, Роберт Фултон. 1825 – первая железная дорога, паровоз, Джордж Стефенсон.
1824 год. Сади Карно – исследователь по теплу. Рассмотрел идеальную тепловую машину (отсутствовало трение и теплообмен) – поэтому процессы стали обратимыми.
Рабочее тело – газ в цилиндре под поршнем.

2 изотермы, 2 изобаты.
1-2 – рабочее тело получает от нагревателя температуру Тн и теплоту Q1.
2-3 – газ, расширяясь, охлаждается до температуры Тх.
3-4 – газ изотермически сжимают, при этом он отдает холодильнику количество теплоты Q2.
4-1 – газ сжимают до тех пор, пока его температура не станет равной начальной.
![]() - идеальная тепловая
машина.
- идеальная тепловая
машина.
![]() - реальная тепловая
машина.
- реальная тепловая
машина.
К середине XIX
века в трудах Майера, Гельмгольца и
Джоуля было доказано, что теплота и
работа – это две формы, в которых энергия
может переходить от одного тела к
другому. Теплота и работа
![]() энергия. 1 кал = 4,186 Дж
энергия. 1 кал = 4,186 Дж
Все это позволило расширить рамки закона сохранения и превращения энергии.
![]()
Количество теплоты,
переданное телу, идет на превращение
его внутренней энергии U
на совершение системой работ. Суть легче
понять, если
![]() .
Возможны 2 способа передачи энергии: в
виде теплоты А
или энергии Q.
Джоуль получил всеобщий закон природы.
Энергия в природе не возникает и не
исчезает, а только переходит из одной
формы в другую.
.
Возможны 2 способа передачи энергии: в
виде теплоты А
или энергии Q.
Джоуль получил всеобщий закон природы.
Энергия в природе не возникает и не
исчезает, а только переходит из одной
формы в другую.
Начала термодинамики.
Термодинамика рассматривает Тепловые процессы без учета молекулярного строения тела, ничего не говорит о механизме, а только устанавливает связи между макроскопическими свойствами вещества.
Состав т/д системы = (p, t, v).
Идеализированный объем т/д – это макроскопическая система в состоянии теплового равновесия (все т/д параметры не меняются со временем).
В основе т/д – различие между обратимыми и необратимыми процессами.
Обратимый – это процесс перехода т/д системы из одного состояния в другое, допускающий возможность возвращения в исходное состояние через ту же последовательность промежуточных состояний, что и в прямом процессе.
Необратимый – это процесс, который может самопроизвольно протекать только в одном направлении. Пример: диффузия (где есть перенос чего-либо).
Классическая т/д системы, близкие к равновесию и обратимые процессы. Связи между величинами однозначны => т/д – динамическая теория.
Начала т/д.
Всякая предоставленная самой себе замкнутая система стремится перейти в состояние теплового равновесия, из которого самопроизвольно выйти уже не может. Двигатель, работающий только за счет энергии тел, находящийся в состоянии теплового равновесия, был бы вечным двигателем (2-ого рода), такой двигатель не возможен. Работа превращается в теплоту полностью, а теплота в работу – лишь частично.
1865 год – Клаузиус – особая функция состояния системы (энтропия).
2-ой закон т/д в принципе нельзя доказать.
Если система в
результате обратимого процесса получает
тепло
![]() с температурой Т1,
то энтропия системы увеличивается на
величину
с температурой Т1,
то энтропия системы увеличивается на
величину
![]() - т/д определение энтропии.
- т/д определение энтропии.
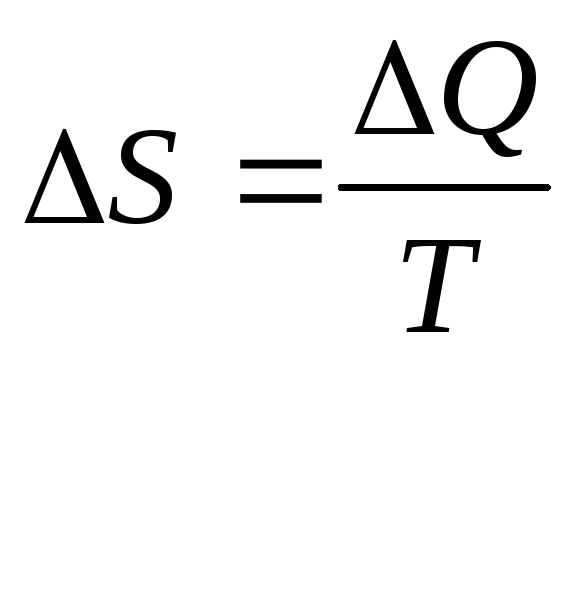
![]()
![]()
![]()
Энтропия замкнутой
системы в случае обратимых процессов
не меняется. Необратимые процессы
![]() - возрастает.
- возрастает.
![]()
![]()
Пример: при
перетекании тепла от более горячего к
более холодному энтропия системы
возрастает. Таким образом, энтропия
замкнутой системы при необратимых
процессах может только возрастать
![]() .
.
Математическая формулировка второго начала т/д: энтропия возрастает до тех пор, пока не наступит тепловое равновесие, при котором энтропия максимальна.
