
- •Способы выражения концентраций растворов Теоретическая часть
- •V(X) – объем раствора, (мл);
- •1.Вычислить массовую долю (%) NaNo3, полученного растворением 7,5г вещества в 42,5 г воды?
- •2. Сколько граммов воды и соли потребуется для приготовления 250 г раствора с массовой долей 15%?
- •3.Сколько граммов хлорида аммония потребуется, чтобы приготовить 1.6 кг раствора с массовой долей 10%?
- •4.Сколько граммов воды потребуется для растворения 12 г хлорида натрия, чтобы получить раствор с массовой долей 5%?
- •1. Рассчитать массовую долю кристаллизационной воды в молекуле медного купороса.
- •1.Приготовление растворов с известной массовой долей
- •2.Определение массовой доли кристаллизационной воды
- •3.Молярная концентрация эквивалента.
Способы выражения концентраций растворов Теоретическая часть
Концентрацией называют величину, измеряемую количеством растворенного вещества, содержащееся в определенной массе или объеме раствора или растворителя.
Массовая доля (ω) выражает отношение массы растворенного вещества (m1) к общей массе раствора (m):
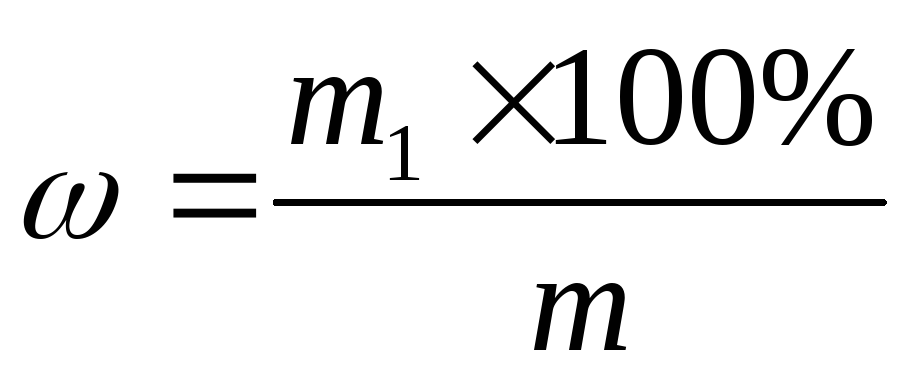
Массовая доля – количество граммов растворенного вещества в 100 г раствора.
Выражается в долях или процентах.
Молярная концентрация показывает, число молей растворённого вещества в одном литре раствора.
Обозначается C(x) и рассчитывается по формуле:
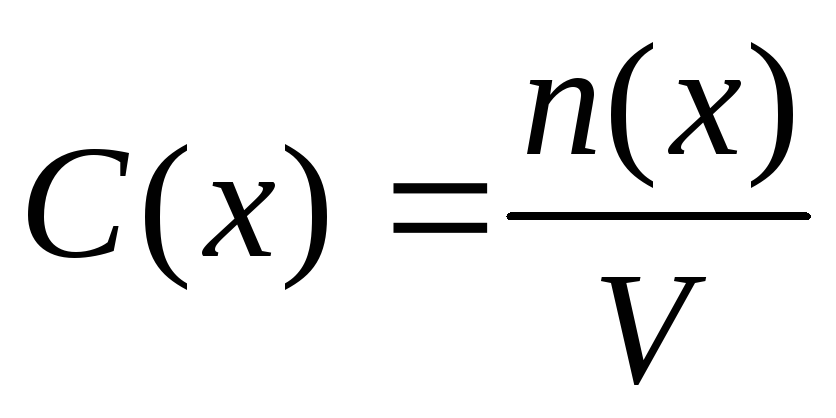 ;
где
;
где
-
C(x) – молярная концентрация, (моль/л);
-
n(x) – количество растворенного вещества, (моль);
-
V – объем раствора, (л).
При приготовлении молярных растворов расчет твердого вещества, кристаллогидрата проводят по формуле:
 ;
где
;
где
-
m – навеска, (г);
-
C(x) – молярная концентрация раствора, (моль/л);
-
M(x) – молярная масса вещества, (г/моль);
-
V(x) – объем раствора, (мл);
-
1000 мл – объем раствора.
Если раствор готовят из концентрированного раствора, то объем его рассчитывают по формуле:
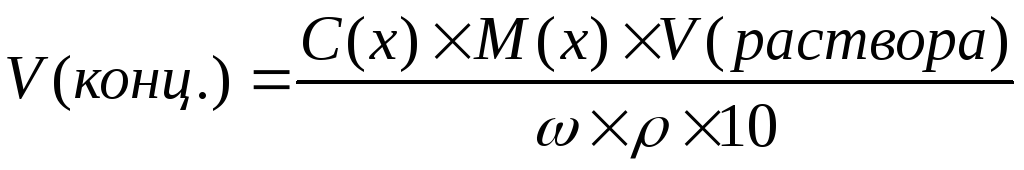 ;
где
;
где
-
C(x) – молярная концентрация раствора, (моль/л);
-
M(x) – молярная масса вещества, (г/моль);
-
V(X) – объем раствора, (мл);
-
ρ – плотность раствора, (г/мл);
-
ω – массовая доля, (%);
-
V(конц) – объем концентрированного раствора, (мл);
-
10 – пересчетный коэффициент.
Молярная концентрация эквивалента показывает, число моль эквивалентов растворённого вещества в одном литре раствора.
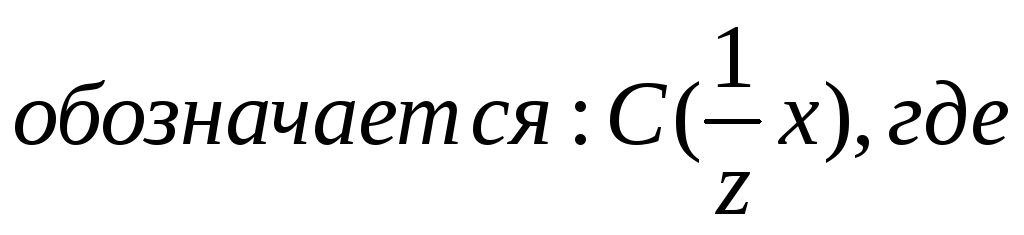
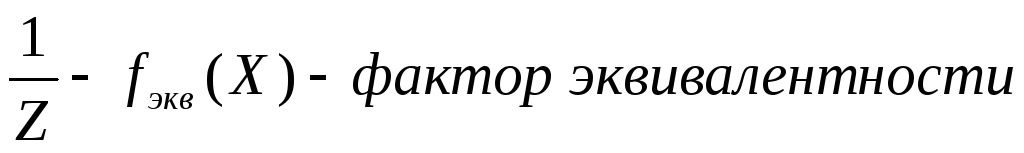
Эквивалент – это реальная или условная частица, которая может присоединить или вытеснить 1 протон водорода в кислотно-основных реакциях или быть эквивалентной 1 электрону в окислительно-восстановительных реакциях.
Фактор эквивалентности ( fэкв.) – это число, показывающее, какая доля реальной частицы вещества эквивалентна одному иону водорода в данной кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции.
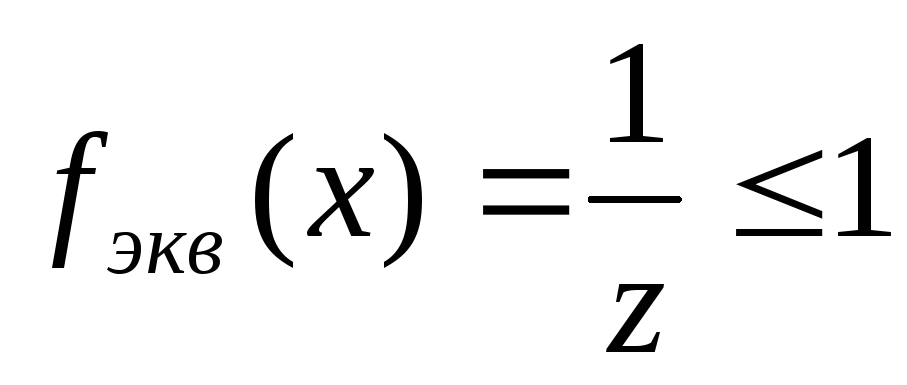
Молярная масса эквивалента вещества x – это масса одного моля эквивалента этого вещества. Она равна произведению фактора эквивалентности вещества в реакции на молярную массу вещества (x):
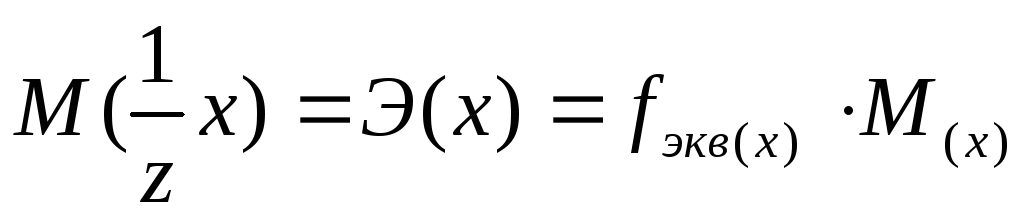
Молярная масса эквивалента кислоты равна её молярной массе, делённой на основность кислоты (если расчёт производят по формуле):
![]()
Фактор эквивалентности кислоты – величина обратная числу катионов водорода
![]()
*при расчёте по уравнению реакции учитывают стехиометрические коэффициенты реакции:
Пример: 2 NaOH + H2SO4 = Na2SO4 + 2 H2O
1 моль гидроксида натрия эквивалентен 0,5 моль серной кислоты. Следовательно, молярная масса эквивалента гидроксида натрия 40 г/моль, то молярная масса эквивалента серной кислоты для этой реакции:
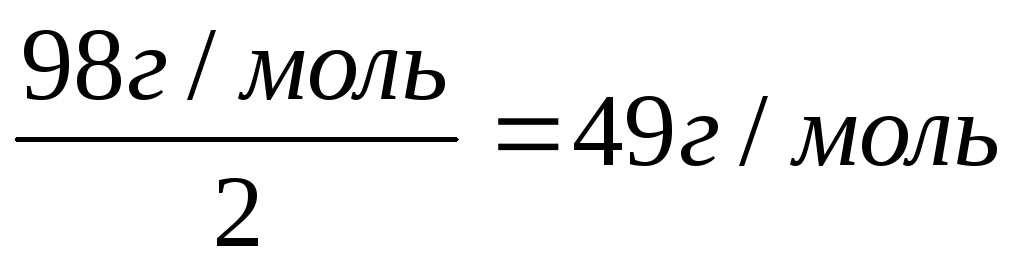
Для уравнения реакции: NaOH + H2SO4 = NaHSO4 + H2O
1 моль гидроксида натрия эквивалентен 1 молекуле серной кислоты, следовательно, молярная масса эквивалента серной кислоты для данной реакции равна 98 г/моль.
Фактор эквивалентности основания – величина обратная числу гидроксильных групп
Молярная масса эквивалента соли равна молярной массе соли, делённой на произведение степени окисления иона металла и числа его ионов в молекуле соли:
![]()
Фактор эквивалентности соли – величина обратная произведение степени окисления иона металла и числа его ионов в молекуле соли
Молярная масса эквивалента окислителя (восстановителя) равна молярной массе окислителя (восстановителя) делённой на число электронов, принятых или отданных одной молекулой данного вещества:
![]()
Фактор эквивалентности окислителя (восстановителя) – величина обратная числу электронов, принятых или отданных одной молекулой данного вещества:
KMnO4 – окислитель, присоединяет 5 электронов
MnO 4 - + 8 H + +5ẻ → Mn2+ + 4 H2O (окислитель)
Для приготовления растворов с молярной концентрацией эквивалента расчёт навески сухого вещества проводят по формуле:
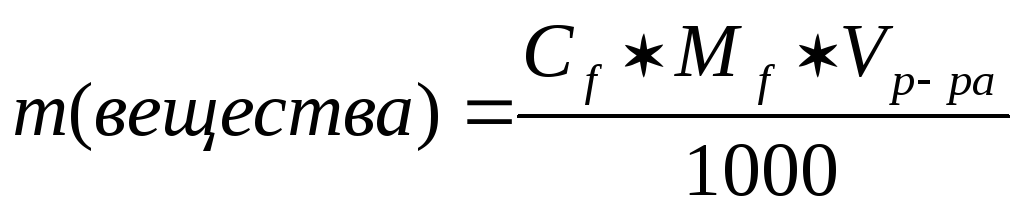 ,
где
,
где
-
Сf _ молярная концентрация эквивалента раствора (моль/л)
-
Мf _ молярная масса эквивалента (г/моль)
-
V раствора _ объём раствора (мл)
-
m _ навеска вещества (г).
-
|
1.Приготовление растворов с известной массовой долей. |
Обучающие задачи |
