
Тема 4. Молекулярно-поверхностные свойства
СИСТЕМЫ НЕФТЬ – ГАЗ – ВОДА – ПОРОДА
-
Молекулярные взаимодействия в веществах.
- Характер молекулярного взаимодействия зависит от природы вещества. При нормальных расстояниях между молекулами вещества (при нормальных давлении и температуре) взаимодействие молекул выражается в притяжении их друг к другу. При сильном сближении молекул возникают силы отталкивания
-
Растворимость и нерастворимость жидкостей.
- Пусть молекулы жидкости В сильнее притягиваются к молекулам жидкости А, чем между собой. Тогда любое случайное скопление молекул В (рис. 35) окажется недолговечным — молекулы жидкости А «растащат» молекулы жидкости В. Жидкость В является в данном случае полностью растворимой в жидкости А.
Если же взаимное притяжение молекул жидкости В намного больше притяжения молекул жидкости В к молекулам жидкости А или если между этими разносортными молекулами существуют силы отталкивания, то скопление молекул жидкости В, находящихся в жидкости А, будет устойчивым. Такие жидкости называются взаимно нерастворимыми или несмешивающимися. Следовательно, характер взаимодействия молекул различных веществ определяет их взаимную растворимость.
-
Поверхностное натяжение.
- Поверхностное натяжение (σ) характеризует избыток свободной энергии, сосредоточенной на одном квадратном сантиметре площади поверхностного слоя на границе раздела двух фаз или работу образования новой поверхности в изотермических условиях:
![]() .
(5.3)
.
(5.3)
Величину коэффициента поверхностного натяжения можно определить как величину работы, необходимой для образования 1 см2 новой поверхности (Дж/м2, Н/м)
-
Зависимость поверхностного натяжения пластовых жидкостей от давления и температуры.
- Поверхностное натяжение с увеличением давления понижается, тем сильнее, чем ниже температура. Поверхностное натяжение уменьшается с повышением температуры
-
Смачивание и краевой угол.
Смачиванием называется совокупность явлений на границе соприкосновения трёх фаз, одна из которых обычно является твёрдым телом и две другие – несмешиваемые жидкости или жидкость и газ.
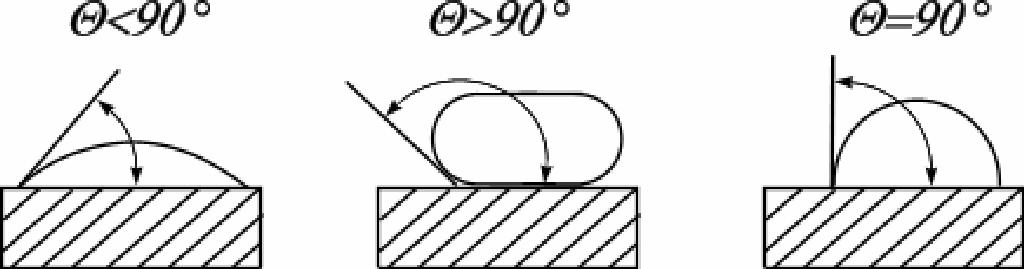
Гидрофильная Гидрофобная Нейтральная
-
Полярность веществ.
- Высокополярные жидкости, т. е. жидкости с высоким поверхностным натяжением, хуже смачивают твердую поверхность, чем жидкости малополярные (т. е. обладающие меньшим поверхностным натяжением)
-
Адгезия и теплота смачивания.
- Адгезия – слипание поверхностей двух соприкасающихся разнородных твердых или жидких тел (в физике).
Когезия (от лат. cohaesus - связанный, сцепленный) — сцепление друг с другом частей одного и того же тела (жидкого или твердого). Обусловлена химической связью и межмолекулярным взаимодействием.
Работа адгезии оценивается уравнением Дюпре:
Wa = σ1,2 + σ2,3 – σ1,3,, (5.6)
где σ12 — поверхностное натяжение жидкости на границе с воздухом
σ32 и σ31 — поверхностное натяжение твердого тела на границе с воздухом и с жидкой фазой.
- Теплота смачивания характеризует степень дисперсности твердого тела и природу его поверхности. Большее количество тепла выделяется при смачивании той жидкостью, которая лучше смачивает твердую поверхность.
