
Нижегородский государственный технический университет
имени Р.Е. Алексеева
Кафедра «Технология электрохимических производств»
Лабораторная работа №6 « исследование процесса электролиза водных растворов NaCl в диафрагменном электролизере с проточным электролитом»
Выполнил: ст. гр. 07-ТЭП
Бекетов С.С.
Проверил: Гунько Ю.Л.
Н.Новгород
2011 г
Введение
Основная масса хлора и щелочи получается электролизом водных растворов NaCl в ваннах трех типов: диафрагменных, мембранных (аналог диафрагменных) и ртутных. В электролизерах первого типа катодом служит стальная сетка, анодом — графитовые стержни (или оксидно-рутениево-титановые электроды); катодное пространство отделено от анодного асбестовой диафрагмой. Последняя разделяет катодный и анодный газы, щелочной католит и кислый анолит. Диафрагма, препятствуя диффузии и конвекции в электролите, не устраняет однако попадание ионов ОН' в анодное пространство путем миграции в процессе электролиза. В результате такой миграции будет происходить взаимодействие катодного и анодного продуктов (щелочи и хлора), что приведет к понижению выходов по току для этих веществ и загрязнению получающейся щелочи хлоратом. Попадание ионов гидроксила в анодное пространство при их миграции устраняется путем непрерывной подачи рассола в это пространство и протекания его через диафрагму со скоростью, большей скорости встречной миграции ионов ОН'. Для того, чтобы получить вытекающие щелока более концентрированными по щелочи, скорость подачи рассола держат по возможности меньшей, когда скорости встречных процессов миграция ионов ОН' и протекания рассола близки друг к другу.
Во всех случаях выход по току для хлора и щелочи не достигают 100%. Одной из причин этого является частичное попадание хлора в катодное пространство. Хлор, растворенный в анолите, попадает вместе с ним в катодное пространство, где, реагируя со щелочью, дает хлораты. Эти соединения частично восстанавливаются на катоде, а частично выводятся вместе со щелоками.
Экспериментальная часть
Цель работы: определить средний выход по току для хлор-газа и щелочи (через 0,5 часа) при электролизе раствора NaCl 50г/л (анолит) и NaOH 5% (католит) при мембранном электролизе при токе I = 3A. Скорость протока через анолит и католит из расчета 17 капель в минуту. Время электролиза 1,5 часа.
Анодная часть электролизера представляет собой сосуд из оргстекла. На его верхней крышке укреплен анод; здесь же имеются отверстия для вывода хлора и подачи рассола. Поступление рассола осуществляется через жидкостной затвор во избежание выхода хлора. Боковой стороной анодный сосуд прижимается к катодному комплекту с последовательным расположением в нем диафрагмы и никелевой сетки, которая является катодом.
Катодный комплект закрепляется во внешнем сосуде электролизера, в котором собираются образующиеся щелока. Верхний слив во внешнем сосуде служит для вывода щелоков. Выделяющийся водород удаляется в атмосферу. Хлороотвод в ходе опыта должен быть постоянно погружен на определенную глубину в поглотительную склянку с раствором щелочи. Выходной наконечник поглотительной склянки соединить с водоструйным насосом для создания необходимого разряжения на линии хлороотвода, для барботирования хлора в поглотительной склянке. На линии хлоропровода от электролизера до поглотительной склянки необходимо создать подсос воздуха во избежание захвата анолита и протекания его в поглотительную склянку (на линии поставлена трубка с отверстием, через которое и осуществляется подсос воздуха).
Электролизер заполняется рассолом до полного покрытия анода раствором (концентрация исходного рассола, скорость его протекания через электролизер, электродная плотность тока и продолжительность опыта—по заданию руководителя). Необходимая токовая нагрузка на электролизер рассчитывается на поверхность анода. В поглотительную склянку заливается 5Н раствор NaOH. После подготовки установки к опыту, начинается подача рассола с заданной скоростью; включается водоструйный насос и, после установления режима, включается ток нужной силы.

Рисунок 1 - Электролизер и электрическая схема работы.
Аn — анод; Кt — катод; Д — диафрагма; Пщел, — приемник щелоков; Пхл—поглотительная склянка для хлора; Р- емкость с рассолом; А — амперметр; V—вольтметр; СИПТ- стабилизированный источник постоянного тока.
Записывается начальное напряжение на ванне; затем напряжение записывается через каждые 0,5 час. За 5 -10 минут до окончания каждого периода склянка с собранными щелоками заменяется на новую. Собранный за это время электролит соответствует составу электролита в катодном пространстве электролизера (католит).
После каждого 0,5 – 1 часа опыта отбирают собранные щелока к ставится новая склянка для их сбора. Измеряется объем щелоков и проводится их анализ на щелочь и активный хлор и одновременно – анализ на щелочь и активный хлор католита.
По окончании опыта измерить объем раствора в поглотительной склянке и анализируется на содержание активного хлора (по методике приложения) для расчетов параметров электролиза анодного процесса.
Средний выход по току для щелочи ВтNaOH рассчитываем по формуле:
![]() (1)
(1)
где GNaOH – количество щелочи, полученной за все время опыта, г;
I – сила тока, А;
t– время, 1 ч;
q – электрохимический эквивалент NaOH, г/А·ч.
Удельный расход электроэнергии для отдельных периодов опыта и средний определяется по формуле:
![]() (2)
(2)
где Vср – среднее напряжение на ванне, В;
Bт – выход по току, %.
Среднее напряжение на ванне Vcp рассчитывается как среднее арифметическое из его промежуточных значений.
Vср = (V1 + V2 + ... + Vn ) / n (3)
где: n – число замеров
Расчеты параметров электролиза по хлору проводят по формулам аналогичным данным выше для расчетов по щелочи.
Концентрация анолита NaCl = 50 г/л
Концентрация католита NaOH = 5%
Расчет токовой нагрузки на электролизер:
I=j·S (4)
где j – плотность тока, А/см2;
S – площадь электрода, см2
I=3 А
Таблица 1 - Экспериментальные данные
-
t, мин
U, В
0
6,4
25
5,6
30
5,4
55
5,3
60
5,2
85
5
90
4,9
Vср = (66.4+5.6+5.4+5.3+5.2+5+4.9) / 7 = 5.4В
Построим зависимость напряжения на электролизере от времени электролиза (рисунок 2)
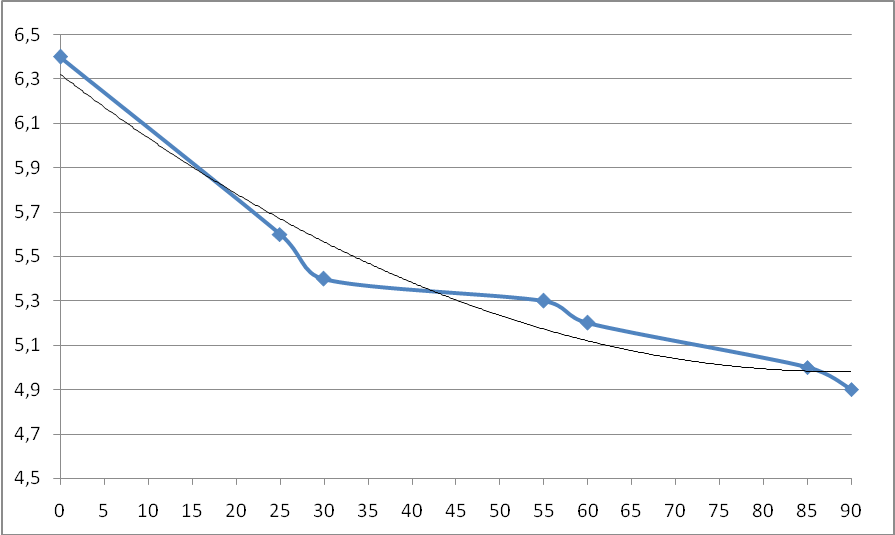
Рисунок 2 - Зависимость напряжения на электролизере от времени электролиза
1 Расчет среднего выхода по току для щелочи
V1 NaOH = мл – объем щелочи в сборнике;
V2 NaOH = мл – объем католита;
V1 НСl = мл – объем соляной кислоты, пошедший на титрование аликвотной доли щелочи из сборника;
V2 НСl = мл – объем соляной кислоты, пошедший на титрование аликвотной доли католита.
Концентрацию щелочи в полученных растворах рассчитываем по формуле:
![]() ,
г/л (5)
,
г/л (5)
где: VHCl - объём 0,1Н НСl, пошедший на титрование раствора, мл;
NHCl = 0,1Н – нормальность раствора соляной кислоты;
VNaOH = 1 мл – объем аликвотной доли раствора щелочи, взятого на титрование;
МNaOH = 40 г-экв/л – эквивалентная масса NaOH.
![]()
![]()
Общее количество щелочи, полученное за все время опыта, можно рассчитать по формуле:
GNaOH = [С1 NaOH·V1 NaOH+ С2 NaOH·V2 NaOH- С0 NaOH·(V1 NaOH+V2 NaOH)]·10-3
где: С0 NaOH – исходная концентрация раствора NaOH, 5% или 50г/л
GNaOH =[70*14.5+15.5*75.6-(50*30)]·10-3 = 2.037 г
Выход по току рассчитываем по формуле (1)
![]()
2 Расчет среднего выхода по току для хлор-газа
V = 120 мл – объем поглотительной щелочи;
a = 14.4 мл – объем раствора Na2S2O3, пошедший на титрование аликвотной доли щелочи из сборника;
Концентрация активного хлора СCl2 в щелочи поглотительной склянке рассчитывается по формуле:
![]() (6)
(6)
где: а—объем 0,1 Н Na2S2O3, пошедший на титрование пробы, мл;
0,003546—титр 0,1Н раствора гипосульфита по хлору, г/мл.
![]()
Количество всего поглощенного хлора gCl2 (г), будет равняться
gCl2 = CCl2 · V, (7)
где: V — объем щелочи в поглотительной склянке, л.
gCl2 = CCl2 · V = 25.53·0,12 = 3.067 г
Выход по току для хлор-газа рассчитываем по формуле (1)
![]()
3 Расчет удельного расхода электроэнергии
![]()
![]()
Опытные и расчетные данные для щелочи приводим в таблице 2, для хлора – в таблице 3.
Таблица 2 - Параметры электролиза по щелочи
|
Время опыта, мин |
Количество протекшего электричества, А·ч |
Среднее напряжение, В |
Объём щелоков, мл |
мл 0,1Н HCl, пошедшего на титрование 1мл щелочи |
NaOH в сборнике |
NaOH в католите |
ВтNaOH, % |
Wр, кВт·ч/т |
||||
|
сборник |
католит |
из сборника |
католита |
г/л |
г |
г/л |
г |
|||||
|
90 |
|
5,4 |
|
|
|
|
70 |
|
75.6 |
|
30 |
12080 |
Таблица 3 - Параметры электролиза по хлору
|
Время опыта, мин |
Количество протекшего электричества, А·ч |
Среднее напряжение, В |
мл 0,1Н раствора Na2S2O3, пошедшего на титрование 1мл поглотительной щелочи |
Концентрация активного хлора в поглотительной щелочи, г/л |
Количество выделенного хлора (общее), г |
ВтСl2, % |
Wр, кВт·ч/т |
|
90 |
|
5,4 |
14.4 |
25.53 |
3.07 |
52 |
7867 |
