
1-1.Хлороводородная кислота HClO3
1-2.Серная кислота H2SO4
1-3.Азотная кислота – вещество г) HNO3
1-4.Ортофосфорная кислота б) H3PO4
1-5. Гидроксид натрия б) NaOH
1-6. Сернистая кислота б) H2SO3
1-7. Сероводородная кислота а) H2S
1-8. Метафосфорная кислота а) HPO3
1-9. Двухосновными кислотами являются а) H2S2O7 е) H2S
1-10. Бескислородными кислотами являются HСl H2S
1-11. Солями являются г) NaHCO3 в) K2CO3 и) CuOHCl
1-12.Кислые соли г) NaHCO3 е) Ca(HS)2
1-13. Основные соли а) Fe(OH)2NO3 и) CuOHCl
1-14.Основания б) NaOH ж) Cu(OH)2
1-15. Щелочи б) NaOH в) KOH е) Ba(OH)2
1-16. Соответствие между названием вещества и его формулой
1) |
Ортофосфорная кислота |
а) |
H3PO4 |
2) |
Карбонат натрия |
б) |
Na2CO3 |
3) |
Гидроксид железа (II) |
в) |
Fe(OH)2 |
4) |
Гидрокарбонат натрия |
г) |
NaHCO3 |
1-17. Соответствие между формулой вещества и его названием:
1) |
Na2SO4 |
а) |
сульфат натрия |
2) |
H2SO4 |
б) |
серная кислота |
3) |
NaHCO3 |
в) |
гидрокарбонат натрия |
|
|
|
|
1-18. Реакцией нейтрализации будет
б) NaOH + HNO3 " NaNO3 + H2O
1-19. Формулы кислотных оксидов б) SiO2 в) CO2 е) NO2
1-20. Щелочи а) NaOH в) LiOH д) Ba(OH)2
1-21. Бескислородные кислоты а) HF г) HCN д) HBr
1-22. Амфотерными называются соединения, которые способны реагировать в) и с кислотами, и со щелочами
1-23. Химические соединения NaNO3, KCl, CaCO3 относятся к б) средним солям
1-24. Соответствие оксидов и кислот:
1) |
SO3 |
а) |
H2SO4 |
2) |
P2O5 |
б) |
H3PO4 |
3) |
CO2 |
в) |
H2CO3 |
4) |
SO2 |
г) |
H2SO3 |
1-25. Соответствие формул солей и названий:
1) |
Na2CO3 |
а) |
карбонат натрия |
2) |
KCl |
б) |
хлорид калия |
3) |
LiNO3 |
в) |
нитрат лития |
4) |
(NH4)2SO4 |
г) |
сульфат аммония |
1-26. Неэлектролитами являются а) SO3 д) CuO е) Fe2O3
1-27. Электролитами являются б) KOH г) NaHCO3 ж) HClO4 з) HPO3
1-28. Уравнение полной диссоциации H3PO4 в) H3PO4 D 3H+ + PO43–
1-29. Уравнение реакции нейтрализации в) H2SO4 + 2NaOH = Na2SO4 + 2H2O
1-30. Амфотерное соединение в) Zn(OH)2
1-31. Формулы основных солей: а) CaOHCl в) Al(OH)2NO3
1-32. Молекулярному уравнению реакции KCl + AgNO3 = AgCl $+ KNO3 соответствует сокращенное ионное уравнение б) Cl– + Ag+ = AgCl
1-33. Молекулярному уравнению реакции CuO + 2HNO3 = Cu(NO)2 + H2O
соответствует сокращенное ионное уравнение: в) CuO + 2H+ = Cu2+ + H2O
1-34. Молекулярному уравнению реакции Zn(OH)2$ + H2SO4 = ZnSO4 + 2H2O соответствует сокращенное ионное уравнение г) Zn(OH)2 + 2H+ = Zn2+ + 2H2O
1-35. Сумма коэффициентов в сокращенном ионном уравнении реакции Zn(OH)2$ + H2SO4 = ZnSO4 + 2H2O равна в) 6
1-36. Сумма коэффициентов в сокращенном ионном уравнении реакции
CuO + 2HNO3 = Cu(NO)2 + H2O а) 5
1-37. Сумма коэффициентов в сокращенном ионном уравнении реакции
Na2CO3 + 2HNO3 = 2NaNO3 + CO2# + H2O б) 5
1-38. Соединения, принимающие участие в процессе
FeS$ + 2HCl = FeCl2 + H2S, которые в ионном уравнении реакции записываются в молекулярном виде д.) FeS$ и H2S
1-39. Соединения, принимающие участие в процессе
CaCO3$ + 2HNO3 = Ca(NO)2 + CO2# + H2O, которые в ионном уравнении реакции записываются в молекулярном виде г) CaCO3$ , CO2# и H2O
1-40. Сумма коэффициентов в полном ионном уравнении, соответствующем реакции Ca(NO3)2 + Na2CO3 = CaCO3$ + 2NaNO3 б) 11
1-41. Сумма коэффициентов в сокращенном ионном уравнении, соответствующем реакции CO2 + 2NaOH = Na2CO3 + H2O г) 5
1-42. Сумма коэффициентов в полном ионном уравнении, соответствующем реакции CO2 + 2NaOH = Na2CO3 + H2O в) 9
1-43. Реакции нейтрализации соответствует сокращенное ионное уравнение: а) H+ + OH– = H2O
Тема 2. Термодинамика и направленность химических реакций.
2-1. Стандартным условиям соответствуют г) Т = 298К, p = 101325 Па, n = 1 моль
2-2. Термодинамическими функциями являются а) H – энтальпия в) S– энтропия г) U – внутренняя энергия
2-3. Стандартная размерность энтальпии г) кДж/моль
2-4. Стандартная размерность энергии Гиббса г) кДж/моль
2-5. Уравнение 1-го закона термодинамики б) Q = DU + АВНЕШ
2-6. Функцию «энтальпия» определяет выражение г) H = U – pV
2-7. Эндотермическим процессам отвечает неравенство: в) DHХР > 0
2-8. Изолированные системы а) не обмениваются ни веществом, ни энергией с окружающей средой
2-9. Открытые системы в) обмениваются и веществом, и энергией
2-10. Система – это группа тел, которые в) находятся во взаимодействии и мысленно или фактически обособлены от окружающей среды
2-11. Функция состояния системы зависит от а) параметров состояния
2-12. Реакции, протекающие с поглощением теплоты, называются... б) эндотермические
2-13. Энтальпией образования вещества называется тепловой эффект ... в) образования сложного вещества из простых веществ, устойчивых при стандартных условиях
2-14. Энтальпией сгорания вещества называется тепловой эффект реакции
сгорания б) 1 моль вещества с образованием высших оксидов в кислороде при стандартных условиях
2-15. Изохорный процесс протекает при постоянном в) объеме
2-16. Изобарный процесс протекает при а) постоянном давлении
2-17. Тепловой эффект реакции, в соответствии с законом Гесса, зависит от
б) конечного и начального состояний системы, но не зависит от пути проведения процесса
2-18. Теплота, подводимая к системе, расходуется на изменение внутренней энергии в
а) изохорном процессе
2-19. Самопроизвольное протекание процесса в изолированной системе, в соответствии со 2-м законом термодинамики, сопровождается а) возрастанием энтропии
2-20. Самопроизвольное протекание процесса в неизолированной системе сопровождается в) уменьшением энергии Гиббса
2-21. Условием равновесия является г) неизменность энергии Гиббса
2-22. Теплотой образования CO2 является тепловой эффект реакции в) C(Т) + O2(Г) = CO2(Г)
2-23. Экзотермической является реакция в) Ca(Т) + O2(Г) = CaO(Т); DH = –645,6 кДж
2-24. Первое следствие из закона Гесса: тепловой эффект химической реакции равен
б) разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ
2-25. Второе следствие из закона Гесса: тепловой эффект химической реакции равен
а) разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов реакции
2-26. Изменение энтальпии реакции сгорания метана CH4 + 2O2 = CO2 + 2H2O рассчитывается по уравнению б)
2-27. Изменение энтальпии при сгорании ацетилена рассчитывается по уравнению 2C2H2 + 5O2 = 4CO2 + 2H2O; DH – ? б)
2-28. Энтропия при протекании реакции 4NH3(Г) + 3O2(Г) = 2N2 (Г) + 6H2O(Ж)б) уменьшается
2-29. Энтропия при протекании реакции 2SO2(Г) + O2(Г) = 2SO3(Г) б) уменьшается
2-30. Изменение энтальпии реакции:
C2H5OH(Ж) + CH3COOH(Ж) = CH3COOC2H5(Ж) + H2O(Ж)
[; ;
; ] б) +13 кДж
2-32. Энтальпия образования HCl составляет ... кДж/моль, если при протекании реакции H2(Г) + Cl2(Г) = 2HCl(Г) выделяется 92,31 кДж в) 46,155
2-33. Изменение энтальпии реакции C6H6(Ж) + 7,5O2(Г) = 6CO2(Г) + 3H2O(Г) равно:
[; ; ]
в) –3133 кДж/моль
2-34. Условие, характеризующее самопроизвольность протекания процессов в неизолированной системе г) DG < 0
2-35. Условие, характеризующее самопроизвольность протекания процессов в изолированной системе: в) DS < 0
2-36. Изменение энергии Гиббса при протекании химической реакции вычисляется по формуле: г)
2-37. Формула для расчета изменения энтропии: б)
2-38. Самопроизвольные процессы в изолированной системе сопровождаются б) увеличением энтропии
2-39. Самопроизвольные процессы в неизолированной системе сопровождаются а) уменьшением энергии Гиббса
2-40. Энергия Гиббса является функцией состояния, и ее изменение равно в) разности между суммой энергий Гиббса конечных веществ и суммой энергий Гиббса начальных веществ
2-41. Энтропия является функцией состояния, и ее изменение равно в) разности между суммой энтропий конечных веществ и суммой энтропий начальных веществ
2-42. Качественно определите: энтропия при протекании реакции
N2(Г) + O2(Г) = 2NO(Г) б) не изменится
2-43. Соответствие между словами и цифрами
S
Т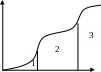
1) |
твердое |
а) |
1 |
2) |
жидкое |
б) |
2 |
3) |
газообразное |
в) |
3 |
2-44. Качественно определите изменение энтропии при протекании реакции 2C4H10(Г)+13O2(Г) = 8CO2(Г)+10H2O(Г) а) DS > 0
2-45. Реакции, протекающие самопроизвольно в обратном направлении:
а) CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г); DG = 170,63 кДж
б) Fe2O3(Т) + 3H2(Г) D 2Fe(Т) + 3H2O (Г), DG = 55,28 кДж
2-46. Самопроизвольно в системе Fe2O3(Т) + 3H2(Г) D 2Fe(Т) + 3H2O (Г), DG = 55,28 кДж.
будет протекать б) обратная реакция
2-47. Прямая реакция протекает самопроизвольно, если изменение свободной энергии Гиббса равно а) DGХР = –190 кДж/моль
2-48. Качественно определите: энтропия при протекании реакции
2C(Т) + 3H2(Г) = C2H6(Г) г) уменьшится
